Clear Sky Science · es
La ribonucleasa 4 desempeña funciones en la homeostasis nerviosa mediada por nociceptores
Por qué esto importa para las personas que viven con dolor
Los nervios del dolor suelen verse como mensajeros simples que alertan cuando algo duele. Este estudio revela que algunas de esas neuronas sensibles al dolor, llamadas nociceptores, gestionan de forma silenciosa la salud de las fibras nerviosas cercanas. El trabajo se centra en una molécula poco conocida, la ribonuclease 4 (RNase4), y muestra que ayuda a mantener bajo control las señales de dolor al tiempo que guía cómo los nervios dañados se descomponen y se reconstruyen. Comprender este doble papel podría abrir nuevas vías para tratar el dolor crónico y mejorar la reparación nerviosa tras una lesión.
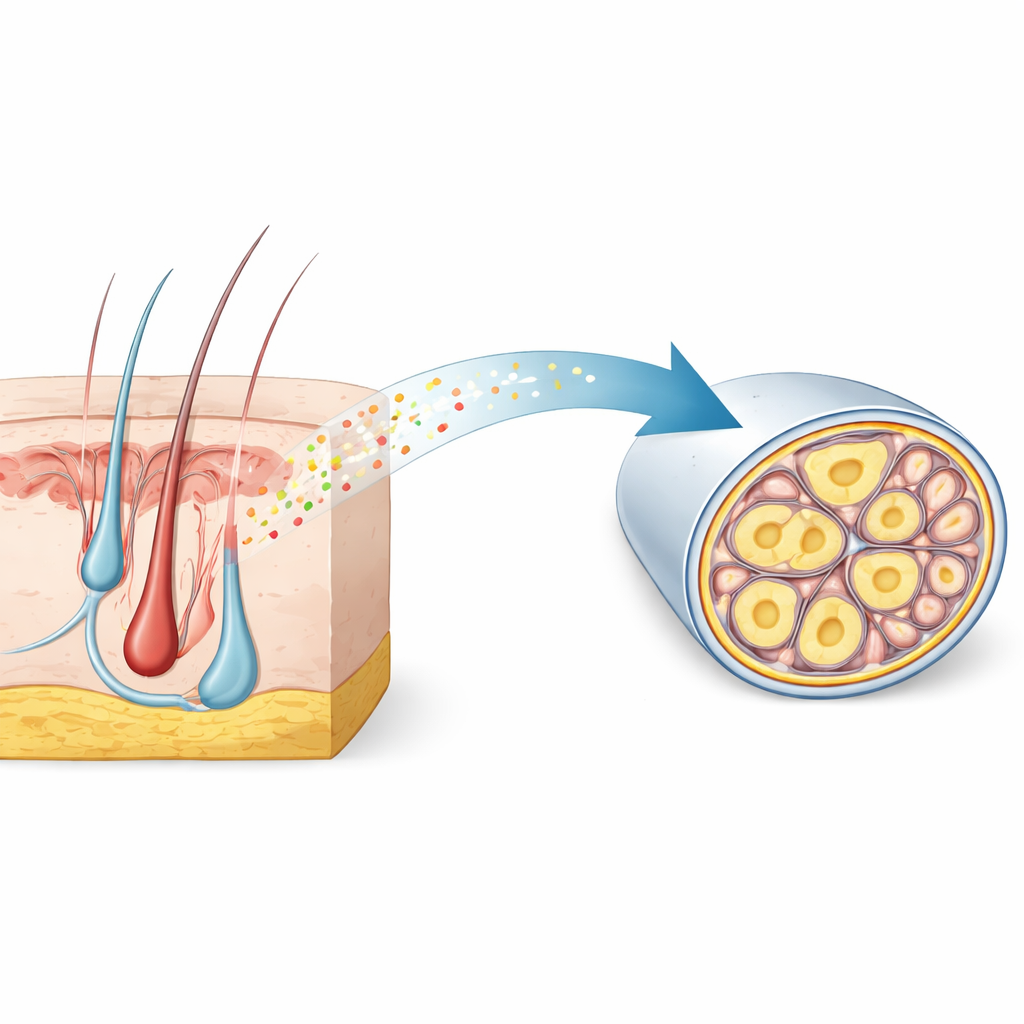
Una firma oculta dentro de los nervios que detectan el dolor
Los investigadores empezaron explorando grandes catálogos genéticos unicelulares de ganglios sensoriales —conjuntos de neuronas que transmiten tacto y dolor desde el cuerpo hasta la médula espinal—. Buscaron genes activados específicamente en nociceptores finos y no mielinizados, que transportan el dolor lento y persistente. Entre miles de candidatos, RNase4 destacó como un marcador altamente selectivo en ratones y mostró un patrón similar en tejido humano. La microscopía confirmó que RNase4 se encuentra principalmente en neuronas de pequeño diámetro y sin mielina que pertenecen a la línea de los nociceptores, pero no en neuronas fuertemente mielinizadas que manejan el tacto rápido y la vibración. Esta conservación entre especies sugiere que RNase4 marca un subconjunto especializado de células sensibles al dolor con un papel biológico compartido.
Modelando el comportamiento nervioso desde el interior
Para investigar qué hace RNase4, el equipo diseñó ratones en los que el gen podía eliminarse ya fuera durante el desarrollo o solo en nociceptores adultos. Cuando RNase4 se eliminó durante el desarrollo, el cableado básico de los circuitos del dolor y la sensibilidad normal al calor y al tacto permanecieron en gran medida intactos. Sin embargo, el secuenciamiento de ARN de núcleos individuales reveló que muchos genes cambiaron su actividad dentro de los nociceptores, incluidos factores de transcripción, proteínas estructurales y componentes de canales de potasio que ayudan a fijar el umbral de disparo eléctrico de las neuronas. En ratones adultos, apagar RNase4 solo en nociceptores provocó un aumento temporal de la sensibilidad al dolor mecánico: los animales reaccionaron con mayor intensidad al tacto ligero con filamentos aplicados en la pata, mientras que la sensibilidad al calor se mantuvo estable. En el transcurso de aproximadamente un mes, esta mayor sensibilidad mecánica se atenuó, lo que sugiere que otras vías compensan con el tiempo para restaurar el equilibrio.
Enviando señales hacia las células vecinas
RNase4 puede secretarse fuera de la célula, lo que abre la posibilidad de que los nociceptores influyan en fibras nerviosas y células de soporte cercanas. En cultivo celular, añadir RNase4 a una línea similar a neuronas sensoriales redujo la actividad de la vía PI3K–AKT–mTOR, un eje central de señalización de crecimiento y supervivencia. En ratones vivos, los autores emplearon luego un modelo de aplastamiento del nervio ciático, que imita una lesión nerviosa traumática seguida de degeneración y regeneración. Tras la lesión, los niveles de RNase4 aumentaron de forma natural en muchos subtipos de nociceptores, especialmente durante las fases tempranas de dolor y recuperación. Cuando RNase4 estaba ausente en los nociceptores, las pruebas conductuales mostraron que los ratones recuperaron la sensación mecánica más rápido que los controles, aunque la recuperación térmica pudo retrasarse dependiendo de la estrategia de eliminación. Esto sugiere que RNase4 normalmente limita ciertos aspectos del crecimiento y la sensibilidad, y que su eliminación inclina el sistema hacia una recuperación táctil más rápida.
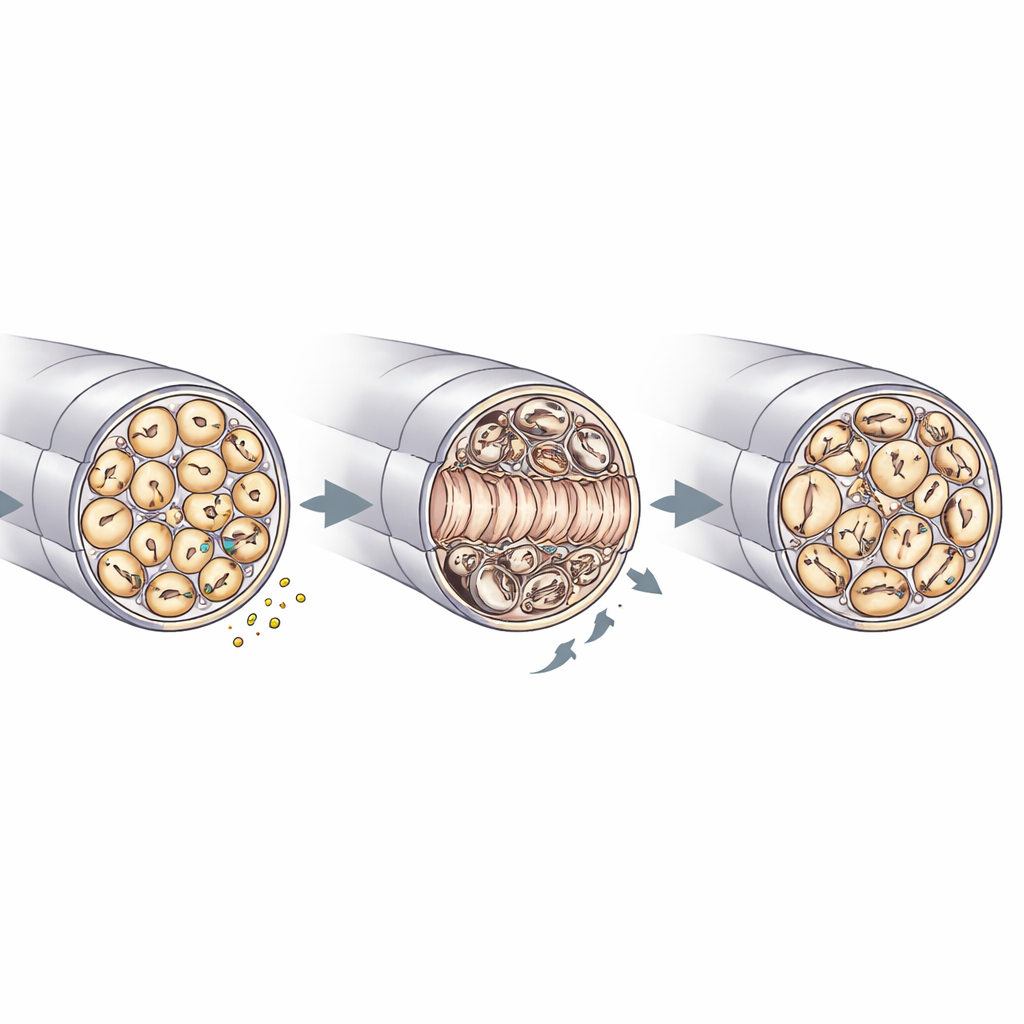
Reparación, calidad de la mielina y mantenimiento nervioso
La microscopía electrónica del nervio ciático ofreció una mirada más cercana sobre cómo RNase4 moldea la arquitectura nerviosa. Antes de la lesión, los nervios de los animales sin el gen y de los controles eran similares, con diámetros axonales, densidades y grosor de la mielina comparables. Tras la lesión por aplastamiento, sin embargo, los nervios sin RNase4 contenían más axones regenerados en el segmento dañado y mostraron un relleno más rápido de los haces no mielinizados tipo "Remak" que albergan muchas fibras finas. Al mismo tiempo, estos nervios con deleción presentaron más irregularidades en la mielina —como pliegues, invaginaciones y engrosamientos focales— y señales de estrés en las células de Schwann, las células gliales que envuelven los axones. También hubo menos restos de mielina dentro de las células inmunitarias, coherente con una depuración más eficiente y una reconstrucción estructural más rápida. Junto con los estudios de señalización, estos hallazgos respaldan un modelo en el que la RNase4 derivada de nociceptores modula la actividad de PI3K–AKT y, mediante efectos no locales, coordina cómo vuelven a crecer los axones, cómo se remodela la mielina y cómo participan las células inmunitarias en la limpieza.
Qué significa esto para tratamientos futuros
En términos sencillos, el estudio pinta a los nociceptores no solo como alarmas sino como gestores locales de la salud nerviosa. RNase4 actúa como un freno y guía molecular: dentro de los nociceptores, ayuda a mantener sus propiedades de disparo normales y su identidad; fuera de ellos, limita el crecimiento excesivo y condiciona cómo responden la mielina y las células de soporte tras una lesión. Eliminar RNase4 puede acelerar la recuperación del tacto tras daño nervioso, pero a costa de más defectos de mielina y una sensibilidad al dolor alterada. Cualquier terapia dirigida a bloquear o potenciar RNase4 tendrá que equilibrar estos compromisos. Aun así, el trabajo destaca a RNase4 y su red de señalización como palancas prometedoras para modular simultáneamente el dolor y favorecer una reparación nerviosa más ordenada.
Cita: Feng, X., Zhang, K., Techameena, P. et al. Ribonuclease 4 Functions in Nociceptor-Mediated Nerve Homeostasis. Nat Commun 17, 2862 (2026). https://doi.org/10.1038/s41467-026-70365-8
Palabras clave: nociceptores, regeneración nerviosa, mielina, dolor neuropático, RNase4