Clear Sky Science · it
Funzioni della ribonucleasi 4 nell’omeostasi nervosa mediata dai nocicettori
Perché è importante per le persone che vivono con il dolore
I nervi del dolore vengono spesso descritti come semplici messaggeri che segnalano quando qualcosa fa male. Questo studio rivela che alcuni di quei neuroni sensoriali del dolore, detti nocicettori, gestiscono anche in modo discreto la salute delle fibre nervose vicine. Il lavoro si concentra su una molecola poco nota, la ribonucleasi 4 (RNase4), e mostra che contribuisce a mantenere sotto controllo i segnali del dolore guidando al contempo come i nervi danneggiati si disfano e si ricostruiscono. Capire questo doppio ruolo potrebbe aprire nuove strade per trattare il dolore cronico e migliorare la riparazione nervosa dopo lesioni.
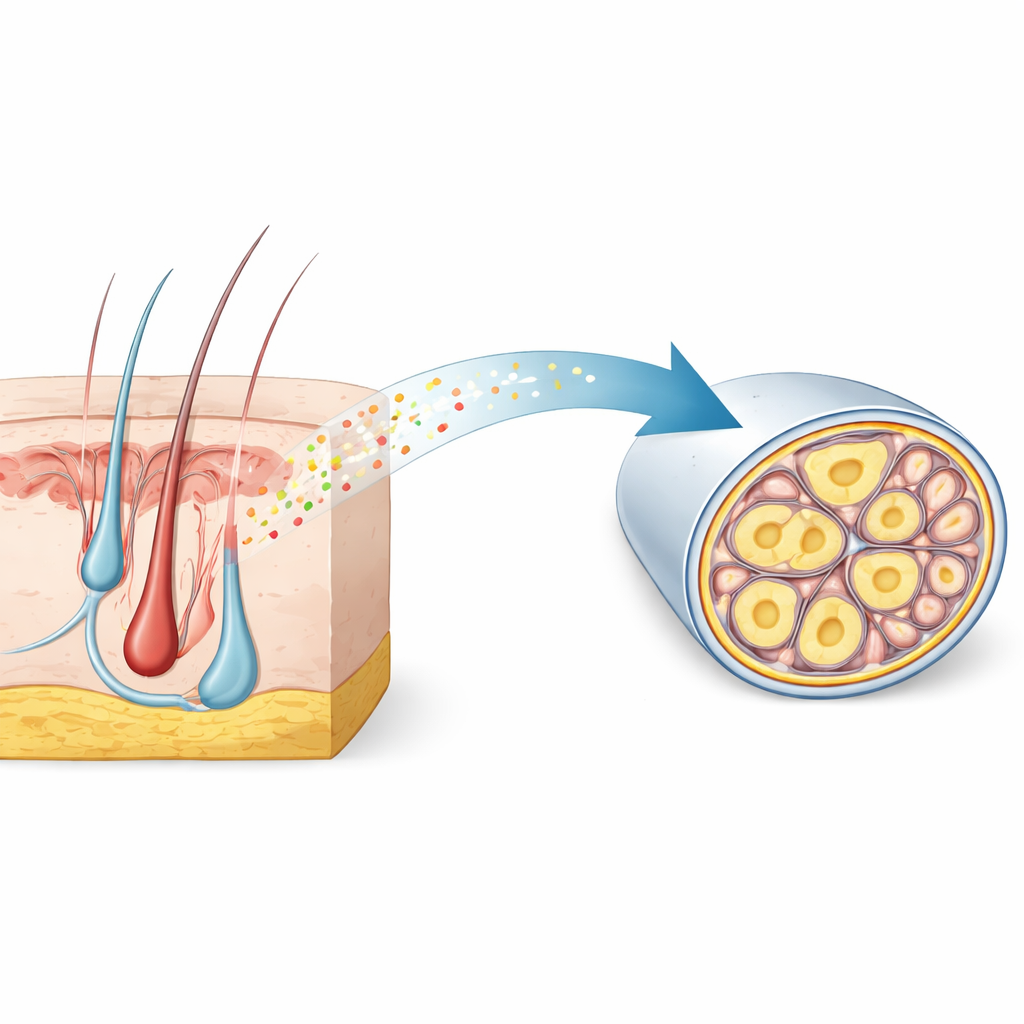
Una firma nascosta all’interno dei nervi sensoriali del dolore
I ricercatori hanno iniziato analizzando grandi atlanti genetici single-cell dei gangli sensoriali, insiemi di neuroni che trasmettono tattile e dolore dal corpo al midollo spinale. Hanno cercato geni attivati specificamente nei nocicettori sottili e non mielinizzati, che trasportano il dolore lento e doloroso. Tra migliaia di candidati, RNase4 è emersa come un marcatore altamente selettivo nei topi e ha mostrato uno schema corrispondente nel tessuto umano. La microscopia ha confermato che RNase4 si trova principalmente in neuroni a piccolo diametro e non mielinizzati appartenenti alla linea dei nocicettori, ma non nei neuroni fortemente mielinizzati che gestiscono il tatto rapido e le vibrazioni. Questa conservazione tra specie suggerisce che RNase4 contrassegna un sottogruppo specializzato di cellule sensoriali del dolore con un ruolo biologico condiviso.
Plasmare il comportamento nervoso dall’interno
Per indagare cosa fa RNase4, il gruppo ha creato topi in cui il gene poteva essere eliminato o durante lo sviluppo o soltanto nei nocicettori degli adulti. Quando RNase4 è stato rimosso durante lo sviluppo, l’architettura di base dei circuiti del dolore e la sensibilità normale a calore e tatto sono rimaste in gran parte intatte. Tuttavia, il sequenziamento RNA a singolo nucleo ha rivelato che molti geni cambiavano attività all’interno dei nocicettori, compresi fattori di trascrizione, proteine strutturali e componenti di canali del potassio che contribuiscono a impostare la soglia di eccitazione elettrica dei neuroni. Nei topi adulti, lo spegnimento di RNase4 solo nei nocicettori ha scatenato un aumento temporaneo della sensibilità al dolore meccanico: gli animali reagivano più intensamente al tocco leggero con filamentini applicati alla zampa, mentre la sensibilità al calore rimaneva stabile. In circa un mese, questa aumentata sensibilità meccanica è diminuita, suggerendo che altri percorsi compensano nel tempo per ristabilire l’equilibrio.
Inviare segnali verso le cellule vicine
RNase4 può essere secreta all’esterno della cellula, aprendo la possibilità che i nocicettori influenzino le fibre nervose vicine e le cellule di supporto. in coltura cellulare, l’aggiunta di RNase4 a una linea simile a neuroni sensoriali attenuava l’attività della via PI3K–AKT–mTOR, un nodo centrale di segnalazione per crescita e sopravvivenza. In topi vivi, gli autori hanno quindi utilizzato un modello di schiacciamento del nervo sciatico, che imita una lesione nervosa traumatica seguita da degenerazione e ricrescita. Dopo la lesione, i livelli di RNase4 aumentavano naturalmente in molti sottotipi di nocicettori, specialmente nelle fasi iniziali di dolore e recupero. Quando RNase4 mancava nei nocicettori, i test comportamentali hanno mostrato che i topi riacquistavano la sensibilità meccanica più rapidamente rispetto ai controlli, sebbene il recupero termico potesse essere più lento a seconda della strategia di eliminazione. Questo suggerisce che RNase4 normalmente limita alcuni aspetti della ricrescita e della sensibilità, e che la sua rimozione inclina il sistema verso un recupero tattile più veloce.
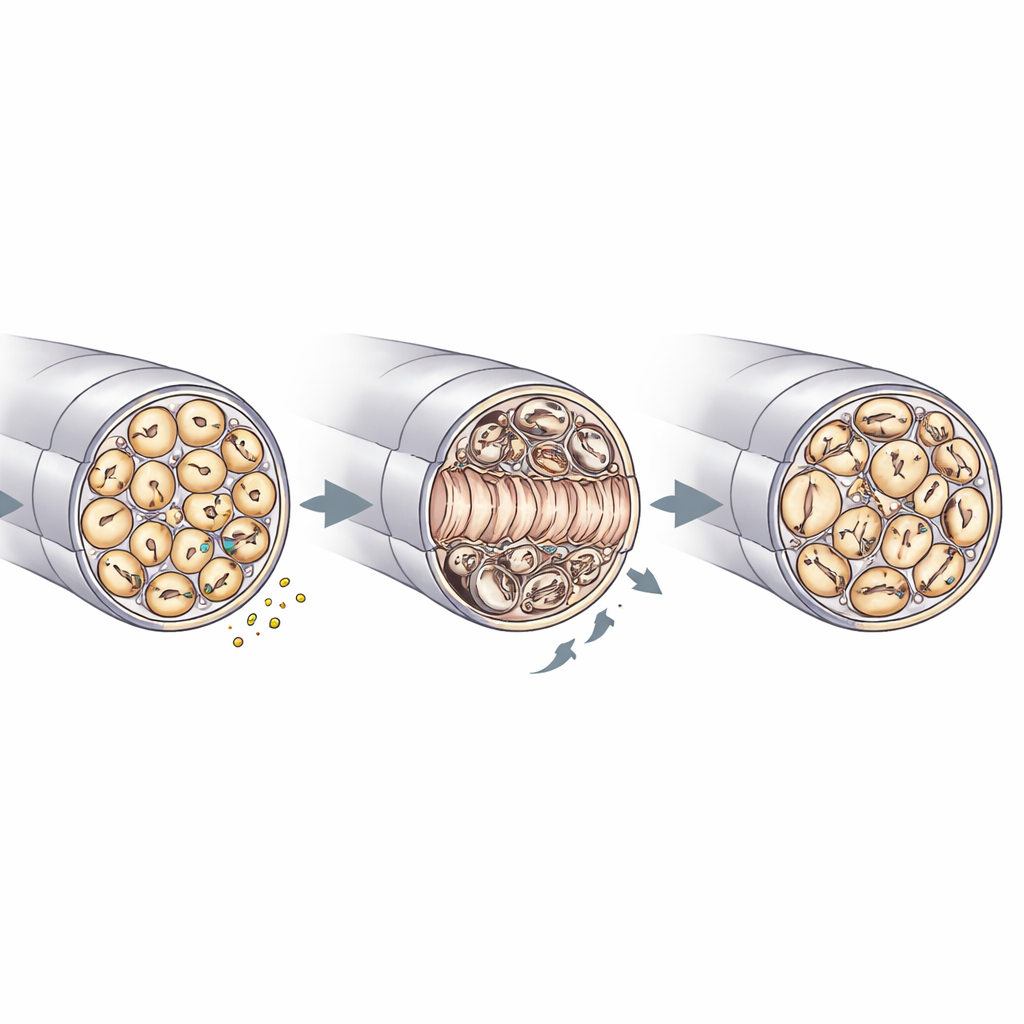
Riparazione, qualità della mielina e manutenzione nervosa
L’ulteriore esame in microscopia elettronica dei nervi sciatici ha offerto uno sguardo più ravvicinato su come RNase4 modella l’architettura nervosa. Prima della lesione, nervi knockout e controlli apparivano simili, con diametri degli assoni, densità e spessore della mielina comparabili. Dopo lo schiacciamento, però, i nervi privi di RNase4 contenevano più assoni rigenerati nel segmento danneggiato e mostravano un riempimento più rapido dei fasci non mielinizzati “Remak” che ospitano molte fibre sottili. Allo stesso tempo, questi nervi knockout presentavano maggiori irregolarità della mielina — come pieghe, infossamenti e ispessimenti focali — e segni di stress nelle cellule di Schwann, le cellule gliali che avvolgono gli assoni. C’era anche meno detrito mielinico all’interno delle cellule immunitarie, coerente con una rimozione più efficiente e una ricostruzione strutturale più rapida. Insieme agli studi di segnalazione, questi risultati supportano un modello in cui la RNase4 derivata dai nocicettori modula l’attività di PI3K–AKT e, attraverso effetti non locali, coordina come gli assoni ricrescono, come la mielina viene rimodellata e come le cellule immunitarie partecipano alla pulizia.
Cosa significa per i trattamenti futuri
In termini semplici, lo studio dipinge i nocicettori non solo come campanelli d’allarme ma come gestori locali della salute nervosa. RNase4 agisce come un freno e una guida molecolare: all’interno dei nocicettori aiuta a mantenere le loro proprietà di eccitazione e la loro identità; all’esterno limita una ricrescita eccessiva e modella come la mielina e le cellule di supporto rispondono dopo una lesione. Rimuovere RNase4 può accelerare il ritorno del tatto dopo un danno nervoso ma a costo di più difetti nella mielina e di una sensibilità al dolore alterata. Qualsiasi terapia mirata a bloccare o potenziare RNase4 dovrà bilanciare questi compromessi. Resta comunque il fatto che RNase4 e la sua rete di segnalazione rappresentano leve promettenti per modulare contemporaneamente il dolore e promuovere una riparazione nervosa più ordinata.
Citazione: Feng, X., Zhang, K., Techameena, P. et al. Ribonuclease 4 Functions in Nociceptor-Mediated Nerve Homeostasis. Nat Commun 17, 2862 (2026). https://doi.org/10.1038/s41467-026-70365-8
Parole chiave: nocicettori, rigenerazione nervosa, mielina, dolore neuropatico, RNase4