Clear Sky Science · tr
Ribonükleaz 4’ün Nositsepton Kaynaklı Sinir Homeostazındaki İşlevleri
Ağrı ile yaşayan insanlar için bunun önemi
Ağrı ileten sinirler sıklıkla bir şey acıdığında bağıran basit elçiler olarak görülür. Bu çalışma, nosiseptör adı verilen bazı ağrı algılayıcı nöronların, yakındaki sinir liflerinin sağlığını sessizce yönettiklerini ortaya koyuyor. Çalışma, az bilinen bir molekül olan ribonükleaz 4 (RNase4) üzerine odaklanıyor ve bunun hem ağrı sinyallerini kontrol altında tutmaya hem de hasarlı sinirlerin nasıl parçalanıp yeniden inşa olduğunu yönlendirmeye yardımcı olduğunu gösteriyor. Bu ikili rolün anlaşılması kronik ağrı tedavileri ve yaralanma sonrası sinir onarımını iyileştirmeye yönelik yeni yollar açabilir.
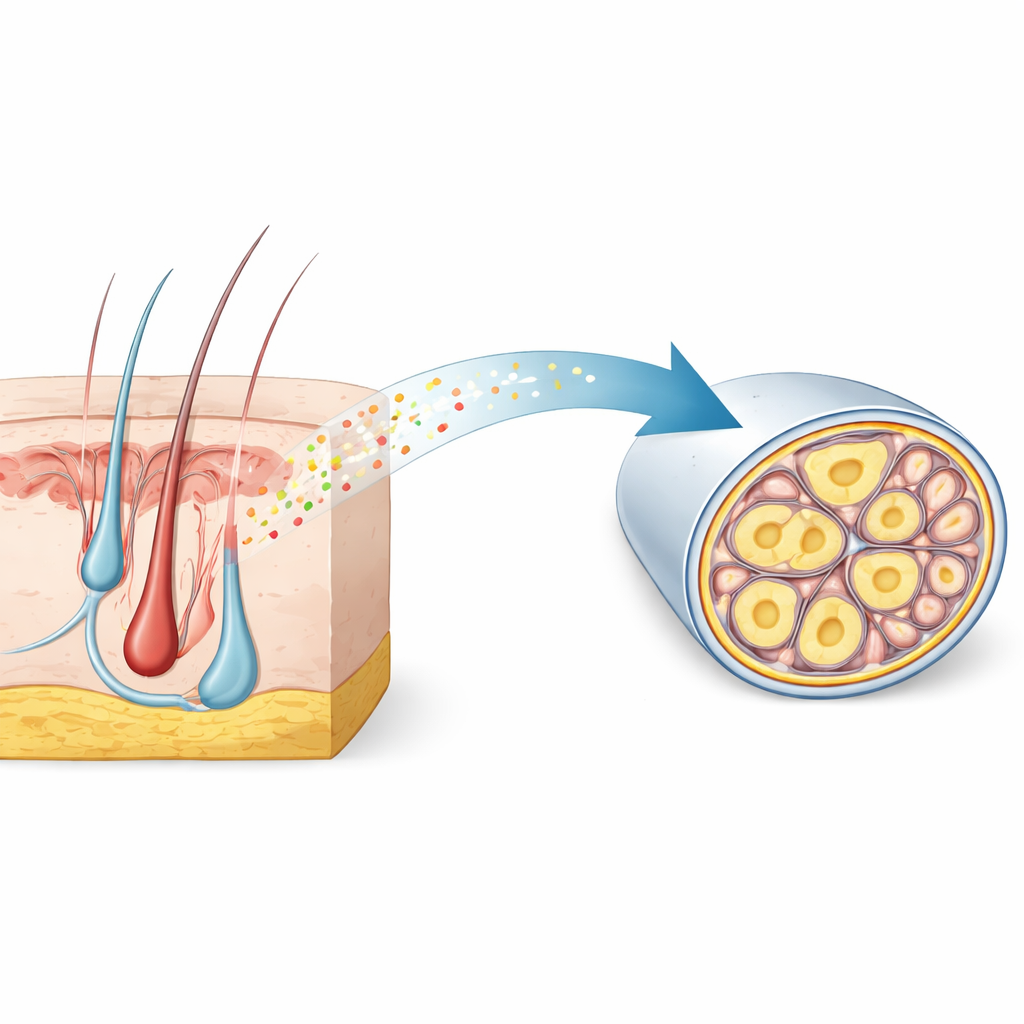
Ağrı algılayan sinirlerin içindeki gizli bir imza
Araştırmacılar, dokudan omuriliğe dokunma ve ağrıyı ileten duyu ganglionlarının—tek hücre düzeyinde geniş genetik atlaslarını—kazıyarak başladılar. Yavaş, sızlayan ağrıyı taşıyan ince, miyelinsiz nosiseptörlerde özel olarak açılan genleri aradılar. Binlerce aday arasında RNase4, farelerde son derece seçici bir belirteç olarak öne çıktı ve insan dokusunda da benzer bir desen gösterdi. Mikroskopi RNase4’ün ağırlıklı olarak nosiseptör soyu içinde yer alan küçük çaplı, miyelinsiz nöronlarda bulunduğunu; hızlı dokunma ve titreşimi işleyen yoğun miyelinli nöronlarda ise bulunmadığını doğruladı. Türler arasındaki bu korunum, RNase4’ün ortak bir biyolojik role sahip özel bir ağrı algılayıcı hücre alt kümesini işaret ettiğini düşündürüyor.
Sinir davranışını içeriden şekillendirmek
RNase4’ün işlevini araştırmak için ekip, geni ya gelişim sırasında erken dönemde ya da sadece erişkin nosiseptörlerde silinebilecek şekilde tasarlanmış fareler üretti. RNase4 gelişim sırasında kaldırıldığında, ağrı devrelerinin temel bağlantıları ile normal ısı ve dokunma duyarlılığı büyük ölçüde korunmuş kaldı. Ancak tek çekirdek RNA dizilemesi, nosiseptörler içinde birçok genin aktivitesinin değiştiğini ortaya koydu; bunlar arasında transkripsiyon faktörleri, yapısal proteinler ve nöronların elektriksel ateşleme eşiklerini belirlemeye yardımcı olan potasyum kanalı bileşenleri vardı. Erişkin farelerde RNase4 yalnızca nosiseptörlerde kapatıldığında ise mekanik ağrı duyarlılığında geçici bir artış tetiklendi: hayvanlar pati üzerine uygulanan ince filamentlere daha güçlü tepki verdi, oysa ısı duyarlılığı sabit kaldı. Yaklaşık bir ay içinde bu artmış mekanik duyarlılık azaldı; bu da zamanla dengeyi yeniden sağlamak için diğer yolların telafi ettiği izlenimini veriyor.
Komşu hücrelere dışa doğru sinyal göndermek
RNase4 hücre dışına salgılanabilir; bu da nosiseptörlerin yakındaki sinir liflerini ve destek hücrelerini etkileyebileceği olasılığını doğuruyor. Hücre kültüründe, sensör nöron benzeri bir hücre hattına RNase4 eklenmesi PI3K–AKT–mTOR yolunda, bir merkezi büyüme ve hayatta kalma sinyal ağı olan aktiviteyi azalttı. Canlı farelerde araştırmacılar ardından travmatik sinir yaralanmasını, dejenerasyonu ve yeniden büyümeyi taklit eden siyatik sinir ezilme modelini kullandı. Yaralanma sonrası RNase4 seviyeleri doğal olarak birçok nosiseptör alt tipinde, özellikle erken ağrı ve iyileşme aşamalarında yükseldi. RNase4 nosiseptörlerden yoksun olduğunda, davranış testleri farelerin mekanik duyuyu kontrol grubuna göre aslında daha hızlı geri kazandığını gösterdi; termal (ısıya bağlı) toparlanma ise silme stratejisine bağlı olarak gecikebiliyordu. Bu durum RNase4’ün normalde yeniden büyüme ve duyarlılığın bazı yönlerini sınırladığını, yokluğunun ise sistemi daha hızlı dokunsal toparlanmaya eğilimli hale getirdiğini düşündürdü.
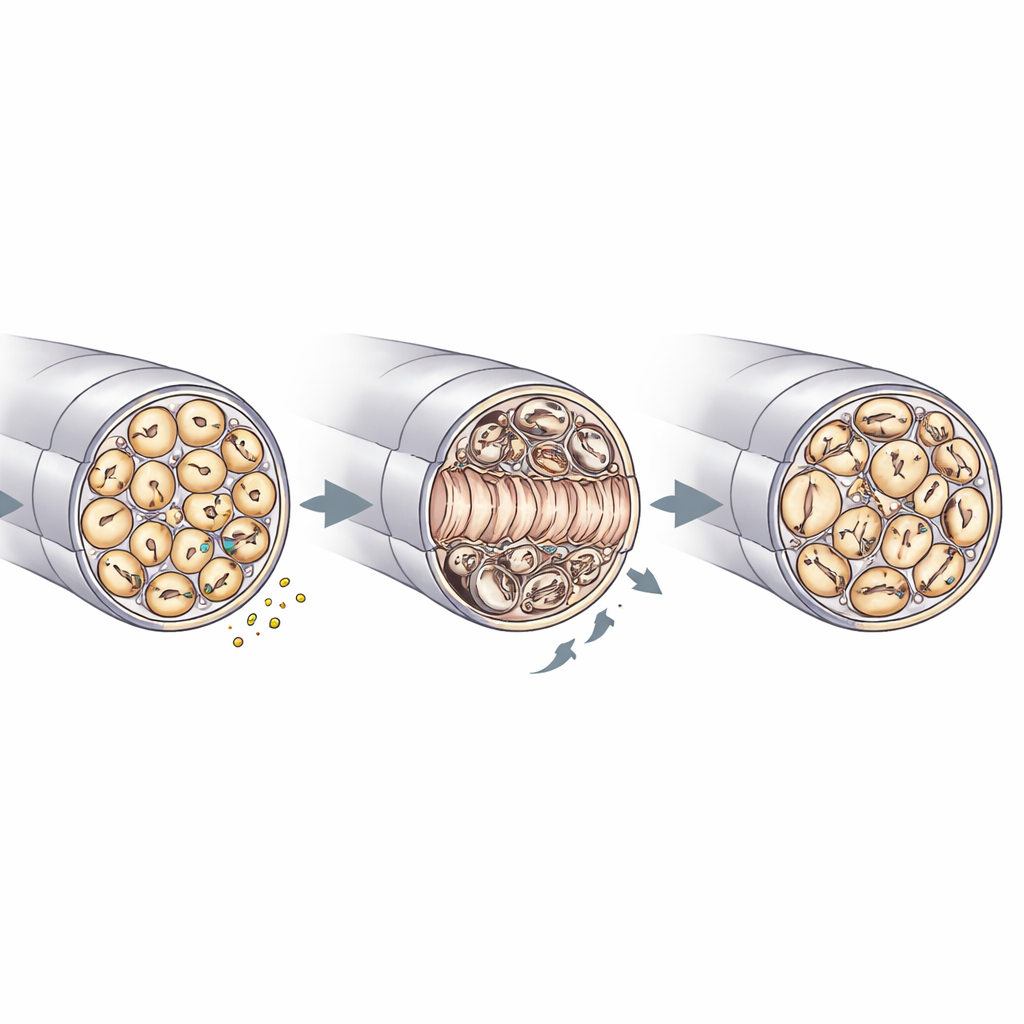
Onarım, miyelin kalitesi ve sinir ev işleri
Siyatik sinirlerin elektron mikroskobu, RNase4’ün sinir mimarisini nasıl şekillendirdiğine dair daha yakından bakış sundu. Yaralanma öncesinde, knockout ve kontrol sinirleri benzer görünüyordu; akson çapları, yoğunlukları ve miyelin kalınlıkları karşılaştırılabilirdi. Ancak ezilme yaralanmasından sonra RNase4 eksikliği olan sinirlerde hasarlı segmentte daha fazla yeniden oluşmuş akson bulundu ve birçok ince lifi barındıran miyelinsiz "Remak" demetlerinin yeniden dolumu daha hızlı gerçekleşti. Aynı zamanda bu knockout sinirler miyelin düzensizlikleri—kırışıklıklar, içe katlanmalar ve odaklanmış kalınlaşma gibi—ve aksonları saran glial hücreler olan Schwann hücrelerinde stres belirtileri sergiledi. Ayrıca immün hücrelerin içinde daha az miyelin kalıntısı vardı; bu da daha etkin bir temizleme ve daha hızlı yapısal yeniden inşa ile uyumluydu. Sinyal çalışmalarıyla birlikte bu bulgular, nosiseptör kaynaklı RNase4’ün PI3K–AKT aktivitesini ayarlayan ve lokal olmayan etkiler aracılığıyla aksonların nasıl yeniden büyüdüğünü, miyelinin nasıl yeniden şekillendiğini ve immün hücrelerin temizlik sürecine nasıl katıldığını koordine eden bir modeli destekliyor.
Gelecekteki tedaviler için ne anlama geliyor
Basitçe söylemek gerekirse, çalışma nosiseptörleri yalnızca alarm zilleri değil, aynı zamanda sinir sağlığının yerel yöneticileri olarak betimliyor. RNase4 moleküler bir fren ve rehber görevi görüyor: nosiseptörlerin içinde normal ateşleme özelliklerini ve kimliklerini korumaya yardımcı oluyor; dışarıda ise aşırı hevesli yeniden büyümeyi sınırlıyor ve yaralanma sonrası miyelin ile destek hücrelerin yanıtlarını şekillendiriyor. RNase4’ün kaldırılması sinir hasarından sonra dokunma duyusunun geri dönmesini hızlandırabilir, ancak daha fazla miyelin kusuru ve değişmiş ağrı duyarlılığı gibi bedelleri olabilir. RNase4’ü engellemeye ya da güçlendirmeye yönelik herhangi bir terapi bu takasları dengelemeyi gerektirecektir. Yine de çalışma, RNase4 ve onun sinyal ağına eş zamanlı olarak ağrıyı modüle etme ve daha düzenli sinir onarımını teşvik etme açısından umut verici kollar olarak dikkat çekiyor.
Atıf: Feng, X., Zhang, K., Techameena, P. et al. Ribonuclease 4 Functions in Nociceptor-Mediated Nerve Homeostasis. Nat Commun 17, 2862 (2026). https://doi.org/10.1038/s41467-026-70365-8
Anahtar kelimeler: nosiseptörler, sinir rejenerasyonu, miyelin, nöropatik ağrı, RNase4