Clear Sky Science · zh
通过动态键驱动在金属有机框架中包封酶,突破孔径限制
为何囚藏脆弱帮手很重要
酶是自然界的小型工蜂,加速着从活细胞到工业制造中发生的化学反应。但在其自然环境之外,这些脆弱的蛋白质很容易失去结构和功能,从而难以在大规模应用中重复使用。本文报道了一种将酶安全封入多孔晶体材料的方法,使其活性保持更久并可重复回收。关键在于,研究小组展示了如何将尺寸实际上大于材料内建开口的酶塞入,从而绕过长期制约绿色化学和医药许多应用的尺寸限制。
构建保护性的晶体“房屋”
研究者使用金属-有机框架(MOF)——由金属簇通过有机“支柱”连接成有序骨架并含有大量空隙的固体。MOF是酶的理想“住所”,因为它们提供了大的内部比表面积和保护性笼室,可以屏蔽蛋白质免受热、溶剂和苛刻条件的侵害。问题在于,许多有用的酶体积太大,无法通过大多数MOF狭窄的窗口。以往的解决方案要么将酶固定在外表面,从而限制了装载量,要么在非常温和的条件下尝试在酶周围生长MOF,但这只适用于少数MOF化学体系。
加入可开合且可自愈的小门
为了解决这一尺寸陷阱,作者设计了一系列其内部连接可暂时松脱又能重新结合、类似自愈缝合的MOF。他们将非常稳定的金属-羧酸盐簇(作为刚性主干)与更柔性的金属-吡啶连接(表现为可逆的“门”)相结合。通过更换不同的金属并改变有机连接体的长度,他们能够精细调节这些门在水中开启的难易程度,同时不致于使整体结构坍塌。金属浸出测量、X射线衍射和计算机模拟等多种手段都指向相同的结论:在水中,仅特定金属位点的较软连接发生松动,而更坚固的主干保持完整,从而维护了总体晶体框架。
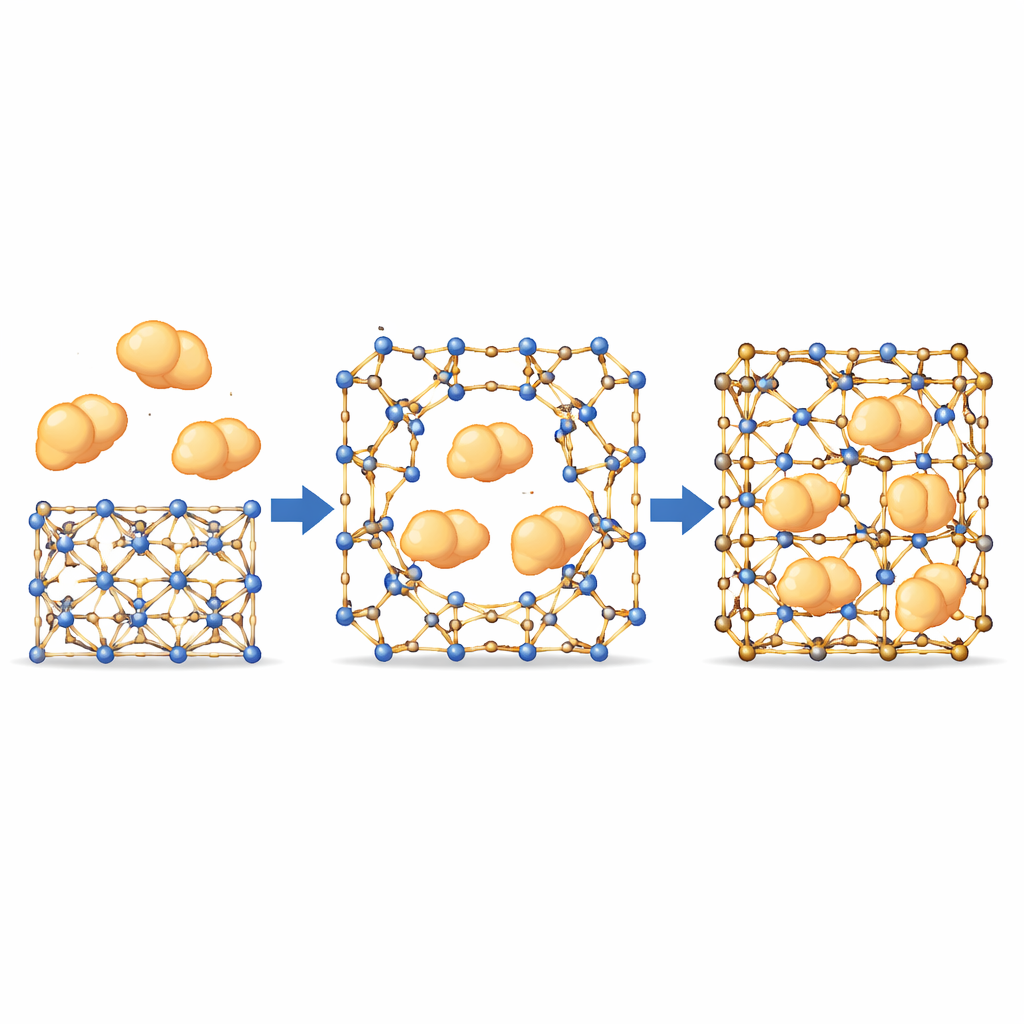
让大酶通过小孔
有了这种门控行为,团队测试了尺寸大于MOF名义孔径的酶是否仍能被引入。他们使用荧光标记的蛋白质与共焦显微镜,观察到酶从晶体表面均匀向内部移动,沿着不符合固定内部通道的路径。这表明当动态键短暂分离时会形成临时开口,使酶渗入,然后框架在其周围“愈合”。重要的是,那些更坚固且这些键几乎不移动的材料变体几乎不吸附酶,证实了这些位点的运动是必需的。在一组具有不同尺寸和性质的酶中,经过精细平衡的MOF实现了高装载量,同时仍保持晶体序。
更强、更持久的催化剂
一旦进入其中,酶表现出稳健且可重复使用的催化性能。作者考察了若干代表性蛋白,包括那些对热、碱性条件和有机溶剂极为敏感的酶。与溶液中游离的相同酶相比,被包封的酶在受压条件下保持了更多活性,并且经过多次反应循环后性能损失很小。动态MOF还实现了两种协同酶的共同包封,这两种酶顺序工作以合成一种有价值的糖基构建块。将两者安置于同一框架内缩短了它们之间的通路,提高了反应效率,并使体系能在重复运行中维持稳定产出。
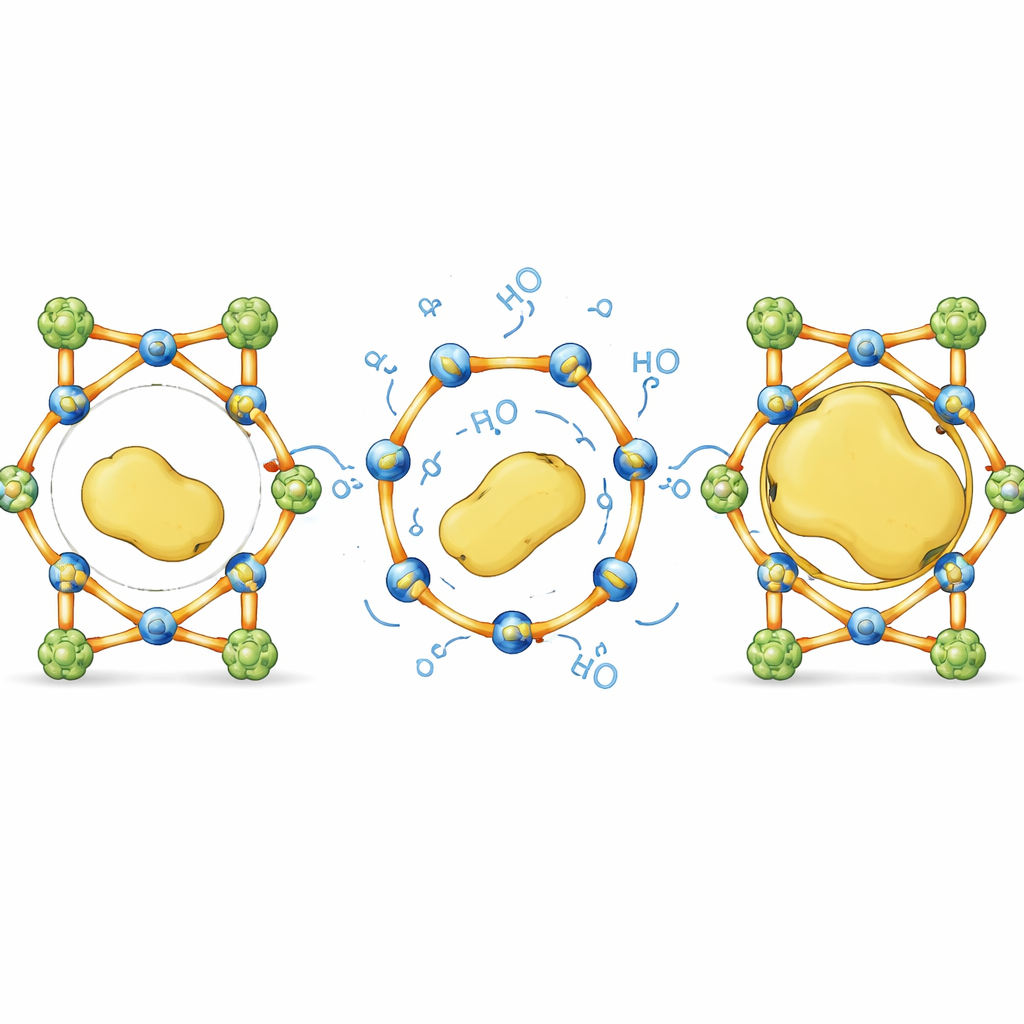
从尺寸限制走向不受尺寸束缚的设计
通俗地说,这项工作将一个带有固定孔洞的刚性海绵变成了一个智能笼,其栏杆能适度弯动以接纳大型访客,然后迅速恢复原状。通过仔细平衡不可破坏的支撑与选择性可逆的连接,作者表明可以在通常会排斥它们的晶体材料中容纳体积庞大且脆弱的酶,而不牺牲结构或功能。这种由动态键驱动的方法为设计不受尺寸限制的“酶旅馆”提供了通用方案,有望改进工业生物催化剂、简化多步合成并创造更耐用的生物基技术。
引用: Li, Y., Qiao, M., Gao, L. et al. Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints. Nat Commun 17, 3642 (2026). https://doi.org/10.1038/s41467-026-70249-x
关键词: 酶固定化, 金属有机框架, 生物催化, 动态配位键, 多酶级联