Clear Sky Science · ar
التغليف المدفوع بروابط ديناميكية للإنزيمات داخل أطر عضوية-معدنية يتجاوز قيود حجم المسام
لماذا يهم احتجاز المساعدين الحساسين
الإنزيمات هي عمال الطبيعة الصغار الذين يسرعون التفاعلات الكيميائية التي تغذي كل شيء من الخلايا الحية إلى التصنيع الصناعي. لكن خارج بيئتها الطبيعية تنهار هذه البروتينات الرقيقة بسرعة، مما يجعل من الصعب إعادة استخدامها على نطاق واسع. يعرض هذا المقال طريقة لوضع الإنزيمات بأمان داخل مادة بلورية مسامية، بحيث تبقى نشطة لفترة أطول ويمكن تدويرها مرارًا. والأهم أن الفريق يبيّن كيفية إدخال إنزيمات أكبر فعليًا من الفتحات المدمجة في المادة، متجاوزًا حدًا حجميًا قد أعاق تطبيقات واعدة في الكيمياء الخضراء والطب.
بناء بيت بلوري واقٍ
يعمل الباحثون مع أطر عضوية-معدنية، أو MOFs — وهي مواد صلبة مكوّنة من مجموعات معدنية مرتبطة بواسطة «عوارض» عضوية لتشكيل هيكل منتظم مليء بالفراغات. تجذب MOFs الإنزيمات لأنها توفر مساحات سطح داخلية كبيرة وأقفاصًا وقائية يمكنها حماية البروتينات من الحرارة والمذيبات والظروف القاسية. لكن المشكلة أن العديد من الإنزيمات المفيدة كبيرة جدًا بحيث لا يمكن ضغطها عبر نوافذ معظم MOFs الضيقة. الحلول السابقة كانت إما تثبيت الإنزيمات على السطح الخارجي، مما حدّ من كمية التحميل، أو محاولة نمو الـMOF حول الإنزيمات في ظروف لطيفة جدًا، وهو ما ينجح فقط مع مجموعة محدودة من كيميائيات الـMOF.
إضافة بوابات صغيرة تفتح وتلتئم
لكسر هذا القيد الحجمي، صمّم المؤلفون عائلة من الـMOFs تكون اتصالاتها الداخلية قادرة على الانفصال وإعادة الالتصاق لفترة قصيرة مثل غرز تلتئم ذاتيًا. جمعوا مجموعات معدنية-كربوكسيلات ثابتة جدًا تعمل كعمود فقري صلب، مع روابط معدنية-بيريديل أكثر مرونة تتصرف كبوابات قابلة للعكس. عبر تبديل معادن مختلفة وتغيير طول الروابط العضوية، تمكنوا من ضبط مدى سهولة فتح هذه البوابات في الماء بدقة دون أن يتفكك الهيكل كليًا. أشارت قياسات تسرب المعادن، والتحليل بواسطة حيود الأشعة السينية، والمحاكاة الحاسوبية كلها إلى نفس الصورة: في الماء، ترتخي فقط الاتصالات الأضعف في مواقع معدنية محددة، بينما يبقى العمود الفقري الأشد متماسكًا، حافظًا على الإطار البلوري الكلي.
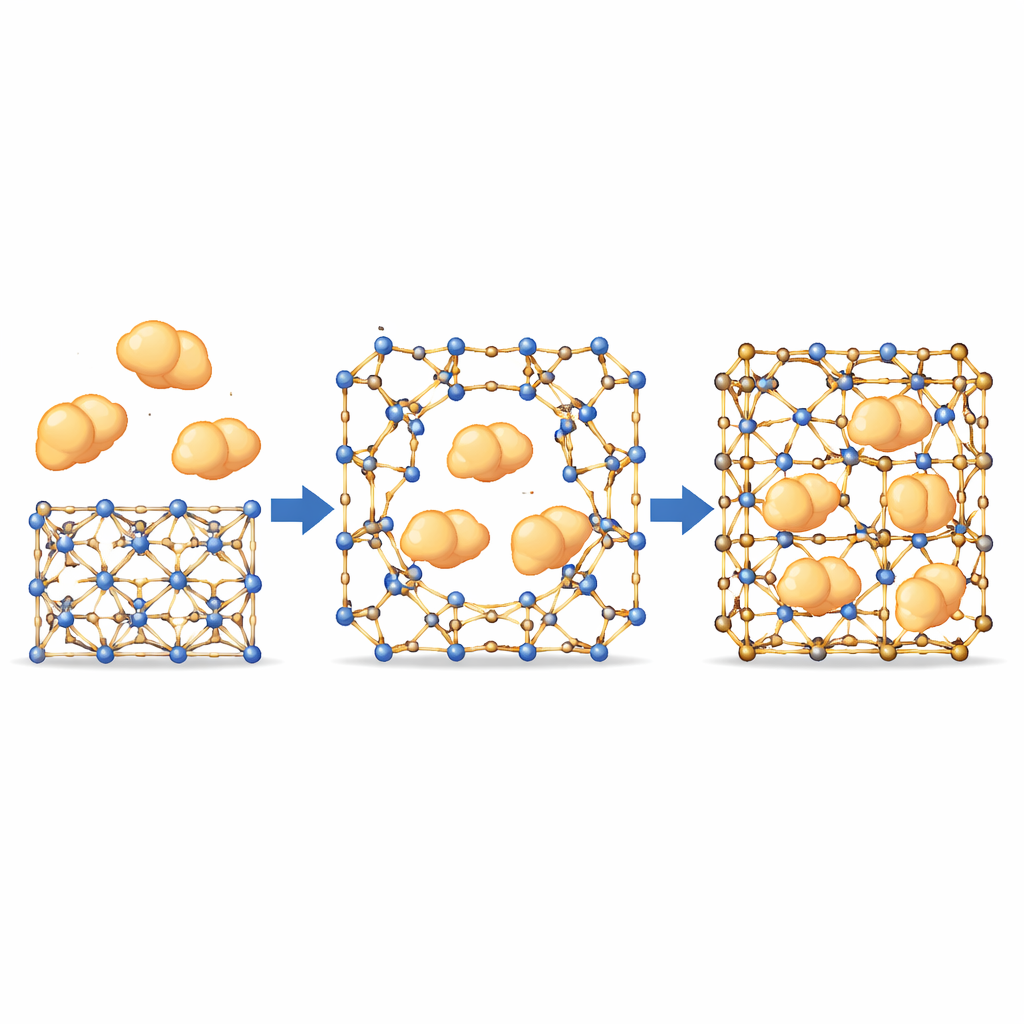
السماح للإنزيمات الكبيرة بالتسلل عبر مسام صغيرة
مع هذا السلوك الشبيه بالبوابة، اختبر الفريق ما إذا كانت الإنزيمات الكبيرة — الأكبر من مسام الـMOF الاسمية — يمكن أن تدخل الداخل. باستخدام بروتينات موسومة فلوريًا والمجهر المربّع الكونفوكالي، راقبوا حركة الإنزيمات تتجه بشكل موحد من سطح البلورة نحو الداخل، متبعة مسارات لا تتطابق مع القنوات الداخلية الثابتة. هذا يوحي بتكوّن فتحات مؤقتة حيث تنفصل الروابط الديناميكية لفترة قصيرة، مما يسمح للإنزيمات بالتسلل قبل أن «تلتئم» البنية حولها. ومن الجدير بالذكر أن المتغيرات الأصعب من المادة، حيث تتحرك هذه الروابط قليلًا، أظهرت اندماجًا طفيفًا للإنزيم تقريبًا، مؤكدة أن الحركة عند هذه المواقع ضرورية. عبر لوحة من الإنزيمات ذات أحجام وخصائص مختلفة، حققت أنسب الـMOFs تحميلًا عاليًا مع الحفاظ على ترتيبها البلوري.
محفزات أقوى وأكثر دوامًا
بمجرد الدخول، تصرفت الإنزيمات كمحفزات قوية وقابلة لإعادة الاستخدام. فحص المؤلفون عدة بروتينات نموذجية، بما في ذلك تلك الحساسة جدًا للحرارة والظروف القلوية والمذيبات العضوية. بالمقارنة مع نفس الإنزيمات حرة في المحلول، احتفظت النسخ المغلفة بنشاط أكبر بكثير عند تعريضها للظروف القاسية، ويمكن تدويرها عبر عدة دورات تفاعل مع فقدان أداء ضئيل. كما مكّن الـMOFs الديناميكي من احتواء إنزيمين متعاونين يعملان على التوالي لصنع بناء سكر ثمين. وضعهما معًا داخل الإطار قلّص المسافة بينهما، معززًا كفاءة التفاعل ومتيحًا للنظام العمل مرارًا مع إنتاج مستدام.
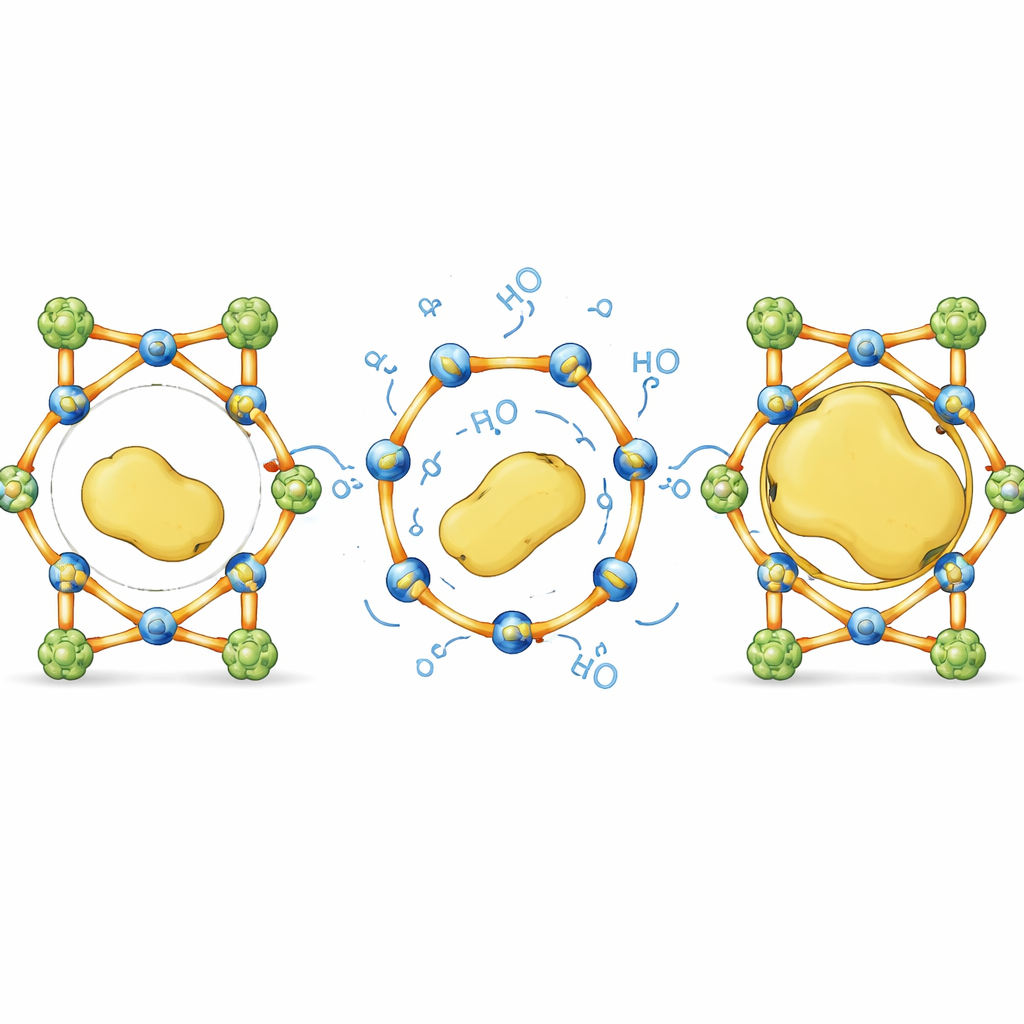
من حدود الحجم إلى تصميم غير متأثر بالحجم
بعبارة بسيطة، يحول هذا العمل إسفنجة صلبة ذات ثقوب ثابتة إلى قفص ذكي يمكن لقضبانه أن تنثني بدرجة كافية لدخول ضيوف كبار ثم تعود إلى مكانها. عبر موازنة الدعم الغير قابل للكسر مع روابط قابلة للعكس انتقائيًا، يبيّن المؤلفون أنه يمكن حزم إنزيمات ضخمة وهشة داخل مواد بلورية كانت ستستبعدها عادةً، دون التضحية بالهيكل أو الوظيفة. تقدم هذه المقاربة المدفوعة بالروابط الديناميكية وصفة عامة لتصميم «فنادق إنزيمات» مستقلة عن الحجم، مع إمكانية تحسين المحفزات الصناعية، وتبسيط التركيبات متعددة الخطوات، وابتكار تقنيات حيوية مبنية أكثر ديمومة.
الاستشهاد: Li, Y., Qiao, M., Gao, L. et al. Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints. Nat Commun 17, 3642 (2026). https://doi.org/10.1038/s41467-026-70249-x
الكلمات المفتاحية: تثبيت الإنزيمات, أطر عضوية-معدنية, التحفيز الحيوي, روابط تنسيقية ديناميكية, تتابعات إنزيمية متعددة