Clear Sky Science · fr
Encapsulation d’enzymes entraînée par des liaisons dynamiques dans des matériaux métal‑organiques au‑delà des contraintes de taille des pores
Pourquoi enfermer des auxiliaires fragiles importe
Les enzymes sont les petits moteurs de la nature, accélérant des réactions chimiques qui alimentent aussi bien les cellules vivantes que la production industrielle. Mais hors de leurs environnements naturels, ces protéines délicates se dégradent rapidement, rendant leur réutilisation à grande échelle difficile. Cet article décrit une méthode pour loger des enzymes en sécurité à l’intérieur d’un matériau cristallin poreux, afin qu’elles conservent leur activité plus longtemps et puissent être recyclées à plusieurs reprises. De façon cruciale, l’équipe montre comment insérer des enzymes qui sont en réalité plus grandes que les ouvertures intégrées du matériau, contournant une limite de taille de longue date qui freinait de nombreuses applications prometteuses en chimie verte et en médecine.
Construire une maison cristalline protectrice
Les chercheurs travaillent avec des matériaux métal‑organiques, ou MOFs — des solides constitués d’amas métalliques reliés par des « poutres » organiques formant une charpente ordonnée remplie d’espaces vides. Les MOFs sont des hébergements attractifs pour les enzymes car ils offrent de grandes surfaces internes et des cages protectrices capables d’isoler les protéines de la chaleur, des solvants et des conditions agressives. Le problème est que beaucoup d’enzymes utiles sont tout simplement trop volumineuses pour passer par les fenêtres étroites de la plupart des MOFs. Les solutions antérieures fixa ient soit les enzymes à la surface extérieure, ce qui limitait la quantité pouvant être chargée, soit tentaient de faire croître le MOF autour des enzymes sous des conditions très douces, ce qui ne fonctionne que pour un sous‑ensemble restreint de chimies de MOF.
Ajouter de petites portes qui s’ouvrent et se réparent
Pour échapper à cette contrainte de taille, les auteurs ont conçu une famille de MOFs dont les connexions internes peuvent brièvement se détacher puis se rattacher comme des points de suture auto‑réparateurs. Ils ont combiné des amas métal‑carboxylate très stables, qui servent de colonne vertébrale rigide, avec des liaisons métal‑pyridyle plus flexibles se comportant comme des « portes » réversibles. En substituant différents métaux et en changeant la longueur des linkers organiques, ils ont pu ajuster finement la facilité d’ouverture de ces portes en milieu aqueux sans provoquer l’effondrement de la structure complète. Les mesures de lixiviation des métaux, la diffraction des rayons X et les simulations informatiques convergent vers la même image : en présence d’eau, seules les connexions les plus souples à des sites métalliques spécifiques s’assouplissent, tandis que la colonne vertébrale plus robuste demeure intacte, préservant le réseau cristallin global.
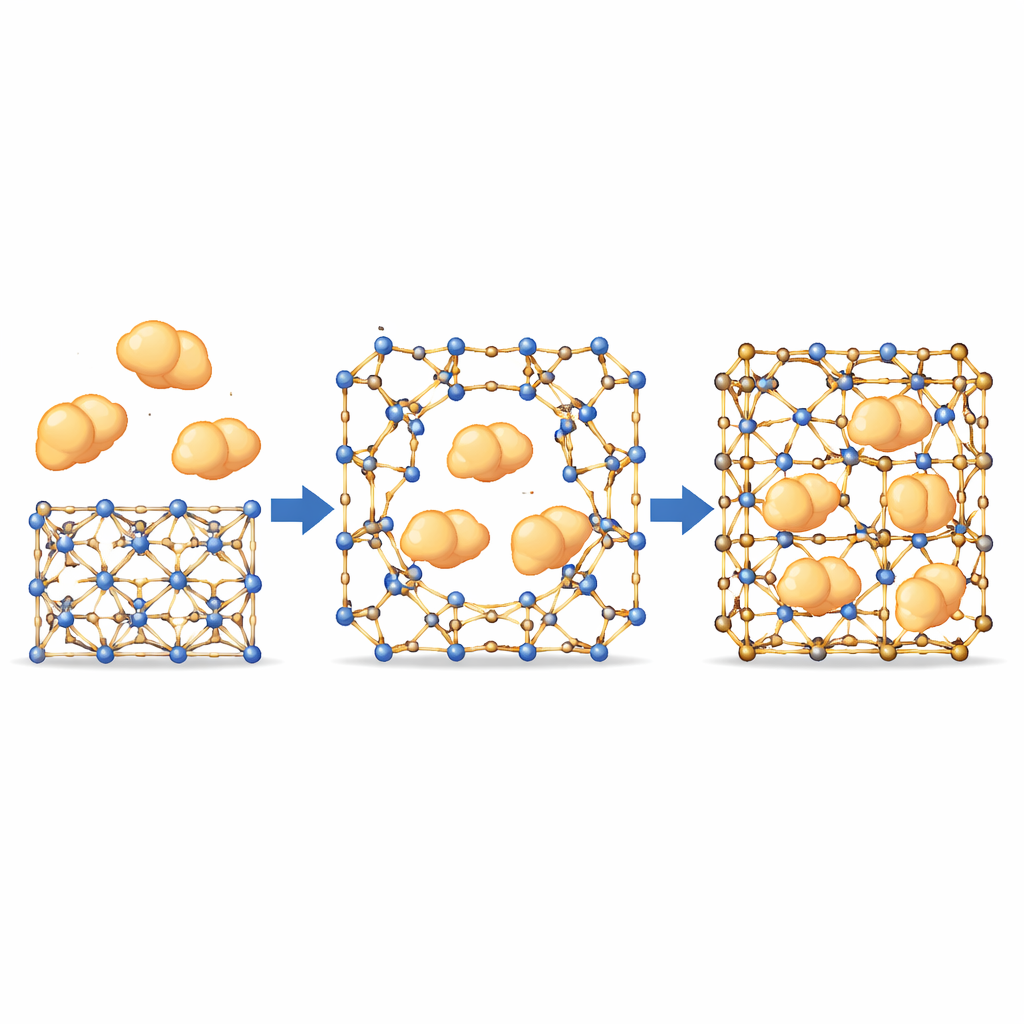
Laisser de grosses enzymes passer par de petits pores
Avec ce comportement de type porte en main, l’équipe a testé si de grandes enzymes — plus grandes que les pores nominaux du MOF — pouvaient toutefois être amenées à l’intérieur. En utilisant des protéines marquées par fluorescence et la microscopie confocale, ils ont observé les enzymes se déplacer de manière uniforme depuis la surface du cristal vers l’intérieur, suivant des trajectoires qui ne correspondaient pas aux canaux internes fixes. Cela suggère que des ouvertures temporaires se forment là où des liaisons dynamiques se séparent momentanément, permettant aux enzymes de s’infiltrer avant que le réseau ne « se répare » autour d’elles. De façon importante, des variantes plus robustes du matériau, où ces liaisons bougent à peine, ont montré presque aucune uptake d’enzyme, confirmant que le mouvement en ces sites est essentiel. Au travers d’un panel d’enzymes de tailles et de propriétés différentes, les MOFs les plus finement équilibrés ont atteint de fortes charges tout en conservant l’ordre cristallin.
Des catalyseurs plus solides et durables
Une fois à l’intérieur, les enzymes ont agi comme des catalyseurs robustes et réutilisables. Les auteurs ont étudié plusieurs protéines représentatives, y compris des enzymes notoirement sensibles à la chaleur, aux conditions alcalines et aux solvants organiques. Comparées aux mêmes enzymes libres en solution, les versions encapsulées ont conservé une grande partie de leur activité sous contrainte, et ont pu être utilisées sur plusieurs cycles réactionnels avec peu de perte de performance. Les MOFs dynamiques ont aussi permis la co‑encapsulation de deux enzymes coopérantes qui agissent en séquence pour fabriquer un bloc de construction sucré de valeur. Les loger toutes deux dans le même réseau a raccourci le trajet entre elles, améliorant l’efficacité de la réaction et permettant au système de fonctionner à répétition avec une production soutenue.
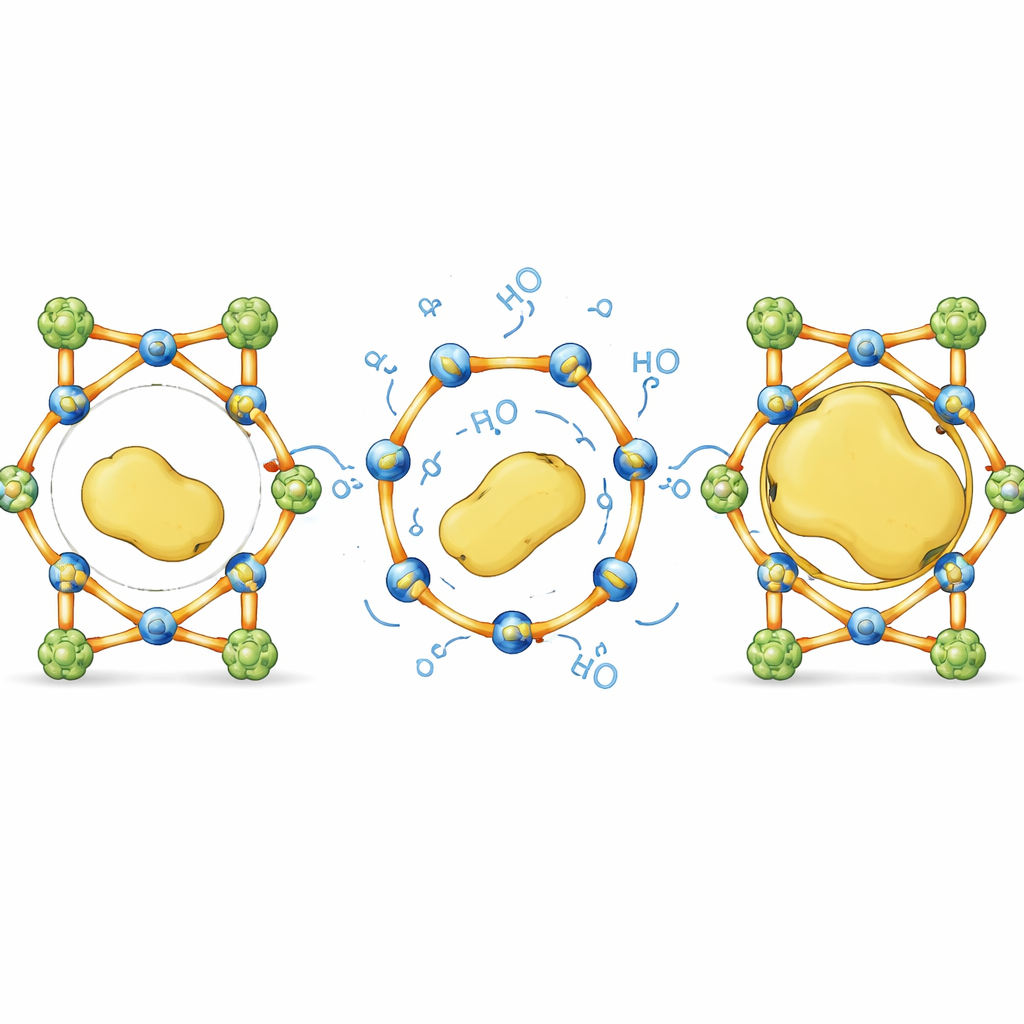
De limites de taille à une conception indépendante de la taille
En termes simples, ce travail transforme une éponge rigide à trous fixes en une cage intelligente dont les barreaux peuvent fléchir juste assez pour laisser entrer de grands invités, puis se refermer. En équilibrant soigneusement des supports incassables avec des liaisons sélectivement réversibles, les auteurs montrent qu’il est possible d’emballer des enzymes volumineuses et fragiles à l’intérieur de matériaux cristallins qui les excluraient normalement, sans sacrifier la structure ni la fonction. Cette approche pilotée par des liaisons dynamiques offre une recette générale pour concevoir des « hôtels pour enzymes » indépendants de la taille, avec le potentiel d’améliorer les bioréacteurs industriels, de rationaliser les synthèses en plusieurs étapes et de créer des technologies bio‑basées plus durables.
Citation: Li, Y., Qiao, M., Gao, L. et al. Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints. Nat Commun 17, 3642 (2026). https://doi.org/10.1038/s41467-026-70249-x
Mots-clés: immobilisation d’enzymes, matériaux métal‑organiques, bioréaction, liaisons de coordination dynamiques, cascades multi‑enzymatiques