Clear Sky Science · de
Dynamisch bindungsgetriebene Einkapselung von Enzymen in metallorganischen Gerüsten jenseits von Porengrößenbeschränkungen
Warum das Einfangen empfindlicher Helfer wichtig ist
Enzyme sind die winzigen Arbeitstiere der Natur und beschleunigen chemische Reaktionen, die alles antreiben, von lebenden Zellen bis zur industriellen Fertigung. Außerhalb ihres natürlichen Umfelds zerfallen diese empfindlichen Proteine jedoch schnell, was ihre wiederholte Nutzung im großen Maßstab erschwert. Dieser Artikel stellt eine Methode vor, Enzyme sicher in einem porösen kristallinen Material unterzubringen, sodass sie länger aktiv bleiben und wiederholt recycelt werden können. Entscheidend ist, dass das Team zeigt, wie man Enzyme einbringt, die tatsächlich größer sind als die eingebauten Öffnungen des Materials und so eine langjährige Größenbeschränkung umgeht, die viele vielversprechende Anwendungen in grüner Chemie und Medizin behindert hat.
Ein schützendes kristallines Haus bauen
Die Forschenden arbeiten mit metallorganischen Gerüsten, kurz MOFs — Festkörper aus Metallclustern, die durch organische „Stäbe“ zu einem geordneten Gerüst mit vielen Hohlräumen verbunden sind. MOFs sind als Unterkunft für Enzyme attraktiv, weil sie große innere Oberflächen und schützende Käfige bieten, die Proteine vor Hitze, Lösungsmitteln und rauen Bedingungen abschirmen können. Das Problem ist, dass viele nützliche Enzyme schlicht zu groß sind, um durch die engen Öffnungen der meisten MOFs hindurchzupassen. Frühere Lösungen befestigten Enzyme entweder an der Außenseite, was die Beladungsmenge begrenzte, oder versuchten, das MOF unter sehr schonenden Bedingungen um die Enzyme herum wachsen zu lassen, was nur für eine kleine Untergruppe von MOF‑Chemien funktioniert.
Kleine Tore hinzufügen, die sich öffnen und heilen
Um dieser Größenfalle zu entkommen, entwarfen die Autorinnen und Autoren eine Familie von MOFs, deren interne Verbindungen sich kurzzeitig lösen und wie selbstheilende Stiche wieder anheften können. Sie kombinierten sehr stabile Metall‑Carboxylat‑Cluster, die als starre Rückgratstruktur wirken, mit flexibleren Metall‑Pyridyl‑Bindungen, die als reversible „Tore“ fungieren. Durch den Austausch unterschiedlicher Metalle und die Variation der Länge der organischen Linker konnten sie fein einstellen, wie leicht sich diese Tore im Wasser öffnen lassen, ohne dass die gesamte Struktur auseinanderfällt. Messungen von Metallauslaugung, Röntgenbeugung und Computersimulationen zeigten dasselbe Bild: Im Wasser lockern sich nur die weicheren Verbindungen an bestimmten Metallstellen, während das robustere Rückgrat intakt bleibt und das gesamte Kristallgerüst bewahrt.
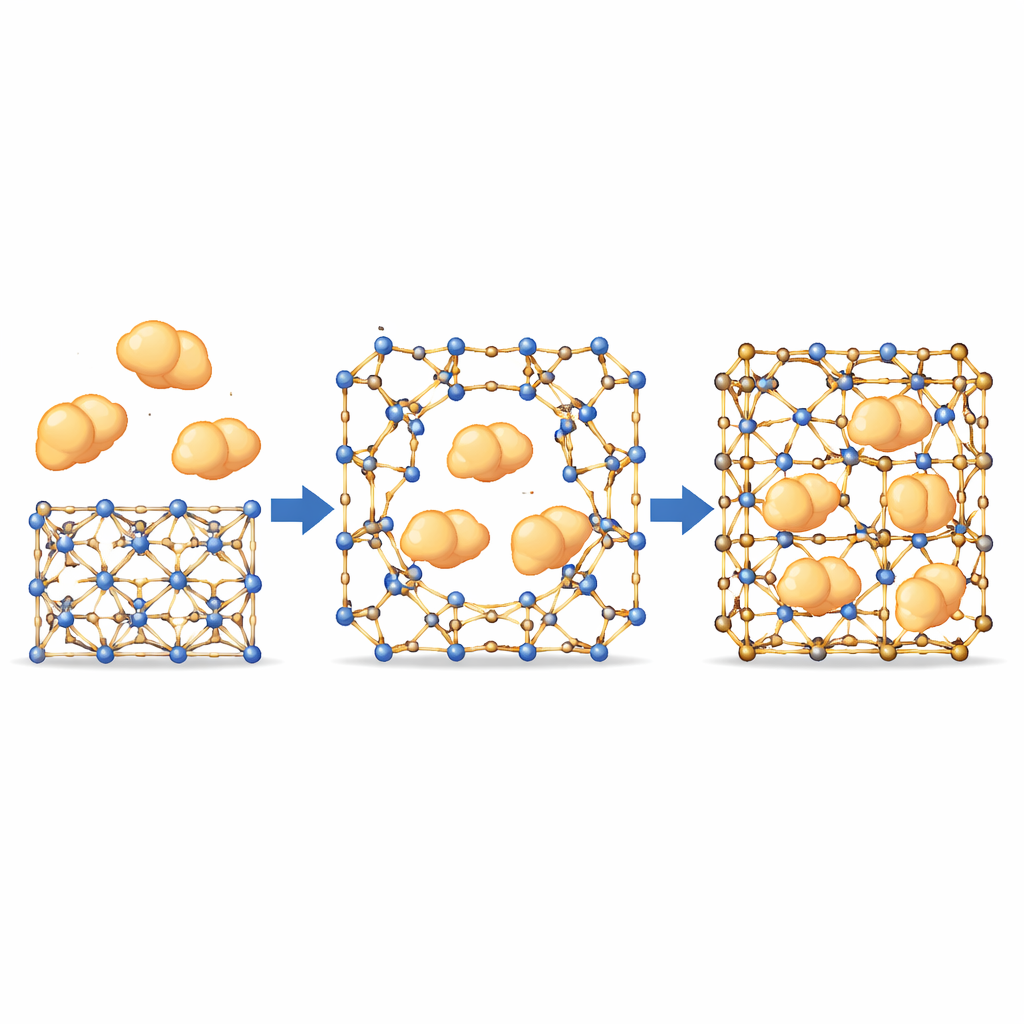
Große Enzyme durch kleine Poren schlüpfen lassen
Mit diesem torähnlichen Verhalten testete das Team, ob große Enzyme — größer als die nominalen Poren des MOF — dennoch hineingezogen werden können. Mit fluoreszenzmarkierten Proteinen und Konfokalmikroskopie verfolgten sie, wie die Enzyme gleichmäßig von der Kristalloberfläche ins Innere wanderten und dabei Pfade folgten, die nicht mit den festen inneren Kanälen übereinstimmten. Das deutet darauf hin, dass temporäre Öffnungen dort entstehen, wo dynamische Bindungen sich kurz trennen, wodurch die Enzyme eindringen können, bevor das Gerüst sich wieder „verheilt“. Wichtig ist, dass robustere Varianten des Materials, bei denen diese Bindungen kaum beweglich sind, nahezu keine Enzymaufnahmen zeigten — ein Beleg dafür, dass Bewegung an diesen Stellen wesentlich ist. Über eine Reihe von Enzymen mit unterschiedlichen Größen und Eigenschaften erreichten die am feinsten austarierten MOFs hohe Beladungen, während sie gleichzeitig ihre kristalline Ordnung beibehielten.
Stärkere, langlebigere Katalysatoren
Einmal innen, verhielten sich die Enzyme als robuste, wiederverwendbare Katalysatoren. Die Autorinnen und Autoren untersuchten mehrere repräsentative Proteine, darunter solche, die als besonders empfindlich gegenüber Hitze, alkalischen Bedingungen und organischen Lösungsmitteln gelten. Im Vergleich zu denselben Enzymen in freier Lösung behielten die einkapselten Varianten bei Belastung einen deutlich größeren Teil ihrer Aktivität und konnten über mehrere Reaktionszyklen mit geringem Leistungsverlust genutzt werden. Die dynamischen MOFs ermöglichten außerdem die gemeinsame Einkapselung zweier zusammenarbeitender Enzyme, die nacheinander eine wertvolle zuckerbasierte Baueinheit herstellen. Beide im gleichen Gerüst zu beherbergen verkürzte den Weg zwischen ihnen, steigerte die Reaktionseffizienz und erlaubte wiederholten Betrieb mit anhaltender Produktivität.
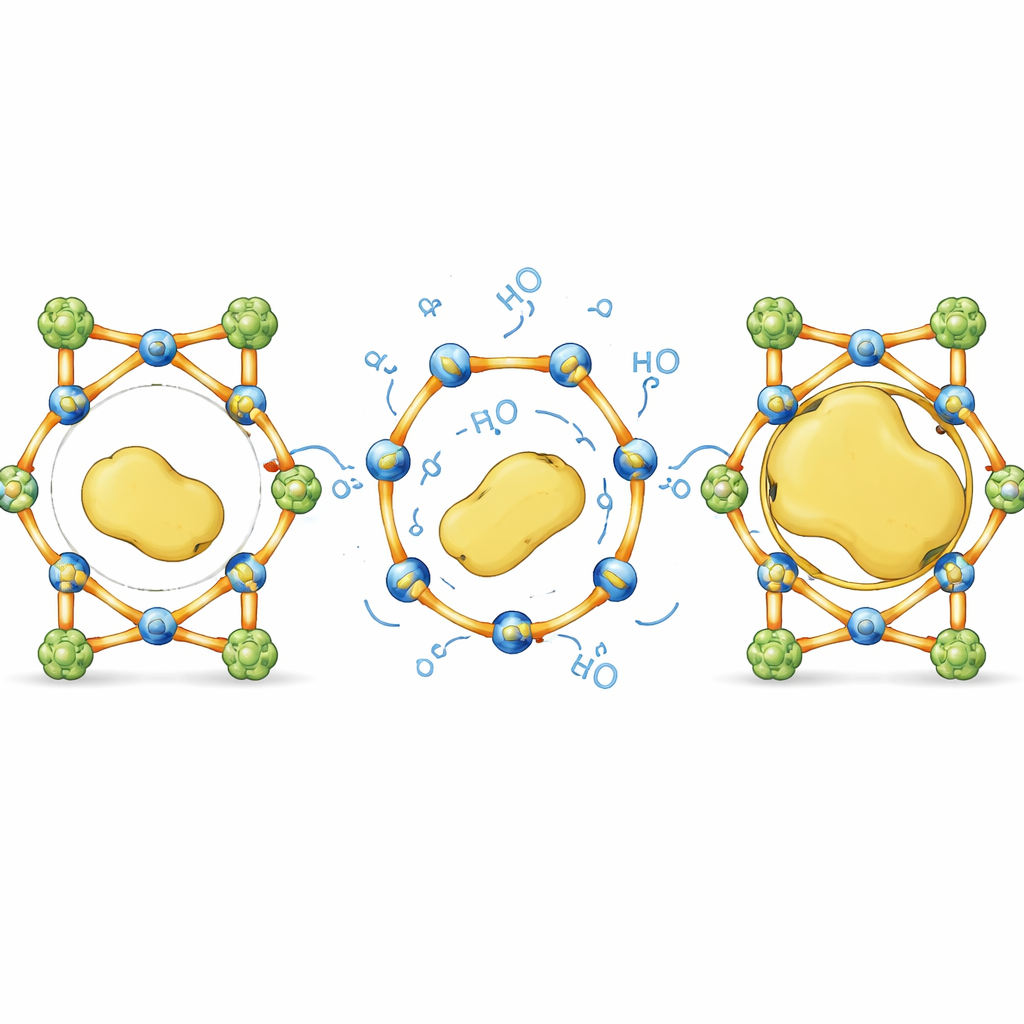
Von Größenlimits zu größenunabhängigem Design
Alltäglich gesprochen verwandelt diese Arbeit einen starren Schwamm mit festen Löchern in einen intelligenten Käfig, dessen Gitterstäbe gerade so nachgeben, dass große Gäste eintreten können, und dann wieder in ihre Position schnappen. Durch das sorgfältige Ausbalancieren unzerbrechlicher Stützen mit selektiv reversiblen Verbindungen zeigen die Autorinnen und Autoren, dass es möglich ist, sperrige, empfindliche Enzyme in kristalline Materialien zu packen, die sie normalerweise ausschließen würden, ohne Struktur oder Funktion zu opfern. Dieser dynamisch bindungsgetriebene Ansatz bietet ein allgemeines Rezept zur Gestaltung größenunabhängiger „Enzym‑Hotels“ mit Potenzial, industrielle Biokatalysatoren zu verbessern, mehrstufige Synthesen zu straffen und langlebigere bio‑basierte Technologien zu schaffen.
Zitation: Li, Y., Qiao, M., Gao, L. et al. Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints. Nat Commun 17, 3642 (2026). https://doi.org/10.1038/s41467-026-70249-x
Schlüsselwörter: Enzymimmobilisierung, metallorganische Gerüste, Biokatalyse, dynamische Koordinationsbindungen, Multi‑Enzym‑Kaskaden