Clear Sky Science · pt
Encapsulamento de enzimas impulsionado por ligações dinâmicas em estruturas metal-orgânicas além das limitações do tamanho dos poros
Por que prender ajudantes frágeis importa
Enzimas são as pequenas máquinas da natureza, acelerando reações químicas que alimentam desde células vivas até processos industriais. Mas fora de seus lares naturais, essas proteínas delicadas se degradam rapidamente, o que dificulta seu reúso em grande escala. Este artigo apresenta uma maneira de alojar enzimas com segurança dentro de um material cristalino poroso, de modo que permaneçam ativas por mais tempo e possam ser recicladas repetidamente. Fundamentalmente, a equipe demonstra como inserir enzimas que na verdade são maiores do que as aberturas incorporadas no material, contornando uma limitação de tamanho de longa data que vinha restringindo muitas aplicações promissoras em química verde e medicina.
Construindo uma casa cristalina protetora
Os pesquisadores trabalharam com estruturas metal-orgânicas, ou MOFs — sólidos formados por aglomerados metálicos ligados por "vigas" orgânicas em uma malha ordenada repleta de espaços vazios. MOFs são acomodações atraentes para enzimas porque oferecem grande área de superfície interna e gaiolas protetoras que podem blindar proteínas contra calor, solventes e condições agressivas. O problema é que muitas enzimas úteis são simplesmente grandes demais para passar pelas janelas estreitas da maioria dos MOFs. Soluções anteriores ou prendiam as enzimas na superfície externa, limitando a carga possível, ou tentavam crescer o MOF ao redor das enzimas sob condições muito suaves, o que funciona apenas para um pequeno subconjunto de químicas de MOF.
Adicionando pequenos portões que abrem e cicatrizam
Para escapar dessa armadilha de tamanho, os autores desenharam uma família de MOFs cujas conexões internas podem desencaixar e se recolocar brevemente, como pontos de sutura autorreparáveis. Eles combinaram aglomerados metal–carboxilato muito estáveis, que atuam como uma espinha dorsal rígida, com ligações metal–piridil mais flexíveis que se comportam como "portões" reversíveis. Ao trocar metais diferentes e alterar o comprimento dos ligantes orgânicos, foi possível ajustar finamente com que facilidade esses portões se abrem em água sem causar a desintegração da estrutura inteira. Medições de lixiviação de metal, difração de raios X e simulações computacionais convergiram para a mesma imagem: em água, apenas as conexões mais flexíveis em sítios metálicos específicos afrouxam, enquanto a espinha dorsal mais resistente permanece intacta, preservando o arcabouço cristalino global.
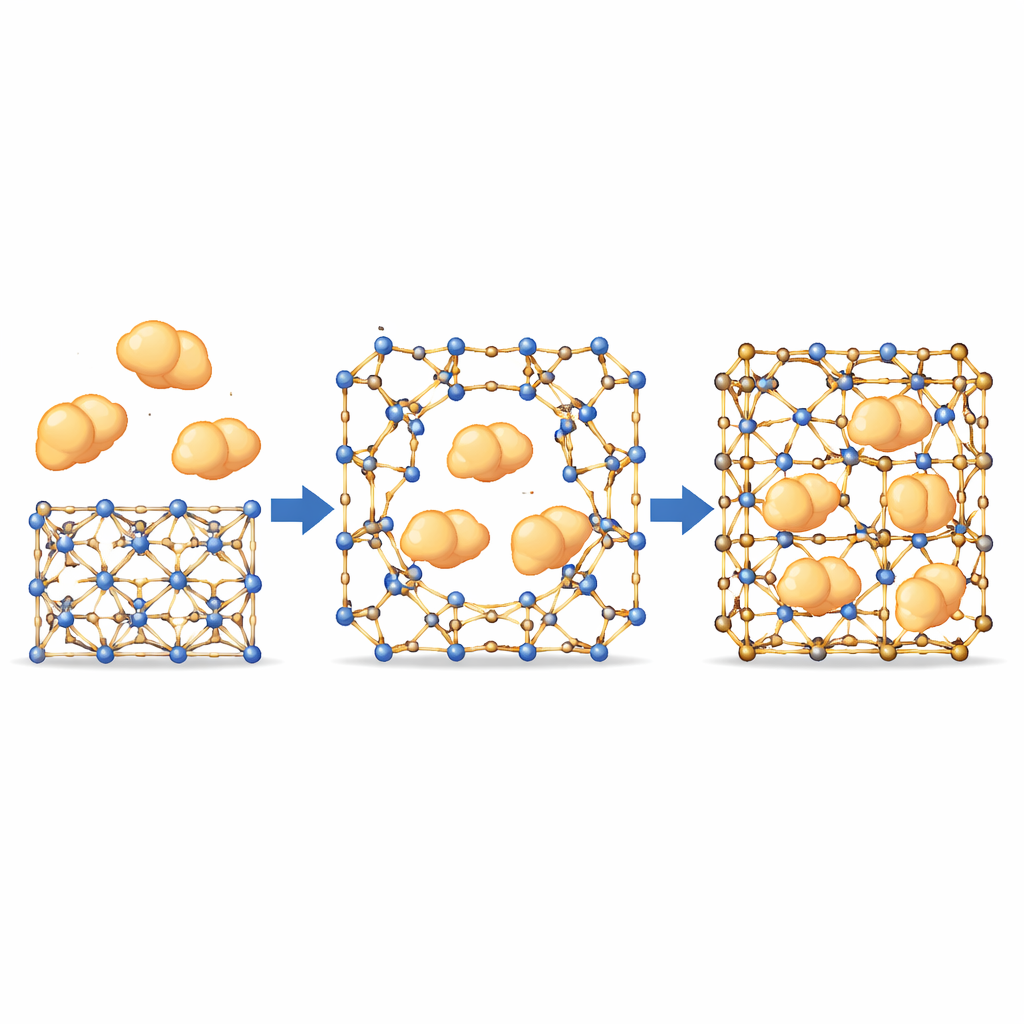
Deixando enzimas grandes passarem por poros pequenos
Com esse comportamento em forma de portão, a equipe testou se enzimas grandes — maiores que os poros nominais do MOF — ainda poderiam ser incorporadas. Usando proteínas marcadas com fluoróforo e microscopia confocal, observaram as enzimas moverem-se de forma uniforme da superfície do cristal em direção ao interior, seguindo trajetórias que não correspondiam aos canais internos fixos. Isso sugere que aberturas temporárias se formam onde ligações dinâmicas se separam brevemente, permitindo que as enzimas infiltrem antes que a estrutura "cicatrize" ao redor delas. É importante notar que variantes mais rígidas do material, nas quais essas ligações praticamente não se movem, mostraram quase nenhuma incorporação de enzimas, confirmando que o movimento nesses sítios é essencial. Em um painel de enzimas com tamanhos e propriedades variados, os MOFs com o balanço mais fino atingiram alta carga mantendo a ordem cristalina.
Catalisadores mais fortes e duradouros
Uma vez no interior, as enzimas se comportaram como catalisadores robustos e reutilizáveis. Os autores examinaram várias proteínas representativas, incluindo algumas notoriamente sensíveis ao calor, a condições alcalinas e a solventes orgânicos. Em comparação com as mesmas enzimas em solução livre, as versões encapsuladas mantiveram muito mais de sua atividade quando submetidas a estresse, e puderam ser recicladas em múltiplas corridas reacionais com pouca perda de desempenho. Os MOFs dinâmicos também permitiram a coencapsulação de duas enzimas cooperativas que atuam em sequência para produzir um valioso bloco de construção à base de açúcar. Abrigar ambas dentro do mesmo arcabouço encurtou o trajeto entre elas, aumentando a eficiência da reação e permitindo que o sistema operasse repetidamente com produção sustentada.
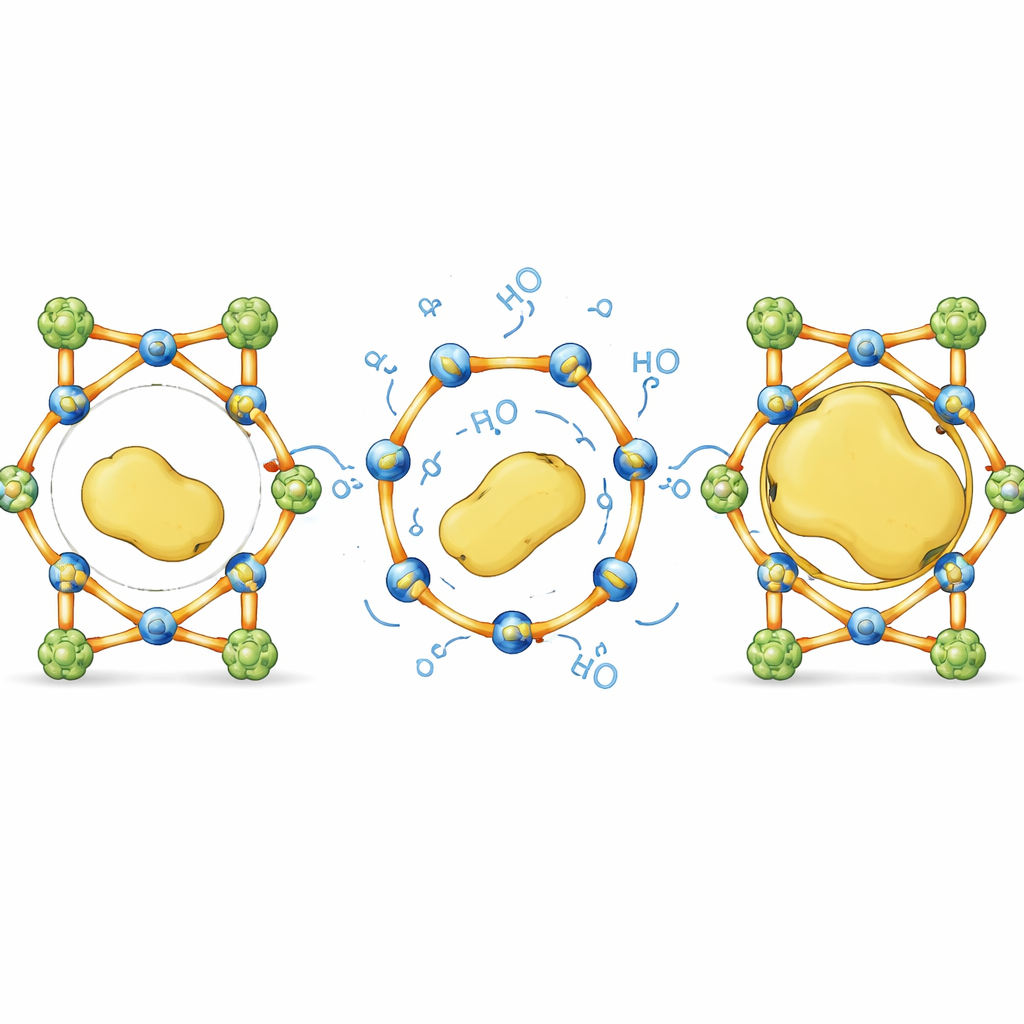
De limites de tamanho a um desenho indiferente ao tamanho
Em termos cotidianos, este trabalho transforma uma esponja rígida com furos fixos em uma gaiola inteligente cujas barras podem flexionar o suficiente para admitir grandes hóspedes e depois voltar ao lugar. Ao equilibrar cuidadosamente suportes inquebráveis com ligações reversíveis seletivas, os autores mostram que é possível acomodar enzimas volumosas e frágeis dentro de materiais cristalinos que normalmente as excluiriam, sem sacrificar estrutura ou função. Essa abordagem guiada por ligações dinâmicas oferece uma receita geral para projetar "hotéis de enzimas" independentes de tamanho, com potencial para melhorar biocatalisadores industriais, simplificar sínteses em múltiplas etapas e criar tecnologias bio‑baseadas mais duráveis.
Citação: Li, Y., Qiao, M., Gao, L. et al. Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints. Nat Commun 17, 3642 (2026). https://doi.org/10.1038/s41467-026-70249-x
Palavras-chave: imobilização de enzimas, estruturas metal-orgânicas, biocatálise, ligações de coordenação dinâmicas, cascatas multi-enzimáticas