Clear Sky Science · ru
Динамическое удержание ферментов в металло‑органических каркасах, выходящее за пределы ограничений размера пор
Почему важно защищать хрупких помощников
Ферменты — крошечные рабочие лошадки природы, ускоряющие химические реакции, которые поддерживают все: от живых клеток до промышленного производства. Но вне их естественной среды эти деликатные белки быстро разрушаются, что затрудняет их повторное использование в масштабах. В этой статье описан способ аккуратно поместить ферменты внутрь пористого кристаллического материала, чтобы они дольше сохраняли активность и могли перерабатываться многократно. Ключевой момент: авторы демонстрируют, как вводить ферменты, размеры которых фактически превышают встроенные отверстия материала, обходя долгое время служившее барьером ограничение размера — фактор, тормозивший многие перспективные применения в зеленой химии и медицине.
Построение защитного кристаллического дома
Исследователи работают с металло‑органическими каркасами, или МОКами — твердыми телами, состоящими из металлических кластеров, соединенных органическими «балками» в упорядоченную решетку с пустотами. МОКи привлекательны как укрытие для ферментов потому, что предлагают большую внутреннюю площадь и защитные «клетки», которые могут оградить белки от тепла, растворителей и жестких условий. Загвоздка в том, что многие полезные ферменты просто слишком велики, чтобы протиснуться через узкие окна большинства МОКов. Ранее предложенные решения либо прикрепляли ферменты к внешней поверхности, что ограничивало загрузку, либо пытались вырастить МОК вокруг ферментов в очень щадящих условиях, что работает лишь для небольшого числа химий МОКов.
Добавление крошечных ворот, которые открываются и заживают
Чтобы выйти из этой ловушки размера, авторы спроектировали семейство МОКов, внутренние соединения которых могут кратковременно расстегиваться и снова прикрепляться, как самозалечивающиеся стежки. Они комбинировали очень стабильные металло‑карбоксилатные кластеры, служащие жестким каркасом, с более гибкими металло‑пиридиновыми связями, которые действуют как обратимые «ворота». Подбирая различные металлы и изменяя длину органических звеньев, авторы тонко настраивали, насколько легко эти ворота открываются в воде, не разрушая при этом всю структуру. Измерения вымывания металлов, рентгеновская дифракция и компьютерные моделирования давали единый образ: в воде только более «мягкие» связи в определенных металловых узлах ослабляют, тогда как прочный каркас остается целым, сохраняя общую кристаллическую структуру.
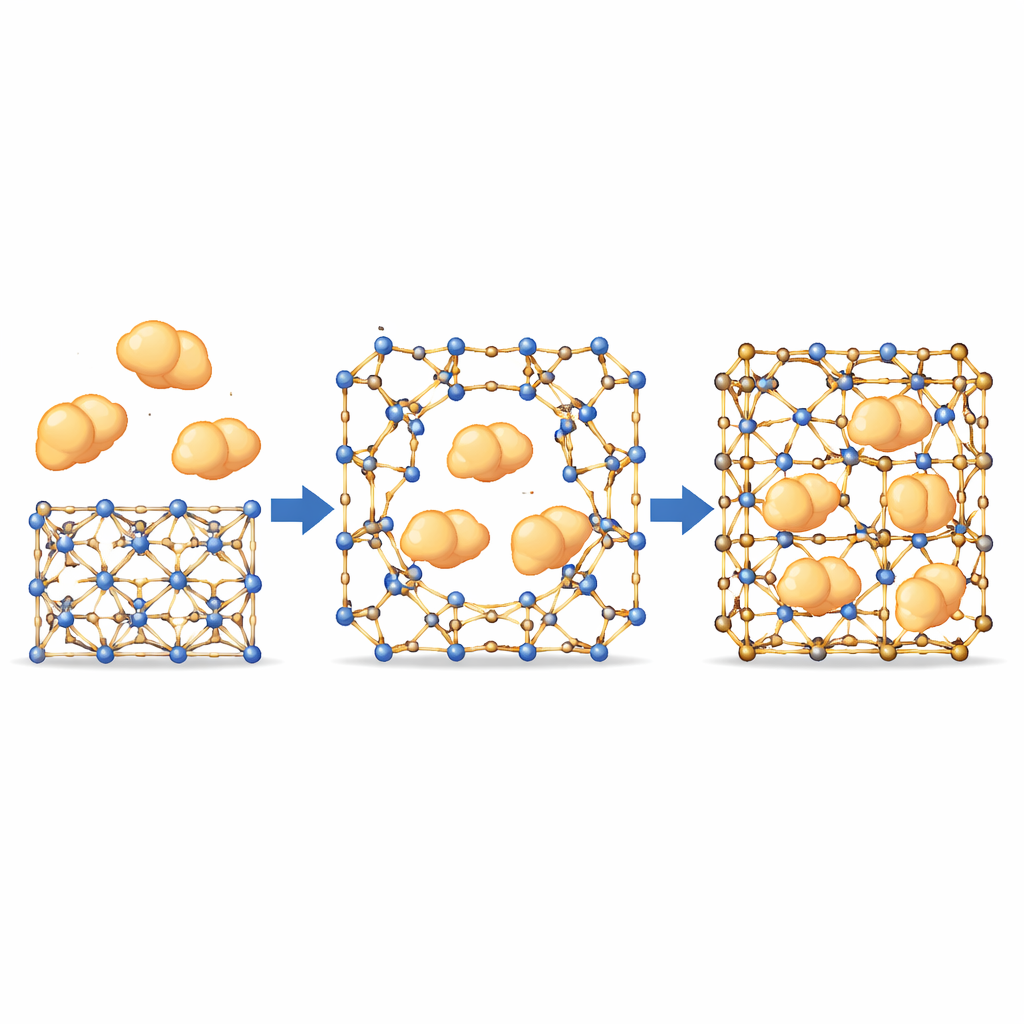
Как крупные ферменты проходят через маленькие поры
Имея такое поведение «ворот», команда проверила, можно ли заселить внутрь большие ферменты — крупнее номинальных пор МОКа. С помощью флуоресцентно меченых белков и конфокальной микроскопии они наблюдали, как ферменты равномерно перемещаются от поверхности кристалла вглубь, по траекториям, которые не совпадали с фиксированными внутренними каналами. Это указывает на то, что образуются временные отверстия там, где динамические связи на мгновение размыкаются, позволяя ферментам проникнуть, прежде чем каркас «заживет» вокруг них. Важно, что более жесткие варианты материала, в которых эти связи едва шевелятся, практически не поглощали ферменты, что подтверждает необходимость подвижности именно в этих узлах. В панеле ферментов с различными размерами и свойствами наиболее точно сбалансированные МОКи обеспечили высокую загрузку, сохранив при этом кристаллический порядок.
Более прочные, дольше служащие катализаторы
Оказавшись внутри, ферменты вели себя как надежные многократно используемые катализаторы. Авторы изучили несколько типичных белков, в том числе те, которые особенно чувствительны к теплу, щелочному окружению и органическим растворителям. По сравнению с теми же ферментами в свободном растворе инкапсулированные версии гораздо лучше сохраняли активность при стресс‑воздействиях и могли выдержать несколько циклов реакций с минимальной потерей эффективности. Динамические МОКи также позволили совместно инкапсулировать две сотрудничающие ферменты, работающие последовательно для получения ценного сахарного строительного блока. Размещение обоих в одном каркасе сократило расстояние между ними, повысив эффективность реакции и обеспечив возможность многократной работы с устойчивым выходом.
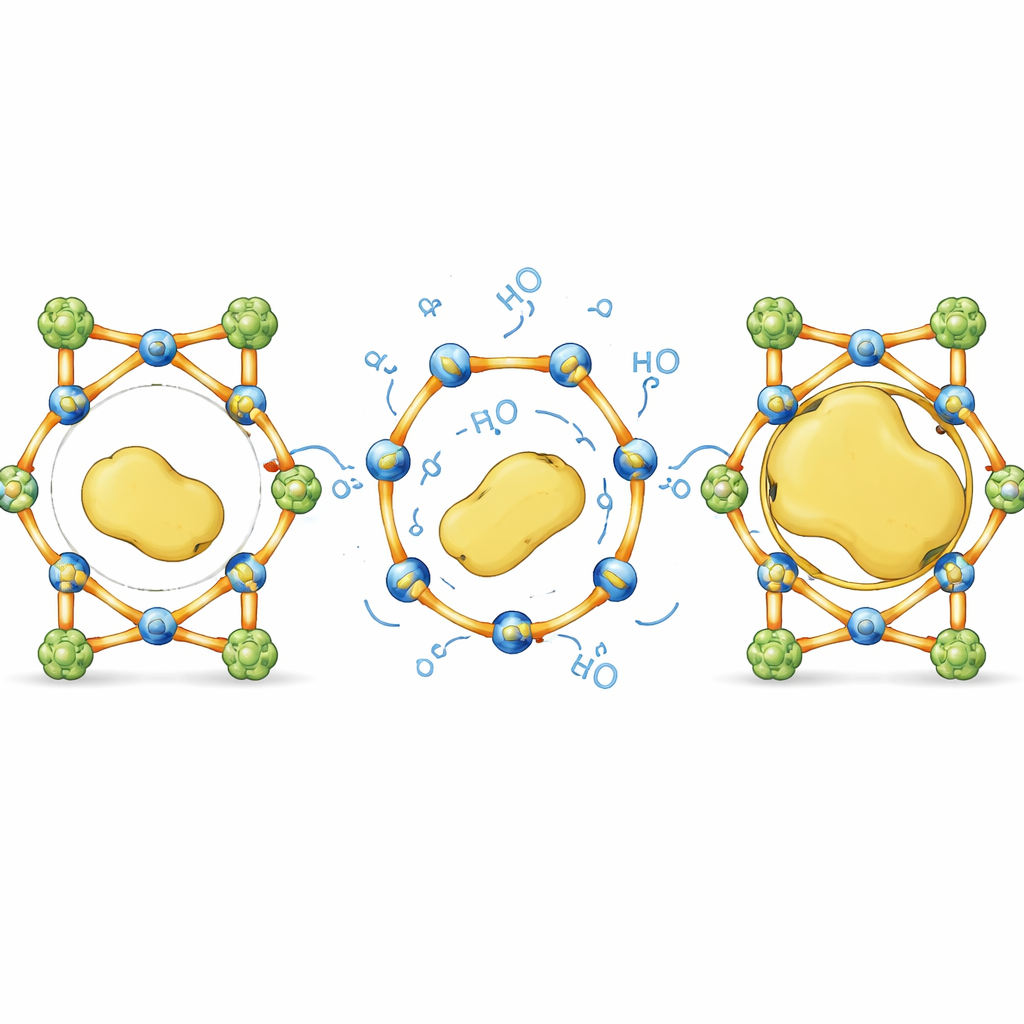
От ограничений размера к дизайну, независимому от размера
В повседневном представлении эта работа превращает жесткую губку с фиксированными отверстиями в умную клетку, чьи прутья могут немного изгибаться, чтобы впустить крупных гостей, а затем снова защелкнуться. Тщательно уравновешивая неразрушимые опоры и выборочно обратимые связи, авторы показывают, что возможно упаковывать громоздкие, хрупкие ферменты в кристаллические материалы, которые обычно бы их исключали, не жертвуя ни структурой, ни функцией. Этот подход, основанный на динамических связях, предлагает универсальный рецепт для проектирования «гостиниц для ферментов», не зависящих от размера, с потенциалом улучшить промышленные биокатализаторы, упростить многоступенчатые синтезы и создать более долговечные био‑технологии.
Цитирование: Li, Y., Qiao, M., Gao, L. et al. Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints. Nat Commun 17, 3642 (2026). https://doi.org/10.1038/s41467-026-70249-x
Ключевые слова: иммобилизация ферментов, металло‑органические каркасы, биокатализ, динамические координационные связи, многоферментные каскады