Clear Sky Science · tr
Gözyaşı boyutu sınırlamalarını aşan dinamik bağ kontrollü enzim kapsülasyonu metal–organik kafeslerde
Narin yardımcıları hapsetmenin önemi
Enzimler, canlı hücrelerden endüstriyel üretime kadar her şeyi besleyen kimyasal reaksiyonları hızlandıran doğanın küçük işçileri gibidir. Ancak doğal ortamlarının dışındayken bu hassas proteinler çabucak bozulur ve büyük ölçekte yeniden kullanımı zorlaşır. Bu makale, enzimleri gözenekli kristal bir malzemenin içine güvenle yerleştirme yöntemini bildirir; böylece enzimler daha uzun süre aktif kalır ve tekrar tekrar geri dönüştürülebilir. Kritik olarak, ekip malzemenin yerleşik açıklıklarından daha büyük olan enzimleri bile içeri sokmanın yolunu gösterir; bu da yeşil kimya ve tıpta birçok umut verici uygulamayı geride tutan uzun süredir devam eden bir boyut sınırlamasını aşar.
Koruyucu bir kristal ev inşa etmek
Araştırmacılar metal–organik kafesler (MOF’lar) ile çalışıyor — metal kümelerinin organik “çubuklarla” bağlanarak boşluklarla dolu düzenli bir iskelet oluşturduğu katı malzemeler. MOF’lar, geniş iç yüzey alanları ve proteinleri ısı, çözücüler ve zorlu koşullardan koruyabilecek kafesler sunduğu için enzimler için çekici konaklardır. Sorun şu ki, birçok yararlı enzim çoğu MOF’un dar pencerelerinden sıkışıp geçecek kadar küçük değildir. Daha önceki çözümler ya enzimleri dış yüzeye sabitleyerek yüklenecek miktarı sınırladı ya da MOF’u enzimlerin etrafında çok nazik koşullarda büyütmeye çalıştı; bu da yalnızca sınırlı bir MOF kimyası alt kümesi için işe yarıyordu.
Açılan ve iyileşen küçük kapılar eklemek
Bu boyut tuzağından kaçmak için yazarlar, iç bağlantılarının kısa süreliğine çözülebileceği ve kendiliğinden iyileşen dikişler gibi tekrar bağlanabileceği bir MOF ailesi tasarladı. Çok kararlı metal–karboksilat kümelerini, sert bir omurga görevi gören yapıyı, daha esnek ve tersinir “kapılar” gibi davranan metal–piridil bağlantılarla birleştirdiler. Farklı metallerin yer değiştirilmesi ve organik bağlayıcıların uzunluğunun değiştirilmesiyle, bu kapıların suda ne kadar kolay açılacağını bütün yapıyı dağıtmadan hassas bir şekilde ayarlayabildiler. Metal sızıntısı ölçümleri, X ışını kırınımı ve bilgisayar simülasyonları hep aynı resmi gösterdi: suda, sadece belirli metal noktalarındaki daha yumuşak bağlantılar gevşerken, daha sağlam omurga bütünlüğü koruyarak genel kristal iskeleti muhafaza ediyor.
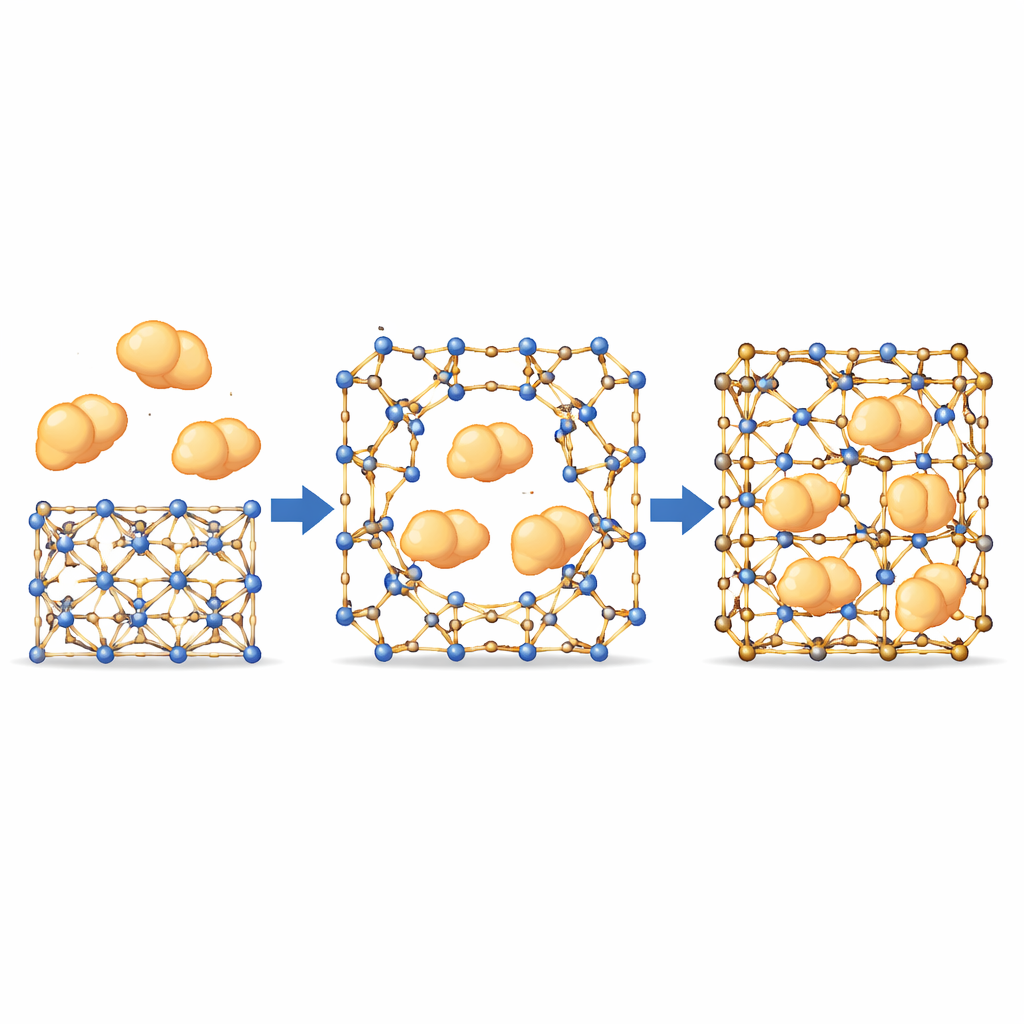
Büyük enzimlerin küçük gözeneklerden geçmesine izin vermek
Kapı benzeri bu davranış elde edildiğinde, ekip nominal gözeneklerden daha büyük olan büyük enzimlerin yine de içeri çekilip çekilemeyeceğini test etti. Floresan etiketli proteinler ve konfokal mikroskopi kullanarak enzimlerin kristal yüzeyinden içeri doğru homojen şekilde hareket ettiğini izlediler; izlenen yollar sabit iç kanallarla örtüşmüyordu. Bu, dinamik bağların kısa süreli ayrıldığı yerlerde geçici açıklıkların oluştuğunu ve enzimlerin iskelet “iyileşmeden” önce içeri sızmasına izin verdiğini düşündürüyor. Önemli olarak, bu bağların neredeyse hiç hareket etmediği daha sert varyantlar neredeyse hiç enzim almamış; bu da bu bölgelerdeki hareketin gerekli olduğunu doğruluyor. Farklı boyut ve özelliklere sahip enzim panelinde, en dengeli MOF’lar yüksek dolum elde ederken kristal düzenlerini koruyabildi.
Daha güçlü, daha uzun ömürlü katalizörler
İçeride, enzimler sağlam, yeniden kullanılabilir katalizörler olarak davrandı. Yazarlar ısıya, alkalin koşullara ve organik çözücülere karşı özellikle hassas olanlar da dahil olmak üzere birkaç temsilci proteini inceledi. Aynı enzimlerin çözelti içindeki serbest hallerine kıyasla, kapsüllenmiş versiyonlar stres altında çok daha fazla aktivitesini korudu ve çok sayıda reaksiyon döngüsü boyunca performansını büyük ölçüde kaybetmeden yinelenebildi. Dinamik MOF’lar ayrıca ardışık olarak çalışan iki işbirlikçi enzimin birlikte kapsüllenmesine de olanak verdi; bu enzimler değerli bir şeker bazlı yapı taşı üretiyordu. Her ikisinin aynı kafes içinde barındırılması aralarındaki yolu kısalttı, reaksiyon verimliliğini artırdı ve sistemin sürekli çıktı ile tekrar tekrar çalışmasına izin verdi.
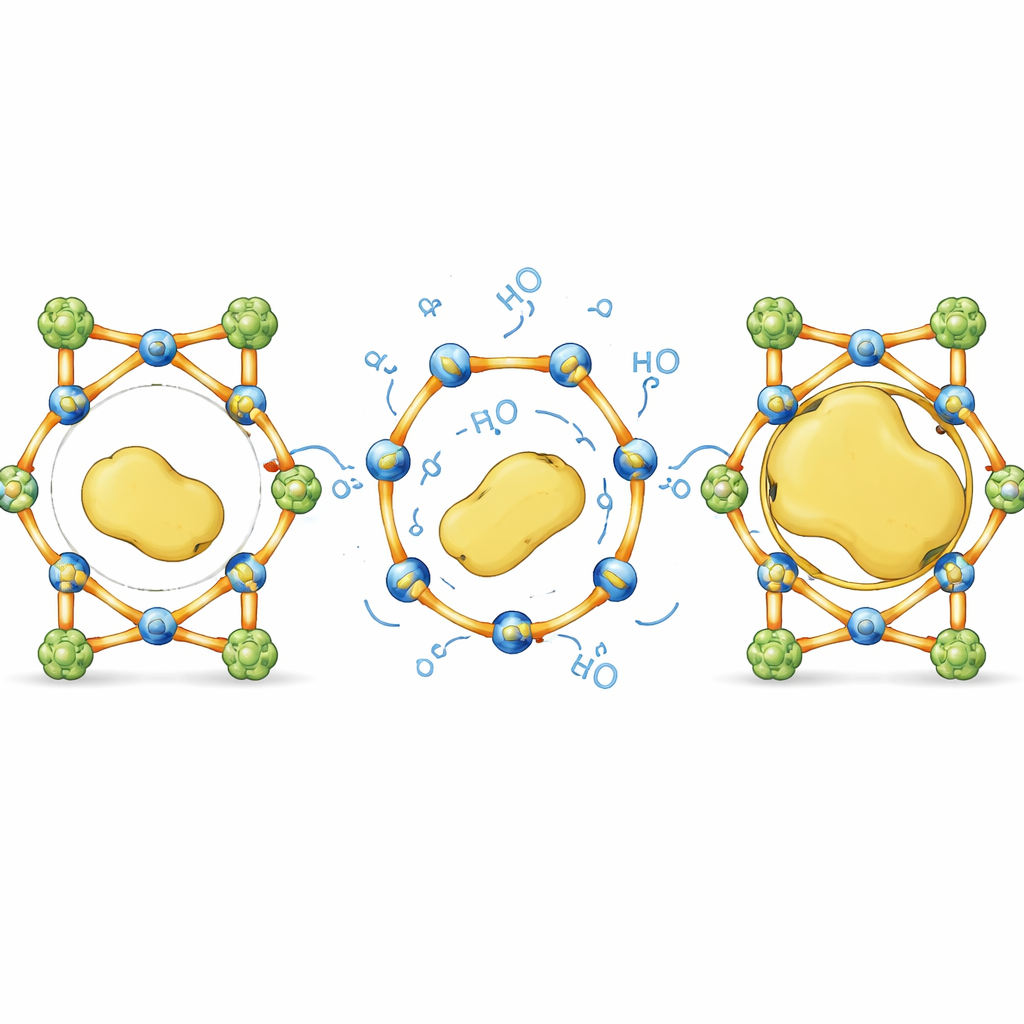
Boyut sınırlarından boyuta duyarsız tasarıma
Günlük ifadeyle, bu çalışma sabit delikli katı bir süngeri, büyük misafirleri kabul etmek için çubukları yeterince esneyebilen ve sonra yerine geri çarpabilen akıllı bir kafese dönüştürüyor. Kırılmaz destekleri seçici olarak tersinir bağlantılarla dikkatle dengeleyerek, yazarlar normalde onları dışlayacak olan kristal malzemelerin içine hantal, narin enzimleri paketlemenin; yapı veya işlevden ödün vermeden mümkün olduğunu gösteriyor. Bu dinamik bağ odaklı yaklaşım, endüstriyel biokatalizörleri iyileştirme, çok adımlı sentezleri hızlandırma ve daha dayanıklı biyolojik temelli teknolojiler oluşturma potansiyeline sahip boyuttan bağımsız “enzim otelleri” tasarlamak için genel bir reçete sunuyor.
Atıf: Li, Y., Qiao, M., Gao, L. et al. Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints. Nat Commun 17, 3642 (2026). https://doi.org/10.1038/s41467-026-70249-x
Anahtar kelimeler: enzim immobilizasyonu, metal-organik kafesler, biokataliz, dinamik koordinasyon bağları, çoklu enzim kaskadları