Clear Sky Science · nl
Dynamische bindingsgestuurde inkapseling van enzymen in metaal‑organische raamwerken voorbij poriegroottebeperkingen
Waarom het inbouwen van kwetsbare helpers ertoe doet
Enzymen zijn de kleine werkpaarden van de natuur: ze versnellen chemische reacties die alles aandrijven, van levende cellen tot industriële productie. Buiten hun natuurlijke omgeving vallen deze gevoelige eiwitten echter snel uiteen, waardoor hergebruik op grote schaal moeilijk wordt. Dit artikel beschrijft een manier om enzymen veilig in een poreus kristallijn materiaal te plaatsen, zodat ze langer actief blijven en herhaaldelijk kunnen worden ingezet. Cruciaal is dat het team laat zien hoe je enzymen kunt binnenbrengen die groter zijn dan de ingebouwde openingen van het materiaal, waarmee een lang bestaande groottebegrenzing wordt omzeild die veel veelbelovende toepassingen in groene chemie en geneeskunde in de weg stond.
Het bouwen van een beschermend kristallen huis
De onderzoekers werken met metaal‑organische raamwerken, of MOF’s — vaste stoffen opgebouwd uit metaalclusters verbonden door organische “spanten” tot een geordend skelet vol lege ruimtes. MOF’s vormen aantrekkelijke behuizingen voor enzymen omdat ze grote interne oppervlaktes en beschermende kooien bieden die eiwitten kunnen afschermen van hitte, oplosmiddelen en agressieve omstandigheden. Het probleem is dat veel nuttige enzymen simpelweg te groot zijn om door de smalle vensters van de meeste MOF’s te passen. Eerdere oplossingen bevestigden enzymen aan de buitenzijde, wat de laadtoestand beperkte, of probeerden de MOF rondom enzymen te laten groeien onder zeer milde condities, wat slechts werkt voor een kleine subset van MOF‑chemieën.
Het toevoegen van kleine poorten die openen en herstellen
Om deze grootteval te ontsnappen, ontwierpen de auteurs een familie MOF’s waarvan de interne verbindingen tijdelijk los kunnen komen en weer vastklikken als zelfherstellende steken. Ze combineerden zeer stabiele metaal‑carboxylaatclusters, die als een robuust geraamte fungeren, met flexibelere metaal‑pyridylverbindingen die zich gedragen als omkeerbare “poorten.” Door verschillende metalen te wisselen en de lengte van de organische schakels aan te passen, konden ze nauwkeurig regelen hoe gemakkelijk deze poorten in water opengaan zonder dat het gehele materiaal instort. Metingen van metaaluitloging, röntgendiffractie en computersimulaties wezen allemaal naar hetzelfde beeld: in water versoepelen alleen de soepelere verbindingen op specifieke metaalplaatsen, terwijl het steviger geraamte intact blijft en het algehele kristalraamwerk bewaart.
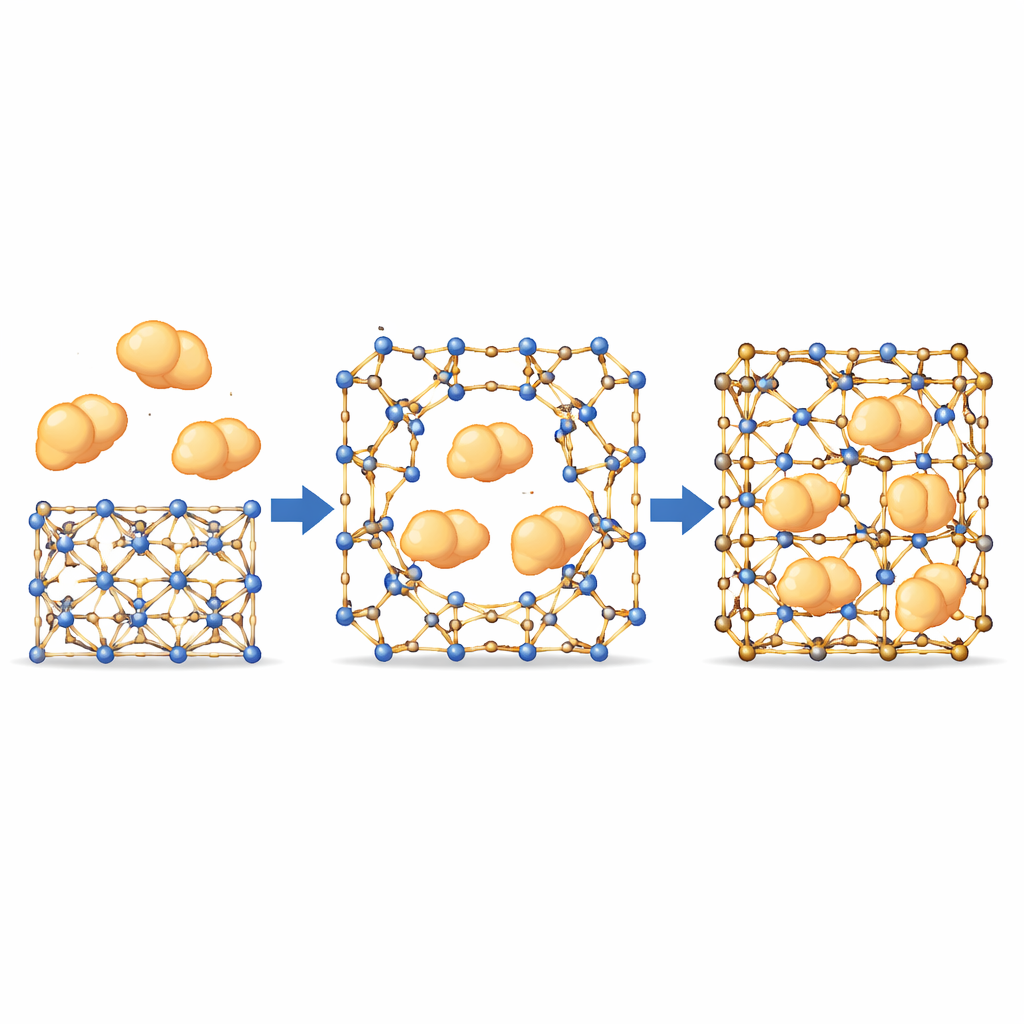
Grote enzymen door kleine poriën laten glippen
Met dit poortachtige gedrag in handen testte het team of grote enzymen — groter dan de nominale poriën van de MOF — toch naar binnen konden worden getrokken. Met fluorescente labels op de eiwitten en confocale microscopie volgden ze hoe de enzymen uniform van het kristaloppervlak naar het interieur bewogen, langs paden die niet overeenkwamen met de vaste interne kanalen. Dit suggereert dat tijdelijke openingen ontstaan waar dynamische bindingen kort loslaten, waardoor de enzymen kunnen binnendringen voordat het raamwerk eromheen “herstelt.” Belangrijk is dat stevigere varianten van het materiaal, waar deze bindingen nauwelijks bewegen, vrijwel geen enzymopname toonden, wat bevestigt dat beweging op deze plaatsen essentieel is. Over een reeks enzymen met verschillende groottes en eigenschappen haalden de het meest precies afgestelde MOF’s hoge ladingspercentages terwijl ze hun kristalorde behielden.
Sterkere, duurzamer katalysatoren
Eens binnen gedroegen de enzymen zich als robuuste, herbruikbare katalysatoren. De auteurs onderzochten meerdere representatieve eiwitten, waaronder exemplaren die berucht zijn vanwege hun gevoeligheid voor hitte, basische omstandigheden en organische oplosmiddelen. Vergeleken met dezelfde enzymen in oplossing behielden de ingekapselde versies veel meer van hun activiteit onder stress en konden ze door meerdere reactierondes worden gehaald met weinig prestatieverlies. De dynamische MOF’s maakten ook het co‑inkapselen van twee samenwerkende enzymen mogelijk die opeenvolgend een waardevol suikergebaseerd bouwblok produceren. Door beide in hetzelfde raamwerk te huisvesten werd de afstand tussen hen verkort, wat de reactiewaarde verhoogde en het systeem in staat stelde herhaaldelijk met constante opbrengst te draaien.
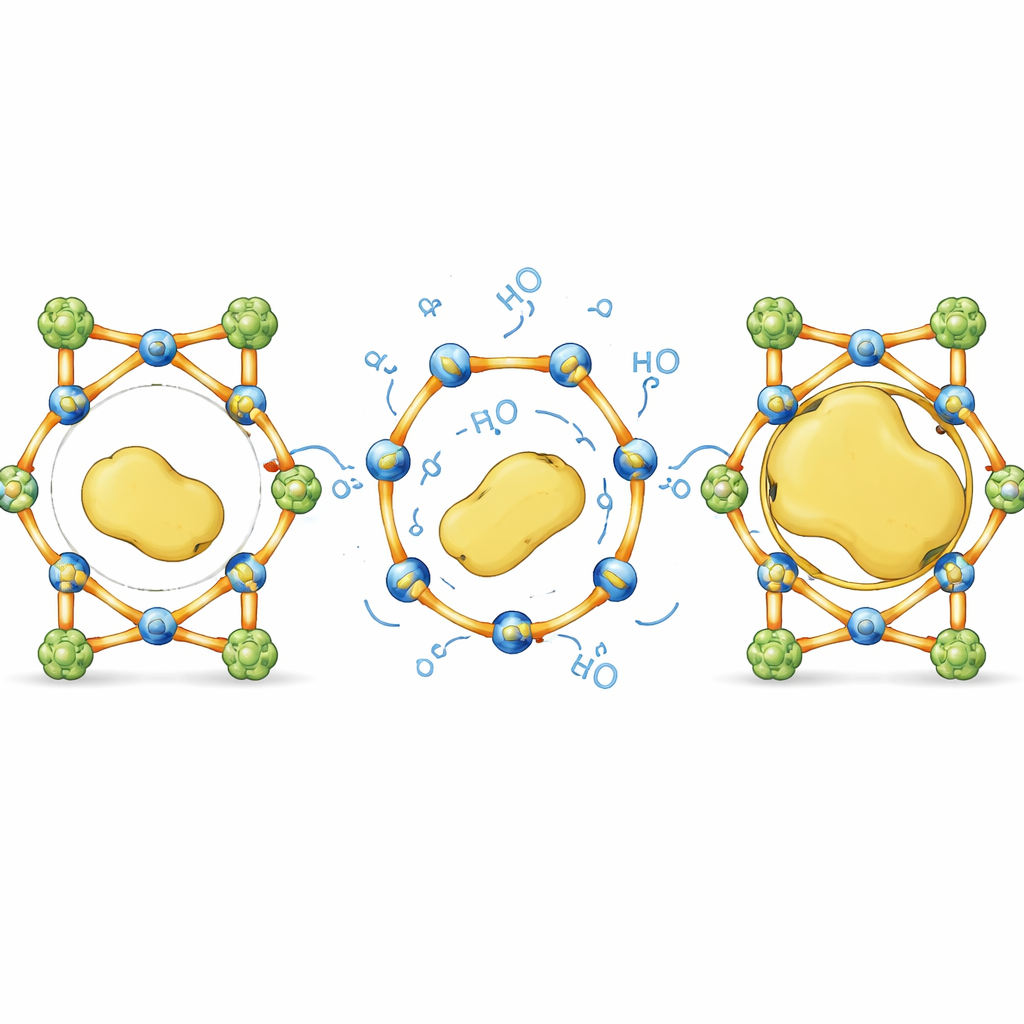
Van groottebeperkingen naar grootte‑onafhankelijk ontwerp
In alledaagse bewoordingen verandert dit werk een stug spons met vaste gaten in een slimme kooi waarvan de spijlen net genoeg kunnen meebuigen om grote gasten binnen te laten en daarna terug te veren. Door onbreekbare steunen zorgvuldig te balanceren met selectief omkeerbare schakels laten de auteurs zien dat het mogelijk is volumineuze, kwetsbare enzymen in kristallijne materialen te proppen die ze normaal zouden uitsluiten, zonder in te leveren op structuur of functie. Deze door dynamische bindingen gedreven aanpak biedt een algemeen recept voor het ontwerpen van grootte‑onafhankelijke “enzymhotels,” met potentieel om industriële biokatalysatoren te verbeteren, meerstapsyntheses te stroomlijnen en duurzamere bio‑gebaseerde technologieën te creëren.
Bronvermelding: Li, Y., Qiao, M., Gao, L. et al. Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints. Nat Commun 17, 3642 (2026). https://doi.org/10.1038/s41467-026-70249-x
Trefwoorden: enzymimmobilisatie, metaal‑organische raamwerken, biokatalyse, dynamische coördinatiebindingen, multi‑enzym cascades