Clear Sky Science · pl
Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints
Dlaczego warto uwięzić delikatnych pomocników
Enzymy to drobne robotniki natury, przyspieszające reakcje chemiczne napędzające wszystko, od komórek żywych po procesy przemysłowe. Jednak poza ich naturalnym środowiskiem te wrażliwe białka szybko ulegają rozkładowi, co utrudnia ich wielokrotne wykorzystanie na skalę przemysłową. W tym artykule opisano metodę bezpiecznego umieszczania enzymów we wnętrzu porowatego kryształu, dzięki czemu dłużej zachowują aktywność i można je wielokrotnie regenerować. Co istotne, zespół pokazuje, jak wprowadzić enzymy większe niż otwory materiału, omijając od dawna istniejące ograniczenie rozmiaru, które blokowało wiele obiecujących zastosowań w zielonej chemii i medycynie.
Budowanie ochronnego kryształowego domu
Naukowcy pracują z metalowo‑organicznymi rusztowaniami, zwanymi MOF‑ami — ciałami stałymi z klastrów metali połączonych organicznymi „wspornikami” w uporządkowaną sieć pełną pustych przestrzeni. MOF‑y są atrakcyjnymi domami dla enzymów, ponieważ oferują dużą powierzchnię wewnętrzną i ochronne klatki, które mogą osłaniać białka przed temperaturą, rozpuszczalnikami i ostrymi warunkami. Problem polega na tym, że wiele użytecznych enzymów jest po prostu za dużych, by przecisnąć się przez wąskie okna większości MOF‑ów. Wcześniejsze rozwiązania albo mocowano enzymy na zewnętrznej powierzchni, co ograniczało ładunek, albo próbowano wzrostu MOF‑u wokół enzymów w bardzo łagodnych warunkach, co działa tylko dla niewielkiego podzbioru chemii MOF‑ów.
Dodanie maleńkich wrót, które otwierają się i goją
Aby uwolnić się od ograniczenia rozmiaru, autorzy zaprojektowali rodzinę MOF‑ów, których wewnętrzne połączenia mogą chwilowo się rozłączać i ponownie łączyć niczym samonaprawiające się szwy. Połączyli bardzo stabilne klastry metal‑karboksylanowe, działające jako sztywne rusztowanie, z bardziej elastycznymi wiązaniami metal‑pirydylowymi, które zachowują się jak odwracalne „wrota”. Poprzez dobór różnych metali i zmianę długości organicznych łączników mogli precyzyjnie regulować, jak łatwo te wróta otwierają się w wodzie, nie powodując rozpadnięcia całej struktury. Pomiary wymywania metali, dyfrakcja rentgenowska i symulacje komputerowe wskazywały na ten sam obraz: w wodzie tylko „miększe” połączenia przy określonych centrach metalicznych się poluzowują, podczas gdy mocniejsze rusztowanie pozostaje nietknięte, zachowując ogólną strukturę kryształu.
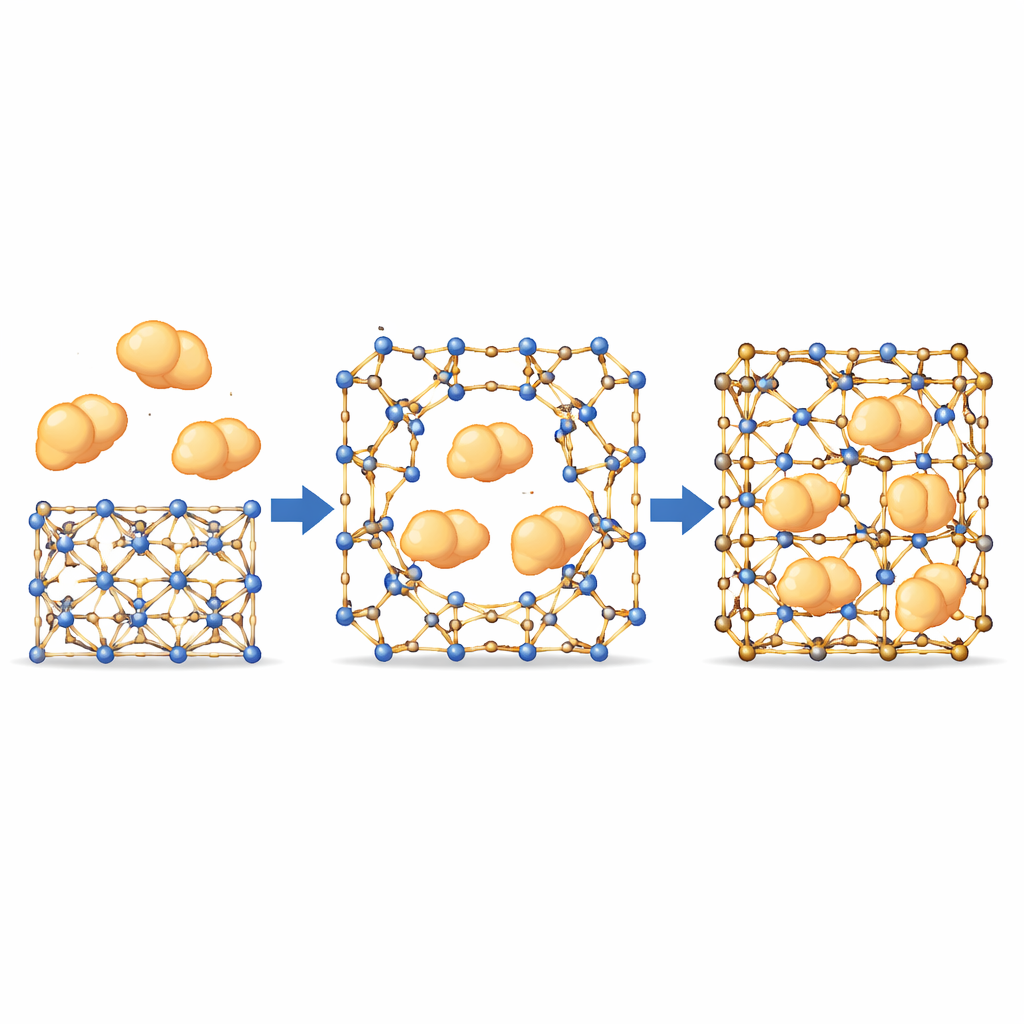
Pozwalanie dużym enzymom przecisnąć się przez małe pory
Dysponując takim zachowaniem przypominającym wrótka, zespół sprawdził, czy duże enzymy — większe niż nominalne pory MOF‑u — mogą jednak zostać wciągnięte do wnętrza. Korzystając z fluorescencyjnie znakowanych białek i mikroskopii konfokalnej, obserwowali enzymy przemieszczające się równomiernie od powierzchni kryształu ku wnętrzu, podążając ścieżkami niepasującymi do stałych wewnętrznych kanałów. To sugeruje, że tworzą się tymczasowe otwory tam, gdzie dynamiczne wiązania chwilowo się rozdzielają, pozwalając enzymom wniknąć, zanim ramka „zasklepi się” wokół nich. Co ważne, bardziej sztywne odmiany materiału, w których te wiązania prawie się nie poruszają, wykazywały niemal brak pobierania enzymów, co potwierdza, że ruch w tych miejscach jest niezbędny. W badanej grupie enzymów o różnych rozmiarach i właściwościach najstaranniej wyważone MOF‑y osiągały wysokie załadowanie przy zachowaniu porządku krystalicznego.
Mocniejsze, dłużej działające katalizatory
Po umieszczeniu wewnątrz enzymy zachowywały się jak trwałe, wielokrotnego użytku katalizatory. Autorzy zbadali kilka reprezentatywnych białek, w tym takie, które są szczególnie wrażliwe na temperaturę, warunki zasadowe i rozpuszczalniki organiczne. W porównaniu z tymi samymi enzymami w roztworze, wersje enkapsulowane znacznie dłużej utrzymywały aktywność pod obciążeniem i mogły być wielokrotnie wykorzystywane w kolejnych przebiegach reakcji przy niewielkiej utracie wydajności. Dynamiczne MOF‑y umożliwiły także wspólną enkapsulację dwóch współpracujących enzymów przeprowadzających kolejne etapy tworzenia cennego cukrowego bloku budulcowego. Umieszczenie obu w tym samym rusztowaniu skróciło dystans między nimi, zwiększając wydajność reakcji i pozwalając systemowi działać powtarzalnie z utrzymanym wydatkiem.
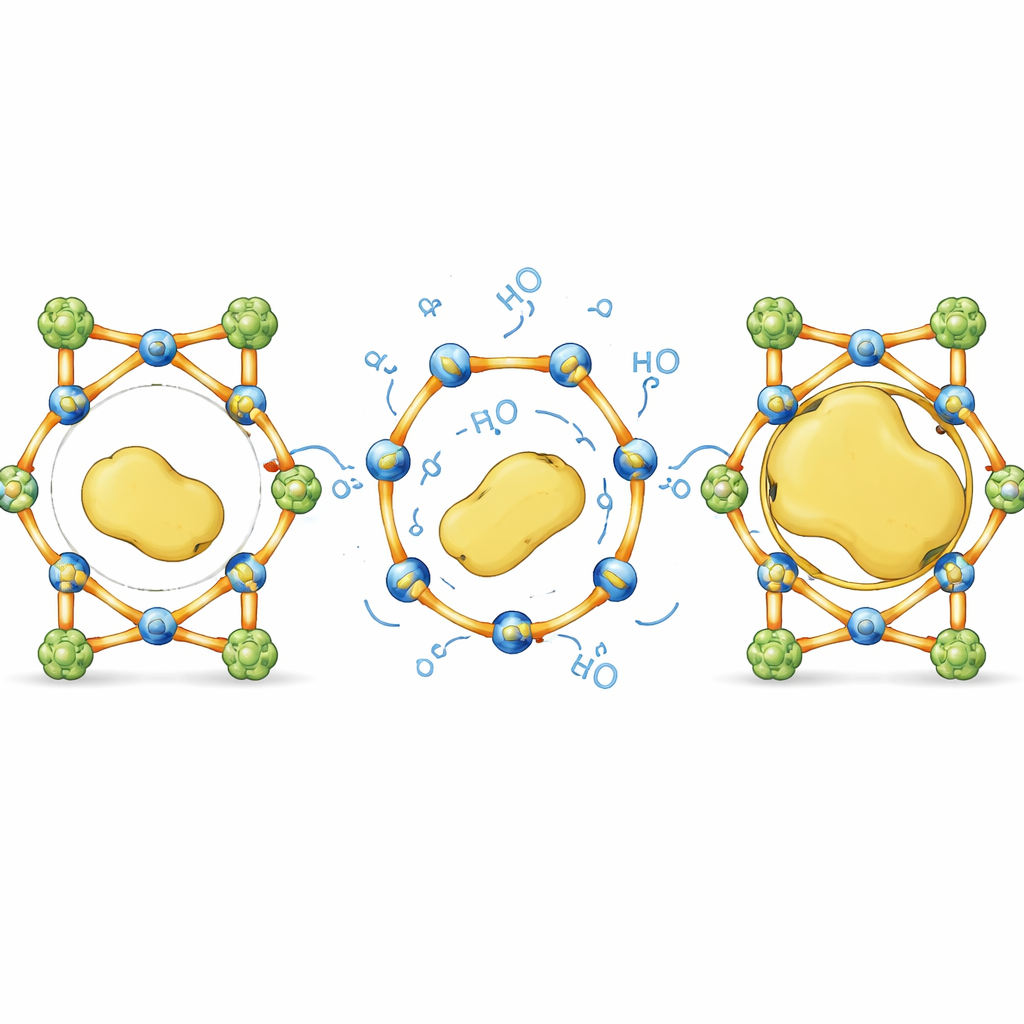
Od ograniczeń rozmiaru do projektu niewrażliwego na rozmiar
W codziennym ujęciu ta praca zamienia sztywną gąbkę o stałych otworach w inteligentną klatkę, której pręty mogą się zgiąć wystarczająco, by wpuścić dużych gości, a potem zatrzasnąć z powrotem. Poprzez staranne wyważenie niełamliwych podpór z selektywnie odwracalnymi łącznikami autorzy pokazują, że możliwe jest upakowanie masywnych, wrażliwych enzymów w kryształowe materiały, które normalnie by ich wykluczyły, bez poświęcania struktury ani funkcji. To podejście oparte na dynamicznych wiązaniach daje ogólną receptę na projektowanie „hoteli dla enzymów” niewrażliwych na rozmiar, z potencjałem poprawy katalizatorów przemysłowych, usprawnienia wieloetapowych syntez i stworzenia trwalszych technologii opartych na biotechnologii.
Cytowanie: Li, Y., Qiao, M., Gao, L. et al. Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints. Nat Commun 17, 3642 (2026). https://doi.org/10.1038/s41467-026-70249-x
Słowa kluczowe: immobilizacja enzymów, metalowo-organiczne rusztowania, biokataliza, dynamiczne wiązania koordynacyjne, kaskady wieloenzymatyczne