Clear Sky Science · sv
Dynamisk bindningsstyrd inkapsling av enzymer i metall–organiska ramverk bortom porstorleksbegränsningar
Varför det spelar roll att fånga in sköra hjälpare
Enzymer är naturens små arbetsmyror, de snabbar upp kemiska reaktioner som driver allt från levande celler till industriell tillverkning. Men utanför sina naturliga miljöer bryts dessa känsliga proteiner snabbt ner, vilket gör dem svåra att återanvända i större skala. Den här artikeln beskriver ett sätt att trygga enzymer inuti ett poröst kristallint material så att de förblir aktiva längre och kan återcirkuleras flera gånger. Avgörande visar teamet hur man kan skjuta in enzymer som faktiskt är större än materialets inbyggda öppningar och därmed kringgå en långvarig storleksgräns som har hindrat många lovande tillämpningar inom grön kemi och medicin.
Bygga ett skyddande kristallhus
Forskarna arbetar med metall–organiska ramverk, eller MOF:er—material uppbyggda av metallkluster kopplade med organiska ”stänger” till ett ordnat skelett fullt av tomrum. MOF:er är attraktiva hem för enzymer eftersom de erbjuder stora interna ytor och skyddande kaviteter som kan skydda proteiner från värme, lösningsmedel och hårda förhållanden. Problemet är att många användbara enzymer helt enkelt är för stora för att pressas genom de smala fönstren i de flesta MOF:er. Tidigare lösningar fäste antingen enzymerna på utsidan, vilket begränsade hur mycket som kunde lastas, eller försökte odla MOF:en runt enzymerna under mycket försiktiga förhållanden, vilket bara fungerar för en liten del av MOF-kemierna.
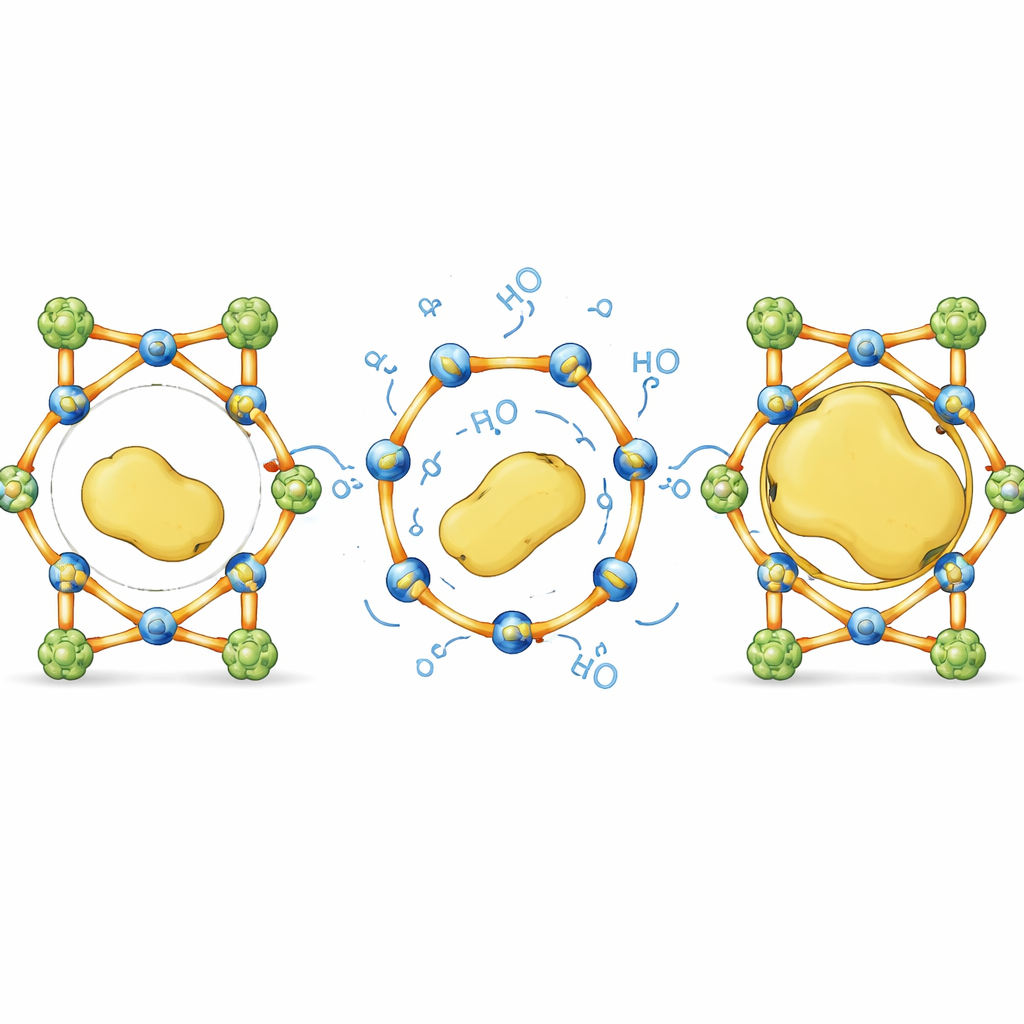
Lägga till små portar som öppnas och läker
För att ta sig ur den här storleksfällan designade författarna en familj av MOF:er vars interna förbindelser kortvarigt kan haka loss och återfästa som självläkande stygn. De kombinerade mycket stabila metall–karboxylatkluster, som fungerar som en styv ryggrad, med mer flexibla metall–pyridyl-länkar som beter sig som reversibla ”grindar”. Genom att byta olika metaller och ändra längden på de organiska länkarna kunde de finjustera hur lätt dessa grindar öppnas i vatten utan att hela strukturen kollapsar. Mätningar av metallutlakning, röntgendiffraktion och datorsimuleringar pekade alla mot samma bild: i vatten lossnar endast de mjukare förbindelserna vid specifika metalplatser, medan den hårdare ryggraden förblir intakt och bevarar det övergripande kristallramverket.
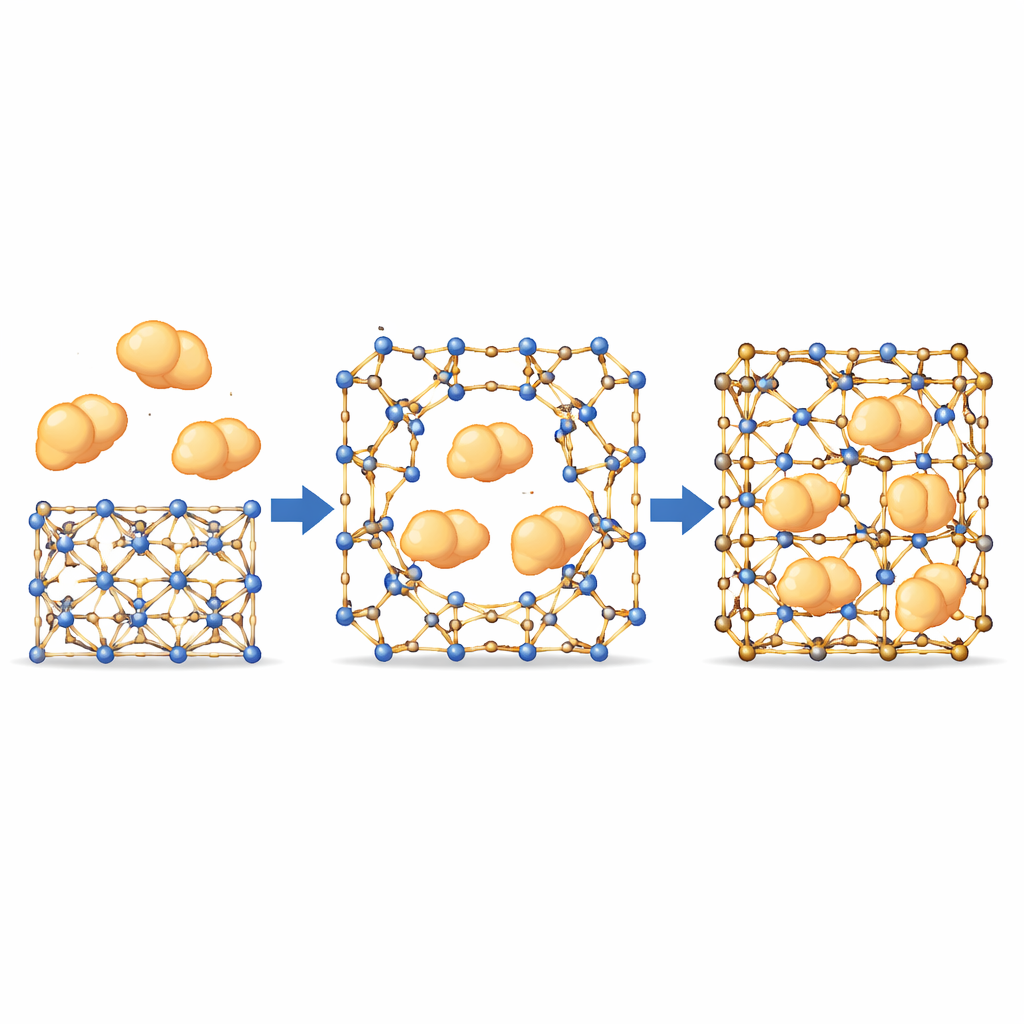
Att låta stora enzymer glida genom små porer
Med detta grindliknande beteende undersökte teamet om stora enzymer—större än MOF:ens nominella porer—ändå kunde dras in. Med fluorescerande märkta proteiner och konfokalmikroskopi följde de enzymernas enhetliga rörelse från kristallytan mot insidan, efter vägar som inte stämde överens med de fasta interna kanalerna. Detta tyder på att temporära öppningar bildas där dynamiska bindningar kortvarigt separerar, vilket tillåter enzymerna att tränga in innan ramverket ”läker” runt dem. Viktigt är att starkare varianter av materialet, där dessa bindningar knappt rör sig, visade nästan ingen enzymupptagning, vilket bekräftar att rörelse vid dessa platser är nödvändig. Över en panel av enzymer med olika storlekar och egenskaper uppnådde de mest finbalanserade MOF:arna hög lastning samtidigt som de behöll sin kristallordning.
Kraftigare, mer långlivade katalysatorer
När de väl var inne fungerade enzymerna som robusta, återanvändbara katalysatorer. Författarna undersökte flera representativa proteiner, inklusive sådana som är notoriskt känsliga för värme, basiska förhållanden och organiska lösningsmedel. Jämfört med samma enzymer fria i lösning behöll de inkapslade varianterna en mycket större del av sin aktivitet under påfrestning och kunde köras genom flera reaktionscykler med liten prestationsförlust. De dynamiska MOF:arna möjliggjorde också sam-inkapsling av två samarbetande enzymer som arbetar i sekvens för att göra en värdefull sockerbasserad byggsten. Att hysa båda i samma ramverk förkortade avståndet mellan dem, ökade reaktionseffektiviteten och gjorde det möjligt för systemet att köras upprepade gånger med bibehållen produktivitet.
Från storleksgränser till storleksblind design
I vardagliga termer förvandlar detta arbete en styv svamp med fasta hål till en smart bur vars ribbor kan flexa precis tillräckligt för att släppa in stora gäster och sedan slå tillbaka på plats. Genom att noga balansera obrutna stöder med selektivt reversibla länkar visar författarna att det är möjligt att packa skrymmande, sköra enzymer i kristallina material som normalt skulle exkludera dem, utan att offra struktur eller funktion. Detta dynamiska, bindningsdrivna tillvägagångssätt erbjuder ett generellt recept för att utforma storleksoberoende ”enzymhotell”, med potential att förbättra industriella biokatalysatorer, effektivisera flerstegs-synteser och skapa mer hållbara biobaserade teknologier.
Citering: Li, Y., Qiao, M., Gao, L. et al. Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints. Nat Commun 17, 3642 (2026). https://doi.org/10.1038/s41467-026-70249-x
Nyckelord: enzymimmobilisering, metall-organiska ramverk, biokatalys, dynamiska koordinationsbindningar, flerenzymkaskader