Clear Sky Science · es
Encapsulación de enzimas impulsada por enlaces dinámicos en marcos metal‑orgánicos más allá de las limitaciones del tamaño de poro
Por qué importa atrapar a estos auxiliares frágiles
Las enzimas son los pequeños caballos de batalla de la naturaleza, acelerando reacciones químicas que sustentan desde las células vivas hasta la fabricación industrial. Pero fuera de sus entornos naturales, estas proteínas delicadas se desestabilizan con rapidez, lo que dificulta su reutilización a escala. Este artículo describe una manera de alojar enzimas de forma segura dentro de un material cristalino poroso, de modo que conserven su actividad durante más tiempo y puedan reciclarse repetidamente. De forma crucial, el equipo muestra cómo introducir enzimas que en realidad son mayores que las aberturas integradas del material, eludiendo un límite de tamaño de larga data que había frenado muchas aplicaciones prometedoras en química sostenible y medicina.
Construir una casa cristalina protectora
Los investigadores trabajan con marcos metal‑orgánicos, o MOF—sólidos formados por racimos metálicos unidos por “vigas” orgánicas en un armazón ordenado lleno de espacios vacíos. Los MOF son alojamientos atractivos para enzimas porque ofrecen grandes áreas superficiales internas y jaulas protectoras que pueden resguardar las proteínas del calor, los disolventes y condiciones agresivas. El problema es que muchas enzimas útiles son simplemente demasiado grandes para pasar por las ventanas estrechas de la mayoría de los MOF. Soluciones anteriores o bien fijaban las enzimas en la superficie exterior, lo que limitaba la carga posible, o intentaban hacer crecer el MOF alrededor de las enzimas en condiciones muy suaves, lo que solo funciona para un subconjunto reducido de quimias de MOF.
Añadir pequeñas compuertas que se abren y se reparan
Para escapar de esta trampa de tamaño, los autores diseñaron una familia de MOF cuyas conexiones internas pueden desprenderse y volver a unirse brevemente, como puntadas autorreparables. Combinan racimos metal‑carboxilato muy estables, que actúan como una espina dorsal rígida, con enlaces metal‑piridilo más flexibles que se comportan como “compuertas” reversibles. Al intercambiar distintos metales y variar la longitud de los enlaces orgánicos, pudieron afinar con precisión cuán fácilmente se abren estas compuertas en agua sin que la estructura global se venga abajo. Medidas de pérdida de metal, difracción de rayos X y simulaciones por ordenador apuntaron al mismo panorama: en agua, sólo las conexiones más blandas en sitios metálicos específicos se aflojan, mientras que la columna vertebral más resistente permanece intacta, preservando el armazón cristalino en su conjunto.
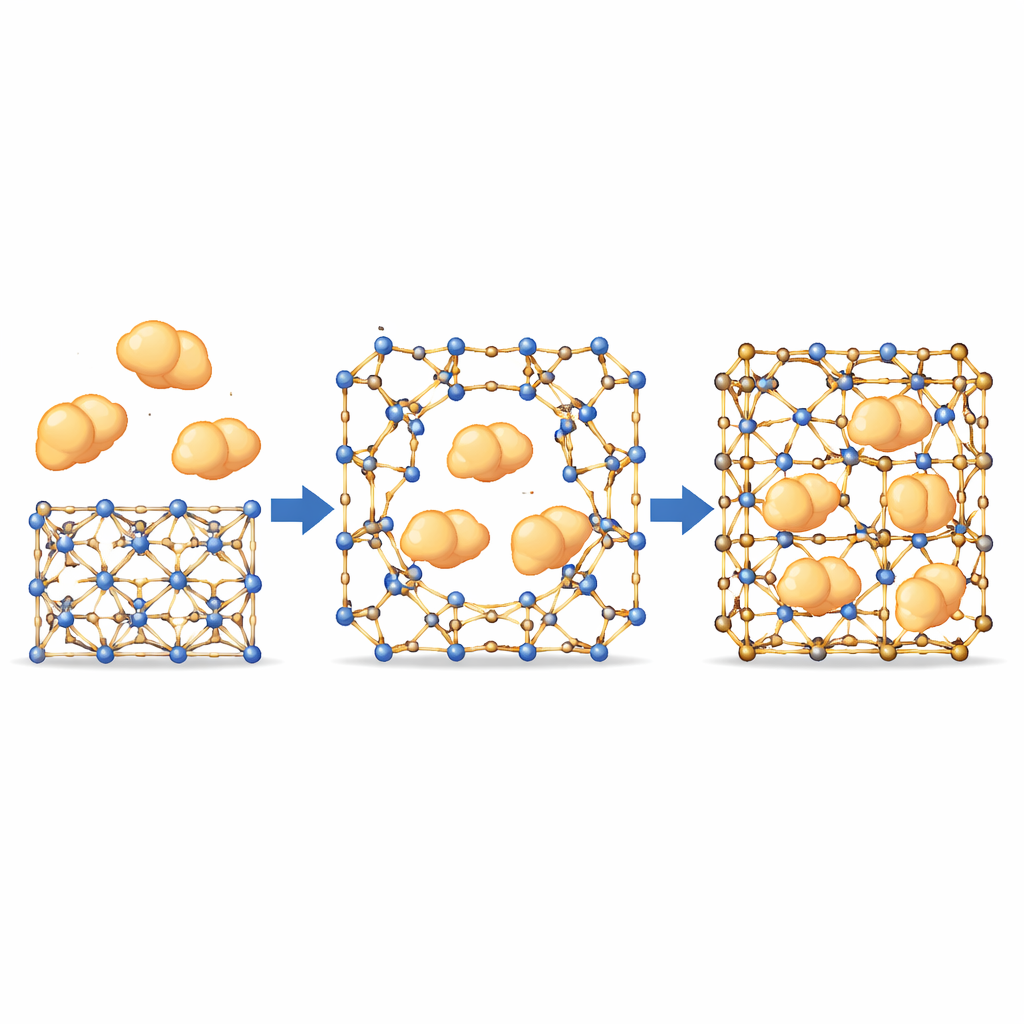
Permitir que enzimas grandes pasen por poros pequeños
Con este comportamiento tipo compuerta a su alcance, el equipo probó si enzimas voluminosas—más grandes que los poros nominales del MOF—podían aun así introducirse. Usando proteínas marcadas fluorescentemente y microscopía confocal, observaron a las enzimas moverse de forma uniforme desde la superficie del cristal hacia el interior, siguiendo trayectorias que no coincidían con los canales internos fijos. Esto sugiere que se forman aberturas temporales donde los enlaces dinámicos se separan brevemente, permitiendo que las enzimas se infiltren antes de que el armazón se “repare” a su alrededor. Es importante señalar que variantes más rígidas del material, donde estos enlaces apenas se mueven, mostraron casi ninguna incorporación de enzimas, confirmando que el movimiento en estos sitios es esencial. En una batería de enzimas con distintos tamaños y propiedades, los MOF más equilibrados lograron una alta carga mientras mantenían el orden cristalino.
Catalizadores más fuertes y duraderos
Una vez dentro, las enzimas actuaron como catalizadores robustos y reutilizables. Los autores examinaron varias proteínas representativas, incluidas algunas notoriamente sensibles al calor, a condiciones alcalinas y a disolventes orgánicos. En comparación con las mismas enzimas en solución libre, las versiones encapsuladas conservaron gran parte de su actividad cuando se sometieron a estrés y pudieron reciclarse a través de múltiples reacciones con poca pérdida de rendimiento. Los MOF dinámicos también permitieron la coencapsulación de dos enzimas cooperantes que actúan en secuencia para fabricar un bloque de construcción valioso basado en azúcares. Alojar ambas dentro del mismo armazón acortó la distancia entre ellas, aumentando la eficiencia de la reacción y permitiendo que el sistema funcionara repetidamente con una producción sostenida.
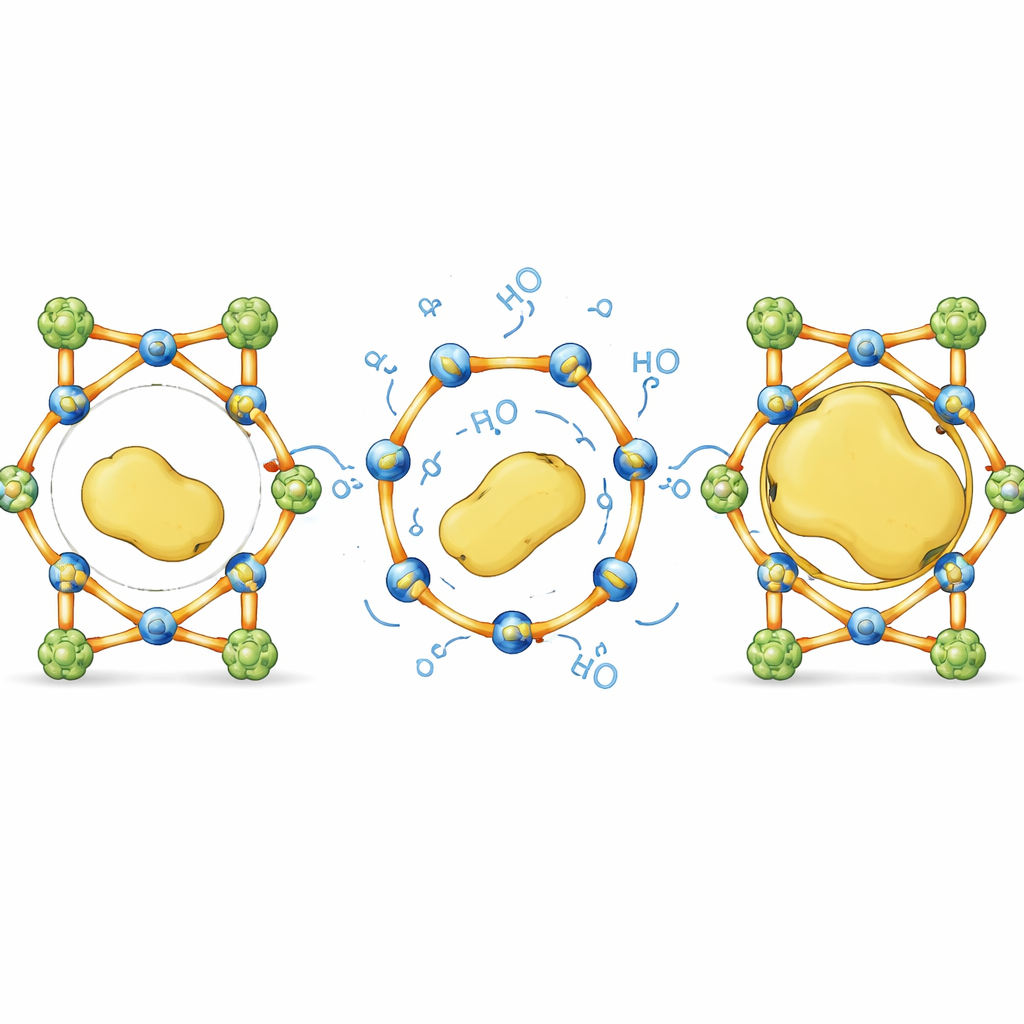
De los límites de tamaño a un diseño ciego al tamaño
En términos cotidianos, este trabajo convierte una esponja rígida con agujeros fijos en una jaula inteligente cuyas barras pueden flexionarse lo justo para admitir huéspedes voluminosos y luego volver a encajar. Al equilibrar cuidadosamente soportes inquebrantables con enlaces selectivamente reversibles, los autores demuestran que es posible alojar enzimas voluminosas y frágiles dentro de materiales cristalinos que normalmente las excluirían, sin sacrificar estructura ni función. Este enfoque impulsado por enlaces dinámicos ofrece una receta general para diseñar “hoteles de enzimas” independientes del tamaño, con potencial para mejorar biocatalizadores industriales, simplificar síntesis multi‑paso y crear tecnologías bio‑basadas más duraderas.
Cita: Li, Y., Qiao, M., Gao, L. et al. Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints. Nat Commun 17, 3642 (2026). https://doi.org/10.1038/s41467-026-70249-x
Palabras clave: inmovilización de enzimas, marcos metal-orgánicos, biocatálisis, enlaces de coordinación dinámicos, cascadas multi-enzimáticas