Clear Sky Science · it
Incapsulamento guidato da legami dinamici di enzimi in metallo‑organici oltre i limiti delle dimensioni dei pori
Perché conviene intrappolare questi fragili aiutanti
Gli enzimi sono i piccoli instancabili della natura, accelerando le reazioni chimiche che alimentano tutto, dalle cellule viventi alla produzione industriale. Ma al di fuori dei loro ambienti naturali queste proteine delicate si degradano rapidamente, rendendo difficile il loro riutilizzo su larga scala. Questo articolo descrive un metodo per alloggiare gli enzimi in modo sicuro all’interno di un materiale cristallino poroso, così che restino attivi più a lungo e possano essere riciclati ripetutamente. Elemento cruciale, il team dimostra come introdurre enzimi che sono in realtà più grandi delle aperture intrinseche del materiale, eludendo un vincolo di dimensione di lunga data che ha frenato molte applicazioni promettenti nella chimica sostenibile e in medicina.
Costruire una casa cristallina protettiva
I ricercatori lavorano con i reticoli metallo‑organici, o MOF—solidi formati da cluster metallici collegati da “travi” organiche in una struttura ordinata piena di spazi vuoti. I MOF sono alloggi attraenti per gli enzimi perché offrono ampie aree superficiali interne e gabbie protettive che possono schermare le proteine da calore, solventi e condizioni aggressive. Il problema è che molti enzimi utili sono semplicemente troppo grandi per passare attraverso le strette finestre della maggior parte dei MOF. Le soluzioni precedenti o fissavano gli enzimi alla superficie esterna, limitando la quantità caricabile, oppure cercavano di far crescere il MOF intorno agli enzimi in condizioni molto miti, valido però solo per un piccolo sottoinsieme di chimie di MOF.
Aggiungere piccoli cancelli che si aprono e si rimarginano
Per sfuggire a questo limite di dimensione, gli autori hanno progettato una famiglia di MOF le cui connessioni interne possono temporaneamente sganciarsi e riattaccarsi come punti auto‑rimarginanti. Hanno combinato cluster metallo‑carboxilato molto stabili, che fungono da spina dorsale rigida, con collegamenti metallo‑piridilici più flessibili che si comportano come “cancelli” reversibili. Variando i metalli e la lunghezza dei leganti organici, hanno potuto regolare finemente quanto facilmente questi cancelli si aprono in acqua senza compromettere l’intera struttura. Misure di perdita di metallo, diffrazione a raggi X e simulazioni al computer hanno fornito tutti lo stesso quadro: in acqua si allentano soltanto le connessioni più morbide in siti metallici specifici, mentre la spina dorsale più resistente resta intatta, preservando il reticolo cristallino nel suo complesso.
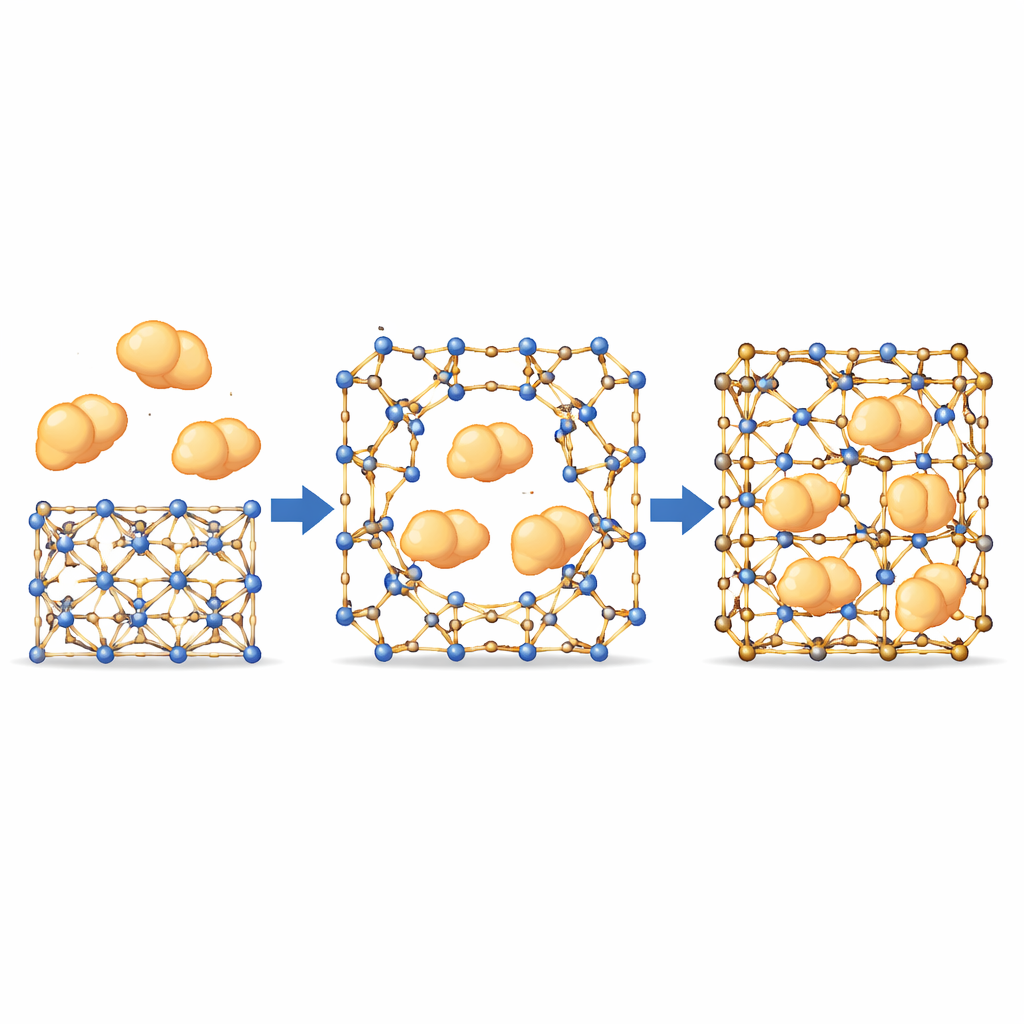
Far passare enzimi grandi attraverso pori piccoli
Con questo comportamento a cancelli a disposizione, il team ha verificato se grandi enzimi—più grandi dei pori nominali del MOF—potessero comunque essere introdotti. Usando proteine etichettate con fluorescenza e microscopia confocale, hanno osservato gli enzimi muoversi in modo uniforme dalla superficie cristallina verso l’interno, seguendo percorsi che non corrispondevano ai canali interni fissi. Questo suggerisce che si formano aperture temporanee dove i legami dinamici si separano brevemente, permettendo agli enzimi di infiltrarsi prima che il reticolo si “rimargini” attorno a loro. Importante, varianti più robuste del materiale, dove questi legami si muovono appena, hanno mostrato quasi nessun assorbimento di enzima, confermando che il movimento in questi siti è essenziale. Su un pannello di enzimi con dimensioni e proprietà diverse, i MOF più finemente bilanciati hanno raggiunto un alto carico mantenendo comunque l’ordine cristallino.
Catalizzatori più forti e duraturi
Una volta alloggiati, gli enzimi si sono comportati come catalizzatori robusti e riutilizzabili. Gli autori hanno esaminato diverse proteine rappresentative, incluse quelle notoriamente sensibili a calore, condizioni alcaline e solventi organici. Rispetto agli stessi enzimi liberi in soluzione, le versioni incapsulate hanno mantenuto molta più attività sotto stress e potevano essere sottoposte a più cicli di reazione con poca perdita di prestazione. I MOF dinamici hanno anche permesso la co‑incapsulazione di due enzimi cooperanti che operano in sequenza per produrre un prezioso blocco costruttivo a base di zucchero. Ospitarli entrambi nello stesso reticolo ha accorciato il percorso tra di loro, aumentando l’efficienza della reazione e permettendo al sistema di funzionare ripetutamente con output sostenuto.
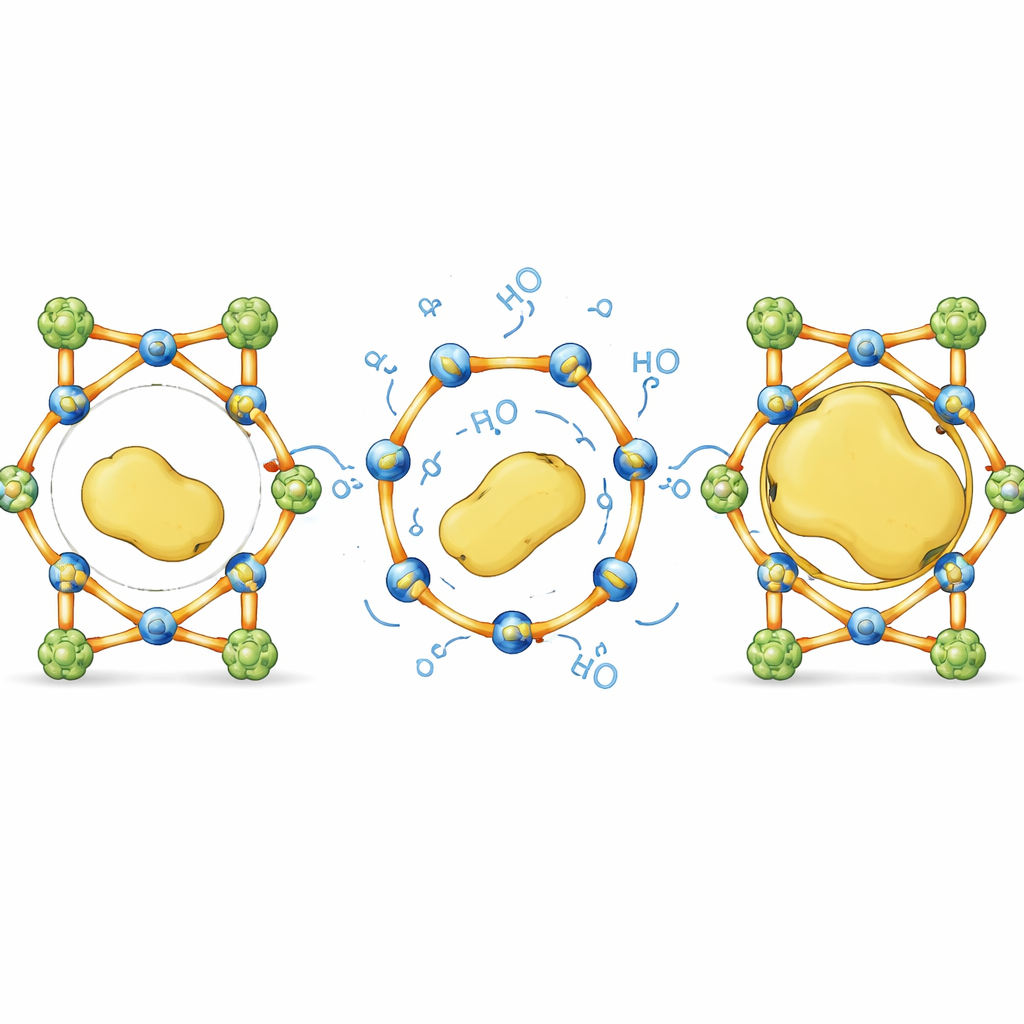
Da limiti di dimensione a progettazione indipendente dalla taglia
In termini quotidiani, questo lavoro trasforma una spugna rigida con fori fissi in una gabbia intelligente i cui sbarre possono flettersi giusto quel tanto che basta per far entrare ospiti grandi e poi tornare al loro posto. Bilanciando con cura supporti indistruttibili con legami reversibili selettivi, gli autori dimostrano che è possibile inserire enzimi ingombranti e fragili all’interno di materiali cristallini che normalmente li escluderebbero, senza sacrificare struttura o funzione. Questo approccio guidato da legami dinamici offre una ricetta generale per progettare “hotel per enzimi” indipendenti dalla taglia, con il potenziale di migliorare i biocatalizzatori industriali, snellire sintesi multi‑step e creare tecnologie bio‑based più durature.
Citazione: Li, Y., Qiao, M., Gao, L. et al. Dynamic bond-driven encapsulation of enzymes in metal–organic frameworks beyond pore size constraints. Nat Commun 17, 3642 (2026). https://doi.org/10.1038/s41467-026-70249-x
Parole chiave: immobilizzazione degli enzimi, reticoli metallo‑organici, biocatalisi, legami di coordinazione dinamici, cascate multi‑enzimatiche