Clear Sky Science · zh
空间转录组学揭示以血管为中心的细胞相互作用驱动小鼠模型中日本脑炎进展
这项脑部感染研究为何重要
日本脑炎是一种由蚊子传播的脑部感染,幸存者常终身残留运动和记忆障碍,儿童尤其脆弱。然而,临床上仍缺乏直接针对病毒或其在脑内引发的有害炎症的药物。本研究使用一种强大的定位描绘技术,几乎以细胞为单位追踪病毒和机体免疫细胞在小鼠大脑中的移动。由此揭示出血管与巡游免疫细胞之间一种出人意料的协同关系,有助于解释疾病为何变得如此具破坏性。
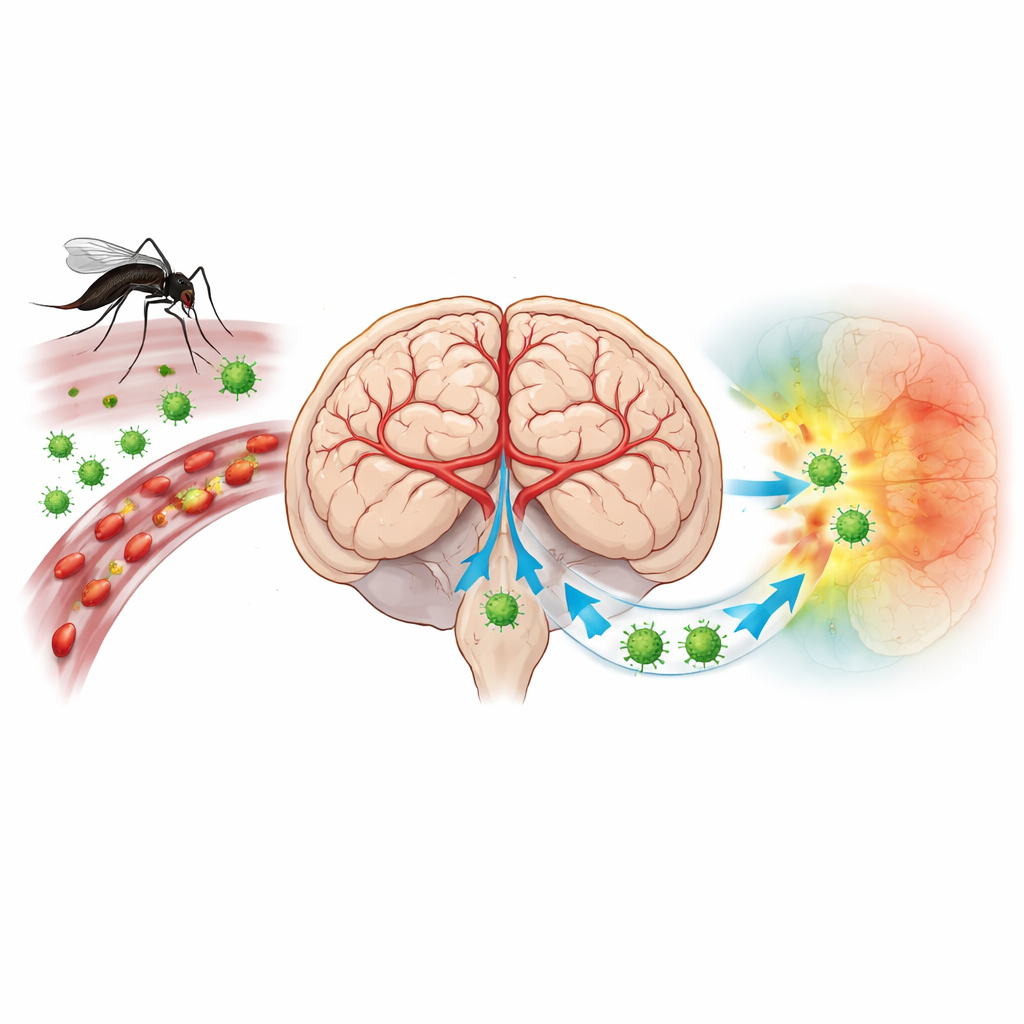
将脑部防御体系转为自我伤害的病毒
日本脑炎病毒(JEV)由蚊子传播,威胁着亚洲和西太平洋地区超过三十亿人口。大多数感染无症状,但当病毒进入大脑时可引起高热、癫痫发作和昏迷。疫苗可降低风险,但仍有大量人群未受保护,且不存在特异性抗病毒治疗。长期以来,科学家怀疑免疫细胞进入大脑的方式以及它们与脑血管的相互作用是疾病发展的关键。然而,传统方法难以清晰显示到底哪些精确细胞被感染以及它们在脆弱的大脑结构中如何排列。
时空分辨的分子感染图谱
研究人员用JEV感染雌性小鼠,并在感染后第3、5和7天取出大脑进行检查,覆盖了病毒水平上升和严重症状出现的阶段。他们使用一种称为空间转录组学的技术,可在一片薄脑切片上成千上万个微小点位读取基因表达,并保留每个点在组织中的空间位置。定制探针使他们能在同一载玻片上同时检测到小鼠和病毒的RNA。通过将这些地图与脑图谱和细胞类型参考结合,他们构建了一个时空图谱:病毒偏好的脑区、被感染的细胞类型以及局部免疫反应如何展开。
血管:通道与放大器
图谱显示JEV最初出现在小部分脑组织中,随后扩展并大量累及丘脑和大脑皮层。更为显著的是最强烈免疫信号出现的位置:沿血管分布,尤其是在包裹大脑的薄膜(脑膜)和负责产生脑脊液的脉络丛处。在这些部位,一类以受体Ackr1为标记的特殊内皮细胞高度激活。此类细胞产生大量趋化因子,吸引免疫细胞,并启动与炎症相关的基因表达,同时下调维持紧密连接的基因——这些紧密连接是保持血脑屏障完整性的“密封”。同期,使用染料的检测证实屏障确实变得通透。
单核细胞:特洛伊木马与信号放大器
在所有进入大脑的免疫细胞中,有一类脱颖而出:Ly6c2阳性的单核细胞。空间图谱和流式细胞术显示这些细胞常被JEV感染,使其成为可能将病毒从受损血管带入脑内的“载体”——类似特洛伊木马的作用。它们不仅运输病毒,还大量产生干扰素-γ,这是一种通常与T细胞和自然杀伤细胞相关的强效免疫信使。干扰素-γ既有助于清除病毒,也会加剧血脑屏障的损伤。研究发现,这些单核细胞聚集在Ackr1阳性的内皮细胞附近,并通过多种趋化因子与之通讯,形成一个吸引更多免疫细胞的反馈回路。在这些血管周围,许多细胞——包括单核细胞自身——表现出爆炸性细胞死亡(焦亡和程序性坏死)的分子特征,将炎性内容物释放到周围组织中。
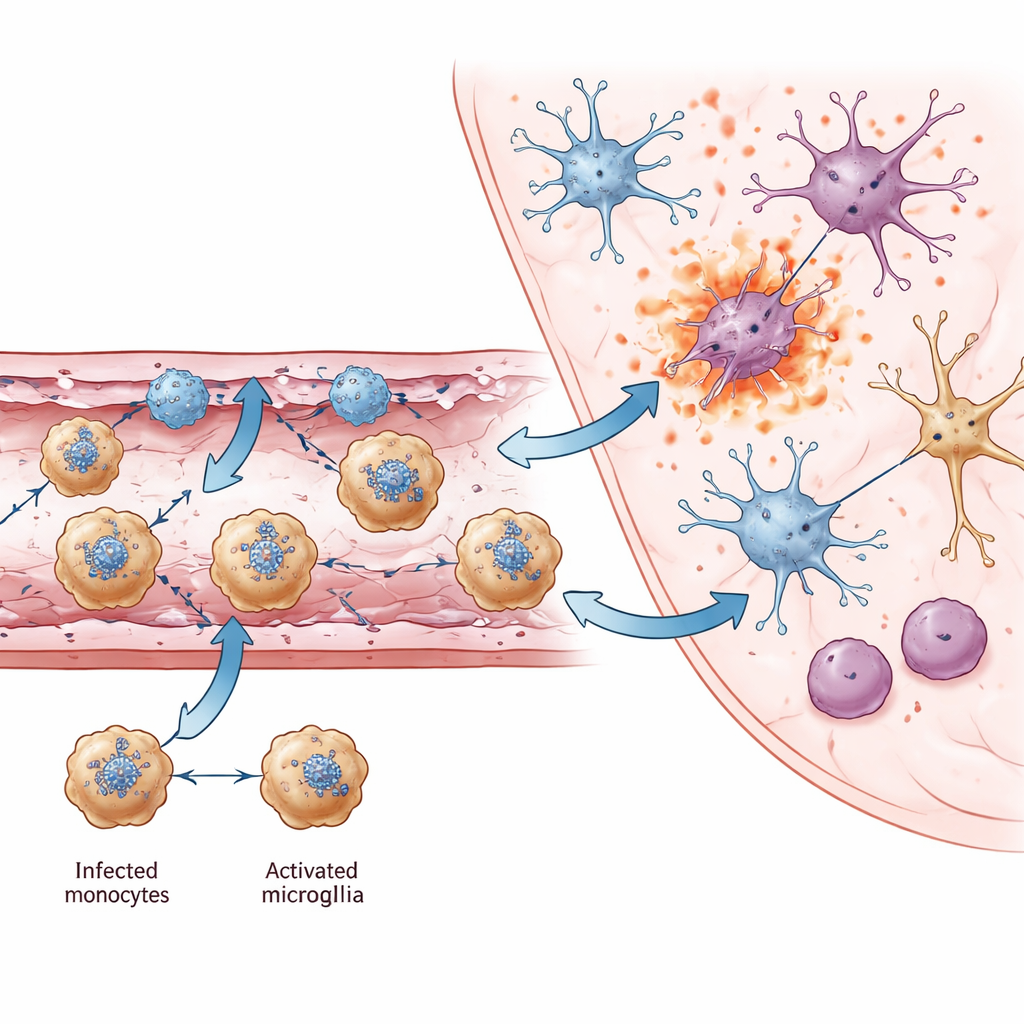
从局部血管损伤到广泛脑损害
随着感染进展,脑内常驻细胞也发生变化。小胶质细胞作为脑内先天免疫哨兵,转为一种以趋化因子Ccl12和强烈抗病毒基因活动为特征的激活状态。尽管这些变化有助于对抗病毒,但它们也伴随与突触、学习和记忆相关基因的丧失。在丘脑等严重感染区域,检测到病毒RNA的不同神经元亚型显示出升高的焦亡和程序性坏死信号,表明炎性细胞死亡是神经元丧失的关键原因。跨多个脑区,作者识别出一些神经元共同基因,其活性下降也与其他脑疾患中的认知和运动问题相关,提示幸存者长期残疾可能有共同的分子基础。
对未来治疗的启示
对普通读者而言,核心信息是日本脑炎不仅仅是病毒攻击神经元的故事。它也是被感染的单核细胞与特化的血管细胞在脑边界处形成有害联盟的故事。它们共同松动血脑屏障,吸引成批免疫细胞,并触发从血管向脑组织扩散的炎性细胞死亡。通过定位这些关键参与者——Ly6c2阳性的单核细胞和Ackr1阳性的内皮细胞——该研究提出了新的治疗方向:抑制特定趋化因子、阻断Ackr1受体或限制单核细胞募集和焦亡的药物,可能在保留抗病毒防御的同时减轻最严重的脑损伤。
引用: Ou, Z., Wang, Z., Chen, Q. et al. Spatial transcriptomics uncovers vasculature-centered cellular interactions driving Japanese encephalitis progression in a mouse model. Nat Commun 17, 4089 (2026). https://doi.org/10.1038/s41467-026-70047-5
关键词: 日本脑炎, 脑炎症, 血脑屏障, 单核细胞, 空间转录组学