Clear Sky Science · ru
Пространственная транскриптомика выявляет сосудо-центричные клеточные взаимодействия, приводящие к прогрессированию японского энцефалита в модели на мышах
Почему это исследование мозговой инфекции важно
Японский энцефалит — переносимая комарами инфекция мозга, которая может оставить у выживших пожизненные нарушения двигательной и памяти, особенно у детей. Тем не менее у врачей по‑прежнему нет препаратов, направленных непосредственно против вируса или против разрушительного воспаления, которое он вызывает в мозге. В этом исследовании использована мощная технология картирования, позволяющая проследить почти по клетке, как вирус и собственные иммунные клетки организма перемещаются по мозгу мыши. Это раскрывает неожиданное сотрудничество между кровеносными сосудами и мигрирующими иммунными клетками, что помогает понять, почему болезнь становится столь разрушительной.
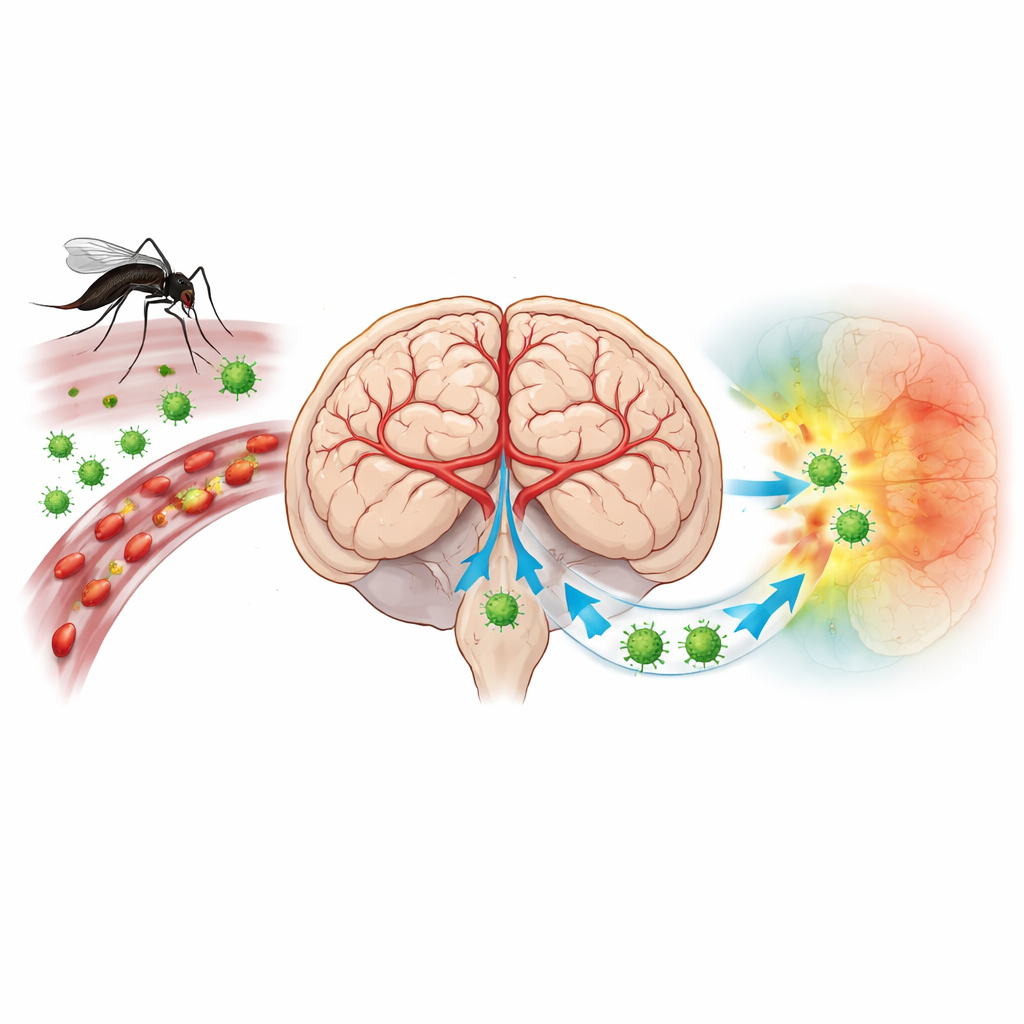
Вирус, который обращает защиту мозга против него самого
Вирус японского энцефалита (JEV) переносится комарами и угрожает более чем трем миллиардам людей в Азии и Западной части Тихого океана. Большинство инфекций протекают бессимптомно, но когда вирус проникает в мозг, он может вызвать высокую температуру, судороги и кому. Вакцинация снижает риск, но многие остаются незащищёнными, и специфического противовирусного лечения нет. Учёные давно предполагали, что ключевую роль в болезни играет проникновение иммунных клеток в мозг и их взаимодействие с сосудистой системой мозга. Однако традиционные методы затрудняли точное определение, какие именно клетки инфицированы и как они расположены в хрупкой архитектуре мозга.
Молекулярная карта инфекции в пространстве и времени
Исследователи инфицировали самок мышей JEV и исследовали их мозги на 3-й, 5-й и 7-й дни после инфекции, охватив период роста вирусной нагрузки и появления тяжёлых симптомов. Они использовали технологию пространственной транскриптомики, которая фиксирует, какие гены активны в тысячах крошечных точек по тонкому срезу мозга, при этом сохраняя информацию о пространственном расположении каждой точки в ткани. Пользовательские зонды позволили одновременно обнаруживать мышиную и вирусную РНК на одном слайде. Сохранив карты вместе с атласами мозга и справочниками по типам клеток, они построили пространственно-временной атлас: какие области мозга предпочитает вирус, какие типы клеток он инфицирует и как разворачиваются локальные иммунные ответы.
Кровеносные сосуды как ворота и усилители
Атлас показал, что JEV сначала появляется в небольшой части ткани мозга, затем расширяется, сильно вовлекая таламус и кору головного мозга. Ещё более заметным было местоположение самых сильных иммунных сигналов: вдоль кровеносных сосудов, особенно в тонких оболочках (менингах), которые покрывают мозг, и в сосудистой сплетении — ткани, участвующей в образовании спинномозговой жидкости. Здесь особый подтип эндотелиальных клеток — клеток, выстилающих сосуды, помеченных рецептором Ackr1 — оказался сильно активирован. Эти клетки продуцировали множество хемокинов, молекул, привлекающих иммунные клетки, включали гены, связанные с воспалением, и ослабляли экспрессию генов, отвечающих за плотные контакты, которые сохраняют целостность гематоэнцефалического барьера. Одновременно тесты с красителем подтвердили, что барьер действительно стал проницаемым.
Моноциты: троянские кони и усилители сигналов
Среди всех иммунных клеток, проникающих в мозг, выделялась одна популяция: моноциты, положительные по маркеру Ly6c2. Пространственные карты и проточная цитометрия показали, что эти клетки часто инфицированы JEV, что делает их вероятными переносчиками, перевозящими вирус через повреждённые сосуды в мозг — по принципу троянского коня. Они выполняли не только транспортную роль. Эти моноциты продуцировали большие количества интерферона‑гамма, мощного иммунного сигнала, обычно ассоциируемого с Т‑клетками и натуральными киллерами. Интерферон‑гамма помогает очищать организм от вирусов, но также усугубляет повреждение гематоэнцефалического барьера. Исследование показало, что моноциты формировали скопления около Ackr1‑положительных эндотелиальных клеток и взаимодействовали с ними посредством множества хемокинов, создавая петлю обратной связи, привлекающую ещё больше иммунных клеток. Вокруг этих сосудов многие клетки — включая сами моноциты — проявляли молекулярные признаки взрывных форм клеточной гибели (пироптоз и некроптоз), выбрасывающей воспалительное содержимое в окружающую ткань.
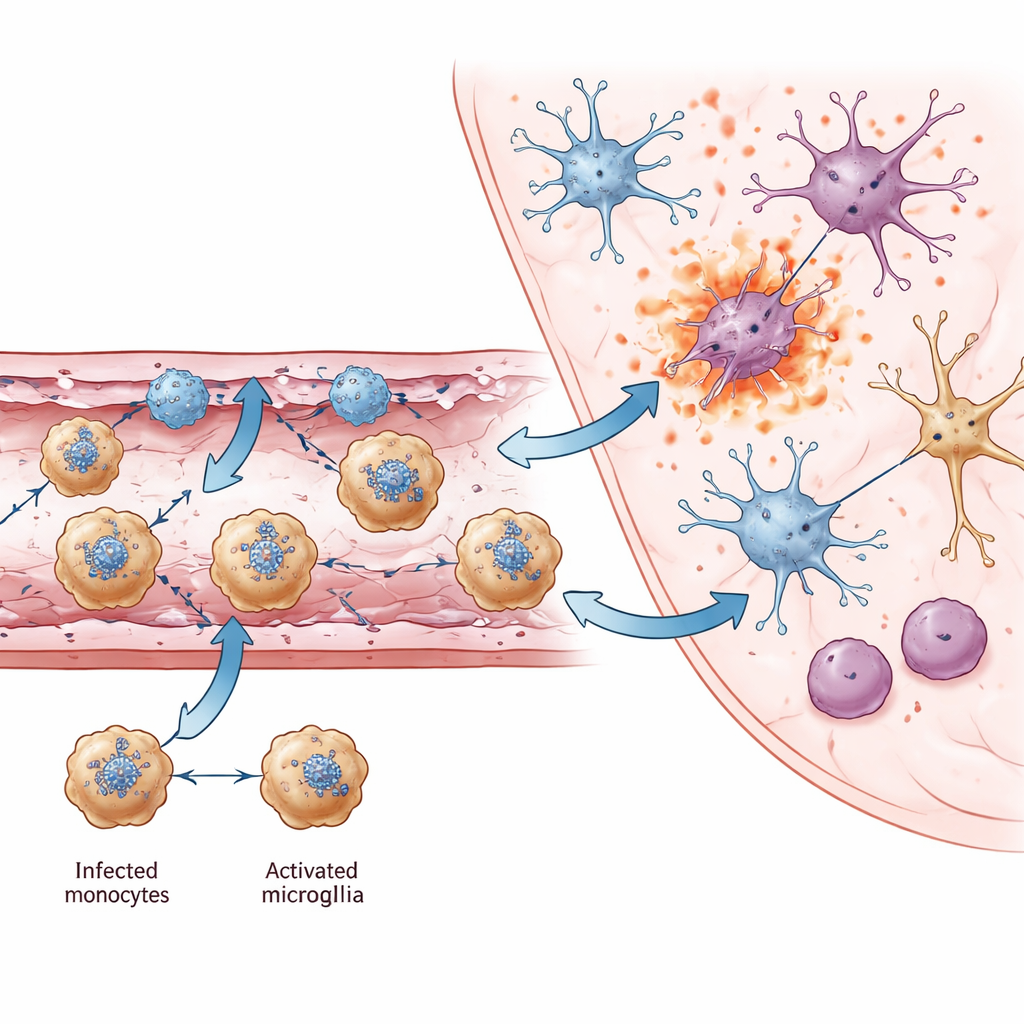
От локального сосудистого повреждения к широкому поражению мозга
По мере прогрессирования инфекции и резидентные клетки мозга изменялись. Микроглия, врождённые иммунные стражи мозга, переходили в активированное состояние, отмеченное хемокином Ccl12 и выражённой антивирусной активностью генов. Хотя эти изменения помогают бороться с вирусом, они также сопровождались снижением экспрессии генов, вовлечённых в синапсы, обучение и память. В сильно инфицированных областях, таких как таламус, разные подтипы нейронов, позитивные по вирусной РНК, демонстрировали повышенные признаки пироптоза и некроптоза, указывая на воспалительную гибель клеток как ключевую причину утраты нейронов. В нескольких областях мозга авторы выделили общие нейрональные гены, чья пониженная активность также связывалась с когнитивными и двигательными нарушениями при других заболеваниях мозга, что указывает на общую молекулярную основу долгосрочных инвалидизаций у выживших.
Что это значит для будущих терапий
Для неспециалиста основной вывод таков: японский энцефалит — это не только история о вирусе, атакующем нейроны. Это также история инфицированных моноцитов и специализированных сосудистых клеток, образующих разрушительный союз на границах мозга. Вместе они ослабляют гематоэнцефалический барьер, привлекают волны иммунных клеток и запускают воспалительные формы клеточной гибели, которые распространяются от сосудов в ткань мозга. Выявив ключевых участников — моноциты с позитивностью по Ly6c2 и эндотелиальные клетки с позитивностью по Ackr1 — исследование предлагает новые терапевтические подходы: препараты, снижающие уровни определённых хемокинов, блокирующие рецептор Ackr1 или ограничивающие набор моноцитов и пироптоз, могли бы смягчить наиболее тяжёлые повреждения мозга, не препятствуя при этом противовирусной защите.
Цитирование: Ou, Z., Wang, Z., Chen, Q. et al. Spatial transcriptomics uncovers vasculature-centered cellular interactions driving Japanese encephalitis progression in a mouse model. Nat Commun 17, 4089 (2026). https://doi.org/10.1038/s41467-026-70047-5
Ключевые слова: Японский энцефалит, воспаление мозга, гематоэнцефалический барьер, моноциты, пространственная транскриптомика