Clear Sky Science · it
La trascrittomica spaziale svela interazioni cellulari centrate sulla vascolatura che guidano la progressione dell’encefalite giapponese in un modello murino
Perché questo studio sull’infezione cerebrale è importante
L’encefalite giapponese è un’infezione cerebrale trasmessa dalle zanzare che può lasciare i sopravvissuti con problemi di movimento e memoria per tutta la vita, soprattutto nei bambini. Eppure i medici sono ancora privi di farmaci che colpiscano direttamente il virus o l’infiammazione dannosa che esso scatena nel cervello. Questo studio utilizza una potente tecnologia di mappatura per osservare, quasi cellula per cellula, come il virus e le cellule del sistema immunitario si muovono attraverso il cervello dei topi. In tal modo rivela una sorprendente collaborazione tra vasi sanguigni e cellule immunitarie mobili che aiuta a spiegare come la malattia diventi così distruttiva.
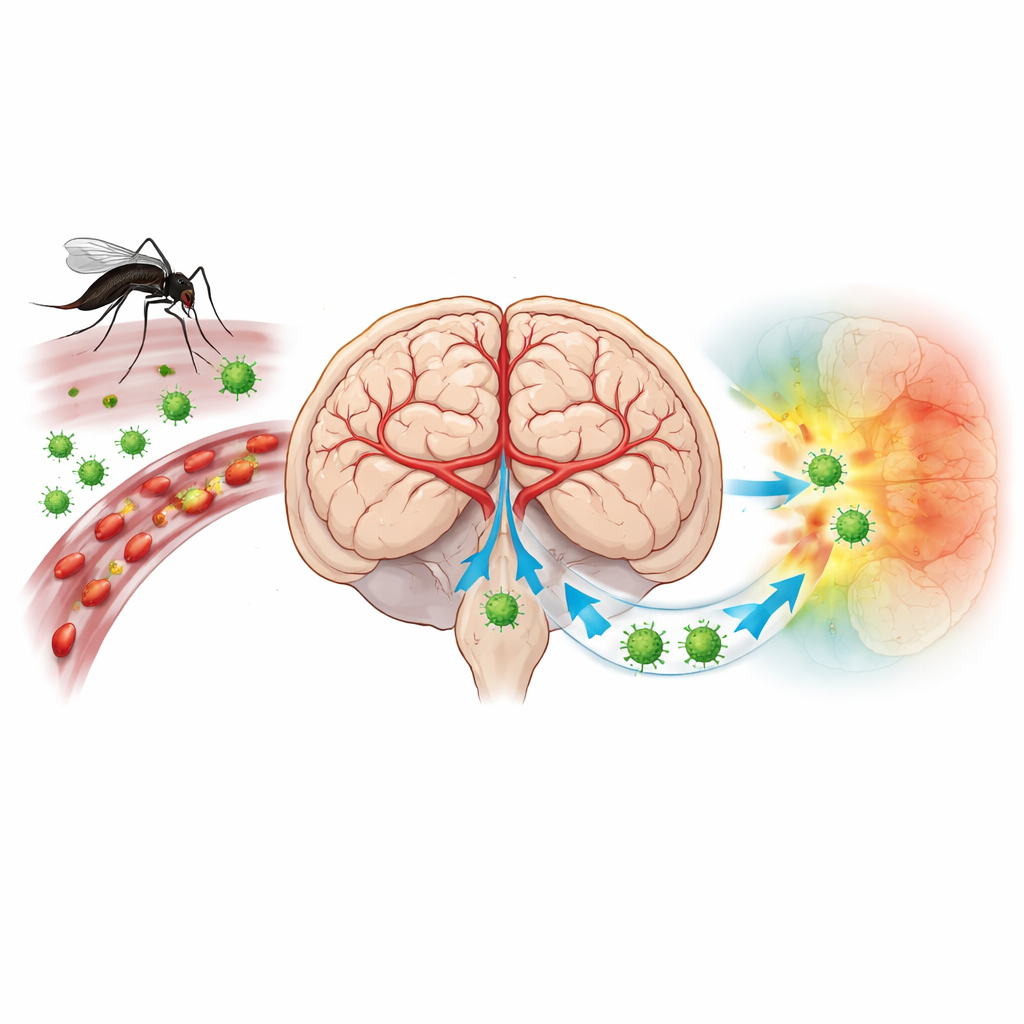
Un virus che rivolge le difese del cervello contro se stesso
Il virus dell’encefalite giapponese (JEV) è trasmesso dalle zanzare e minaccia più di tre miliardi di persone in Asia e nel Pacifico occidentale. La maggior parte delle infezioni è silente, ma quando il virus raggiunge il cervello può causare febbre alta, convulsioni e coma. I vaccini riducono il rischio, ma molte persone rimangono non protette e non esiste un trattamento antivirale specifico. Gli scienziati sospettano da tempo che il modo in cui le cellule immunitarie entrano nel cervello e come interagiscono con i vasi sanguigni cerebrali sia centrale per la malattia. Tuttavia i metodi tradizionali non potevano facilmente mostrare quali cellule esatte erano infettate e come fossero disposte nella delicata architettura cerebrale.
Una mappa molecolare dell’infezione nello spazio e nel tempo
I ricercatori hanno infettato topi femmina con JEV ed esaminato i loro cervelli ai giorni 3, 5 e 7 post-infezione, coprendo l’aumento dei livelli virali e l’insorgenza dei sintomi gravi. Hanno usato una tecnologia chiamata trascrittomica spaziale, che legge quali geni sono attivi in migliaia di piccoli punti su una sottile sezione cerebrale, preservando la posizione di ciascun punto nel tessuto. Sonde personalizzate hanno permesso di rilevare sia l’RNA del topo sia quello virale sulla stessa vetrino. Combinando queste mappe con atlanti cerebrali e riferimenti per tipi cellulari, hanno costruito un atlante spazio-temporale: quali regioni cerebrali il virus predilige, quali tipi cellulari infetta e come si sviluppano le risposte immunitarie locali.
I vasi sanguigni come porte d’ingresso e amplificatori
L’atlante ha mostrato che JEV compare inizialmente in una piccola frazione del tessuto cerebrale, per poi espandersi coinvolgendo in modo massiccio il talamo e la corteccia cerebrale. Ancora più evidente è stato il luogo in cui comparivano i segnali immunitari più forti: lungo i vasi sanguigni, in particolare nelle sottili membrane (meningi) che avvolgono il cervello e nel plesso corioideo, un tessuto che contribuisce a formare il liquido cerebrospinale. Qui, un sottotipo speciale di cellule endoteliali — cellule che rivestono i vasi sanguigni — contraddistinte da un recettore chiamato Ackr1 risultava altamente attivato. Queste cellule producevano numerose chemochine, molecole che attraggono le cellule immunitarie, attivavano geni legati all’infiammazione e sopprimevano geni che mantengono le giunzioni strette, le sigillature che preservano l’integrità della barriera emato-encefalica. Allo stesso tempo, test con un colorante hanno confermato che la barriera era effettivamente diventata permeabile.
Monociti: cavalli di Troia e amplificatori di segnali
Tra tutte le cellule immunitarie che entrano nel cervello, una ha spiccato: una popolazione di monociti positivi per Ly6c2. Mappe spaziali e citometria a flusso hanno mostrato che queste cellule erano spesso infettate da JEV, rendendole probabili vettori che trasportano il virus attraverso vasi danneggiati nel cervello — proprio come un cavallo di Troia. Facevano più che trasportare il virus. Questi monociti producevano grandi quantità di interferone-gamma, un potente messaggero immunitario solitamente associato alle cellule T e alle cellule natural killer. L’interferone-gamma è noto per aiutare a eliminare i virus ma anche per peggiorare il danno alla barriera emato-encefalica. Lo studio ha rilevato che i monociti si raggruppavano vicino alle cellule endoteliali Ackr1-positive e comunicavano con esse tramite molte chemochine, formando un circuito di retroazione che richiamava ulteriori cellule immunitarie. Intorno a questi vasi, molte cellule — inclusi gli stessi monociti — mostravano firme molecolari di forme esplosive di morte cellulare (piropotosi e necroptosi) che riversano contenuti infiammatori nei tessuti circostanti.
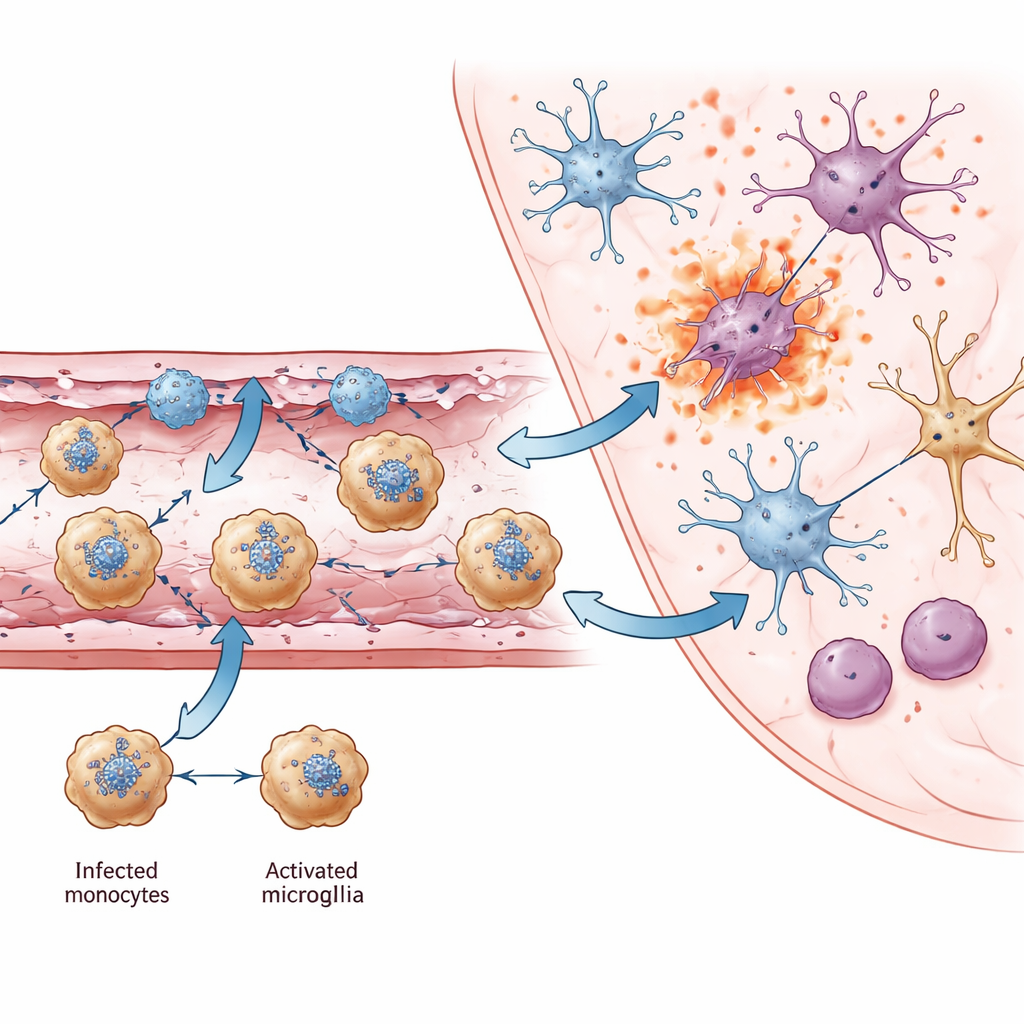
Dal danneggiamento vascolare locale a lesioni cerebrali diffuse
Con il progredire dell’infezione, anche le cellule residenti del cervello cambiarono. Le microglia, le sentinelle immunitarie innate del cervello, passarono a uno stato attivato contraddistinto dalla chemochina Ccl12 e da una forte attività di geni antivirali. Sebbene questi cambiamenti aiutino a combattere il virus, coincidevano anche con la perdita di geni coinvolti nelle sinapsi, nell’apprendimento e nella memoria. Nelle regioni fortemente infettate, come il talamo, diversi sottotipi neuronali che risultavano positivi per RNA virale mostravano segnali elevati di piropotosi e necroptosi, indicando che la morte cellulare infiammatoria è una causa chiave della perdita neuronale. In più regioni cerebrali, gli autori hanno identificato geni neuronali comuni la cui ridotta attività è stata collegata anche a problemi cognitivi e motori in altre malattie cerebrali, suggerendo una base molecolare condivisa per le disabilità a lungo termine osservate nei sopravvissuti.
Cosa significa per i trattamenti futuri
Per un lettore non specialista, il messaggio centrale è che l’encefalite giapponese non è solo la storia di un virus che attacca i neuroni. È anche la storia di monociti infettati e di cellule vascolari specializzate che formano un’alleanza dannosa ai margini del cervello. Insieme allentano la barriera emato-encefalica, richiamano ondate di cellule immunitarie e scatenano forme di morte cellulare infiammatoria che si propagano dai vasi nel tessuto cerebrale. Individuando questi protagonisti chiave — i monociti Ly6c2-positivi e le cellule endoteliali Ackr1-positive — lo studio suggerisce nuovi approcci terapeutici: farmaci che riducano chemochine specifiche, blocchino il recettore Ackr1 o limitino il reclutamento dei monociti e la piropotosi potrebbero attenuare il danno cerebrale più grave consentendo comunque alle difese antivirali di agire.
Citazione: Ou, Z., Wang, Z., Chen, Q. et al. Spatial transcriptomics uncovers vasculature-centered cellular interactions driving Japanese encephalitis progression in a mouse model. Nat Commun 17, 4089 (2026). https://doi.org/10.1038/s41467-026-70047-5
Parole chiave: Encefalite giapponese, infiammazione cerebrale, barriera emato-encefalica, monociti, trascrittomica spaziale