Clear Sky Science · fr
La transcriptomique spatiale révèle des interactions cellulaires centrées sur la vascularisation qui entraînent la progression de l’encéphalite japonaise dans un modèle murin
Pourquoi cette étude sur l’infection cérébrale est importante
L’encéphalite japonaise est une infection cérébrale transmise par les moustiques qui peut laisser les survivants avec des troubles moteurs et mnésiques permanents, en particulier chez les enfants. Pourtant, les cliniciens n’ont toujours pas de médicaments ciblant directement le virus ou l’inflammation délétère qu’il déclenche dans le cerveau. Cette étude utilise une technologie de cartographie puissante pour observer, presque cellule par cellule, comment le virus et les cellules immunitaires de l’organisme se déplacent à travers le cerveau de la souris. Ce faisant, elle met en lumière une association surprenante entre vaisseaux sanguins et cellules immunitaires en migration qui aide à expliquer pourquoi la maladie devient si destructrice.
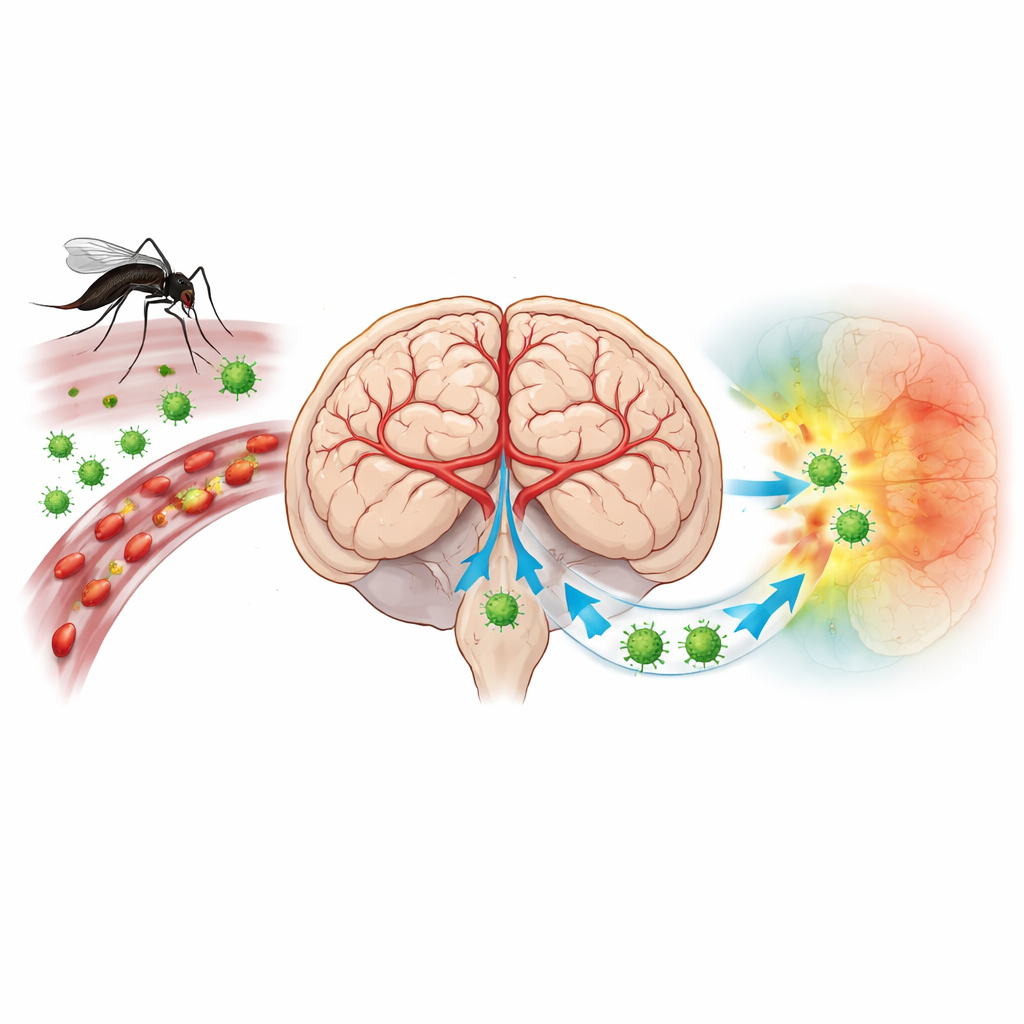
Un virus qui retourne les défenses du cerveau contre lui
Le virus de l’encéphalite japonaise (JEV) est transmis par les moustiques et menace plus de trois milliards de personnes à travers l’Asie et le Pacifique occidental. La plupart des infections sont silencieuses, mais lorsque le virus atteint le cerveau il peut provoquer forte fièvre, convulsions et coma. Les vaccins réduisent le risque, mais beaucoup restent non protégés et il n’existe pas de traitement antiviral spécifique. Les scientifiques soupçonnent depuis longtemps que la manière dont les cellules immunitaires pénètrent dans le cerveau, et leur interaction avec les vaisseaux sanguins cérébraux, est centrale dans la maladie. Cependant, les méthodes traditionnelles ne permettaient pas facilement d’identifier quelles cellules exactes étaient infectées et comment elles s’organisaient dans l’architecture délicate du cerveau.
Une cartographie moléculaire de l’infection dans l’espace et le temps
Les chercheurs ont infecté des souris femelles par JEV et ont examiné leurs cerveaux aux jours 3, 5 et 7 après l’infection, couvrant la montée de la charge virale et l’apparition des symptômes sévères. Ils ont utilisé une technologie appelée transcriptomique spatiale, qui lit les gènes actifs à des milliers de points minuscules sur une fine coupe cérébrale, tout en conservant la position de chaque point dans le tissu. Des sondes personnalisées leur ont permis de détecter à la fois l’ARN de la souris et celui du virus sur la même lame. En combinant ces cartes avec des atlas cérébraux et des références de types cellulaires, ils ont construit un atlas spatiotemporel : quelles régions cérébrales le virus privilégie, quels types cellulaires il infecte et comment se déploient les réponses immunes locales.
Les vaisseaux sanguins comme portes d’entrée et amplificateurs
L’atlas a montré que le JEV apparaît d’abord dans une petite fraction du tissu cérébral, puis s’étend pour toucher fortement le thalamus et le cortex cérébral. Plus frappant encore était l’emplacement des signaux immunitaires les plus intenses : le long des vaisseaux sanguins, en particulier dans les membranes fines (les méninges) qui enveloppent le cerveau et dans le plexus choroïde, un tissu qui participe à la production du liquide cérébrospinal. Là, un sous-type particulier de cellules endothéliales — cellules qui tapissent les vaisseaux — marqué par un récepteur appelé Ackr1 s’est fortement activé. Ces cellules produisaient de nombreuses chimiokines, molécules attirant les cellules immunitaires, et activaient des gènes liés à l’inflammation tout en réprimant des gènes qui maintiennent les jonctions serrées, les scellements qui préservent l’intégrité de la barrière hémato-encéphalique. Parallèlement, des tests au colorant ont confirmé que la barrière était effectivement devenue perméable.
Monocytes : chevaux de Troie et amplificateurs de signaux
Parmi toutes les cellules immunitaires pénétrant dans le cerveau, une population s’est distinguée : des monocytes Ly6c2-positifs. Les cartes spatiales et la cytométrie en flux ont montré que ces cellules étaient souvent infectées par le JEV, ce qui en fait des vecteurs probables transportant le virus à travers des vaisseaux endommagés vers l’intérieur du cerveau — à la manière d’un cheval de Troie. Elles faisaient plus que transporter le virus. Ces monocytes produisaient d’importantes quantités d’interféron-gamma, un messager immunitaire puissant habituellement associé aux lymphocytes T et aux cellules NK. L’interféron-gamma aide à éliminer les virus mais peut aussi aggraver les lésions de la barrière hémato-encéphalique. L’étude a montré que les monocytes se regroupaient à proximité des cellules endothéliales Ackr1-positives et communiquaient avec elles via de multiples chimiokines, formant une boucle de rétroaction qui attirait encore davantage de cellules immunitaires. Autour de ces vaisseaux, de nombreuses cellules — y compris les monocytes eux-mêmes — affichaient des signatures moléculaires de formes explosives de mort cellulaire (pyroptose et nécroptose) qui répandent des contenus inflammatoires dans les tissus environnants.
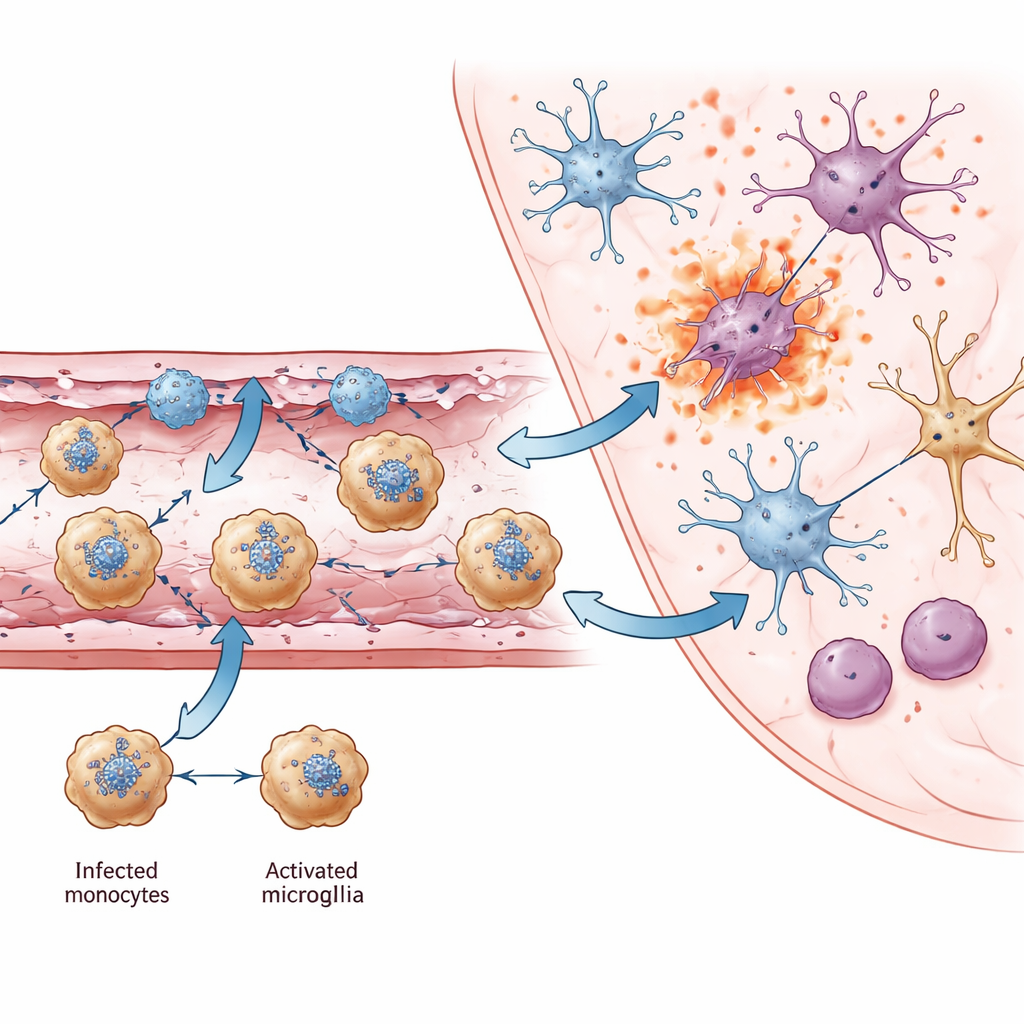
Des dommages vasculaires locaux à une lésion cérébrale étendue
À mesure que l’infection progressait, les cellules résidentes du cerveau ont également changé. Les microglies, sentinelles immunitaires innées du cerveau, sont passées à un état activé marqué par une chimiokine appelée Ccl12 et par une forte activité de gènes antiviraux. Si ces changements contribuent à combattre le virus, ils coïncident aussi avec la perte de gènes impliqués dans les synapses, l’apprentissage et la mémoire. Dans des régions fortement infectées comme le thalamus, différents sous-types de neurones positifs pour l’ARN viral présentaient une augmentation des signaux de pyroptose et de nécroptose, indiquant que la mort cellulaire inflammatoire est une cause majeure de perte neuronale. Dans plusieurs régions cérébrales, les auteurs ont identifié des gènes neuronaux communs dont la diminution d’activité a également été liée à des troubles cognitifs et moteurs dans d’autres maladies cérébrales, suggérant une base moléculaire partagée des incapacités à long terme observées chez les survivants.
Ce que cela signifie pour les traitements futurs
Pour un lecteur non spécialiste, le message principal est que l’encéphalite japonaise n’est pas seulement l’histoire d’un virus attaquant les neurones. C’est aussi l’histoire d’union nuisible entre monocytes infectés et cellules vasculaires spécialisées aux frontières du cerveau. Ensemble, ils relâchent la barrière hémato-encéphalique, attirent des vagues de cellules immunitaires et déclenchent des formes inflammatoires de mort cellulaire qui rayonnent depuis les vaisseaux dans le tissu cérébral. En identifiant ces acteurs clés — les monocytes Ly6c2-positifs et les cellules endothéliales Ackr1-positives — l’étude suggère de nouvelles pistes thérapeutiques : des médicaments réduisant des chimiokines spécifiques, bloquant le récepteur Ackr1 ou limitant le recrutement des monocytes et la pyroptose pourraient potentiellement atténuer les dommages cérébraux les plus sévères tout en préservant les défenses antivirales.
Citation: Ou, Z., Wang, Z., Chen, Q. et al. Spatial transcriptomics uncovers vasculature-centered cellular interactions driving Japanese encephalitis progression in a mouse model. Nat Commun 17, 4089 (2026). https://doi.org/10.1038/s41467-026-70047-5
Mots-clés: encéphalite japonaise, inflammation cérébrale, barrière hémato-encéphalique, monocytes, transcriptomique spatiale