Clear Sky Science · es
La transcriptómica espacial descubre interacciones celulares centradas en la vasculatura que impulsan la progresión de la encefalitis japonesa en un modelo murino
Por qué importa este estudio sobre la infección cerebral
La encefalitis japonesa es una infección cerebral transmitida por mosquitos que puede dejar a los supervivientes con problemas de movimiento y memoria de por vida, especialmente en niños. Aun así, los médicos siguen sin disponer de fármacos que ataquen directamente al virus o a la inflamación dañina que desencadena en el cerebro. Este estudio emplea una potente tecnología de cartografía para observar, casi célula por célula, cómo se desplazan el virus y las propias células inmunitarias por el cerebro de ratón. Al hacerlo, revela una sorprendente asociación entre los vasos sanguíneos y las células inmunes errantes que ayuda a explicar por qué la enfermedad se vuelve tan destructiva.
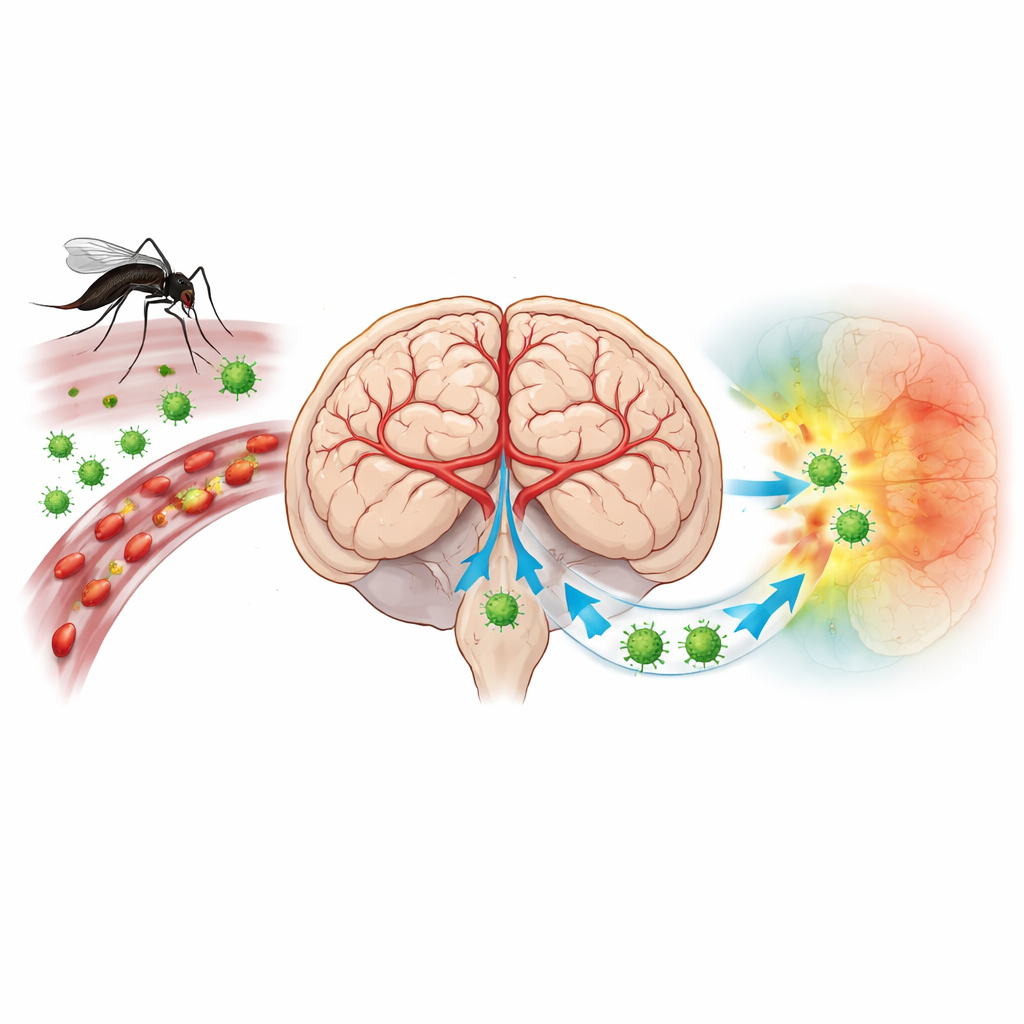
Un virus que vuelve las defensas del cerebro contra sí mismas
El virus de la encefalitis japonesa (JEV) es transmitido por mosquitos y amenaza a más de tres mil millones de personas en Asia y el Pacífico occidental. La mayoría de las infecciones son silenciosas, pero cuando el virus llega al cerebro puede provocar fiebre alta, convulsiones y coma. Las vacunas reducen el riesgo, pero muchas personas siguen sin protección y no existe un tratamiento antiviral específico. Los científicos han sospechado desde hace tiempo que la forma en que las células inmunes entran en el cerebro y cómo interactúan con los vasos sanguíneos cerebrales es central en la enfermedad. Sin embargo, los métodos tradicionales no podían mostrar con facilidad qué células exactas estaban infectadas y cómo se disponían en la delicada arquitectura cerebral.
Un mapa molecular de la infección en espacio y tiempo
Los investigadores infectaron hembras de ratón con JEV y examinaron sus cerebros en los días 3, 5 y 7 tras la infección, abarcando el aumento de los niveles virales y la aparición de síntomas graves. Utilizaron una tecnología llamada transcriptómica espacial, que detecta qué genes están activos en miles de puntos diminutos a lo largo de una fina sección cerebral, conservando la localización de cada punto en el tejido. Sondas personalizadas les permitieron detectar ARN del ratón y del virus en la misma lámina. Al combinar estos mapas con atlas cerebrales y referencias de tipos celulares, construyeron un atlas espaciotemporal: qué regiones cerebrales prefiere el virus, qué tipos celulares infecta y cómo se desarrollan las respuestas inmunitarias locales.
Los vasos sanguíneos como puertas de entrada y amplificadores
El atlas mostró que el JEV aparece primero en una pequeña fracción del tejido cerebral y luego se expande, implicando de forma marcada el tálamo y la corteza cerebral. Aún más llamativo fue dónde surgían las señales inmunitarias más intensas: a lo largo de los vasos sanguíneos, especialmente en las membranas delgadas (meninges) que envuelven el cerebro y en el plexo coroideo, un tejido que ayuda a producir el líquido cefalorraquídeo. Allí se activó de forma destacada un subtipo especial de células endoteliales —las que revisten los vasos— marcado por un receptor llamado Ackr1. Estas células produjeron muchas quimiocinas, moléculas que atraen células inmunitarias, y activaron genes vinculados a la inflamación mientras disminuían la expresión de genes que mantienen las uniones estrechas, los sellos que preservan la integridad de la barrera hematoencefálica. Al mismo tiempo, ensayos con un colorante confirmaron que la barrera efectivamente se volvió permeable.
Monocitos: caballos de Troya y amplificadores de señales
Entre todas las células inmunitarias que entraron en el cerebro, una destacó: una población de monocitos positivos para Ly6c2. Mapas espaciales y citometría de flujo mostraron que estas células estaban a menudo infectadas con JEV, lo que las convierte en probables transportadores que introducen el virus a través de vasos dañados en el cerebro, como un caballo de Troya. Hicieron más que transportar el virus. Estos monocitos produjeron grandes cantidades de interferón-gamma, un mensajero inmunitario potente habitualmente asociado a células T y células asesinas naturales. El interferón-gamma contribuye a eliminar virus pero también agrava el daño a la barrera hematoencefálica. El estudio encontró que los monocitos se agrupaban cerca de las células endoteliales positivas para Ackr1 y se comunicaban con ellas mediante múltiples quimiocinas, formando un circuito de retroalimentación que atraía a aún más células inmunitarias. Alrededor de estos vasos, muchas células —incluidos los propios monocitos— mostraron firmas moleculares de formas explosivas de muerte celular (piroptosis y necroptosis) que vierten contenidos inflamatorios al tejido circundante.
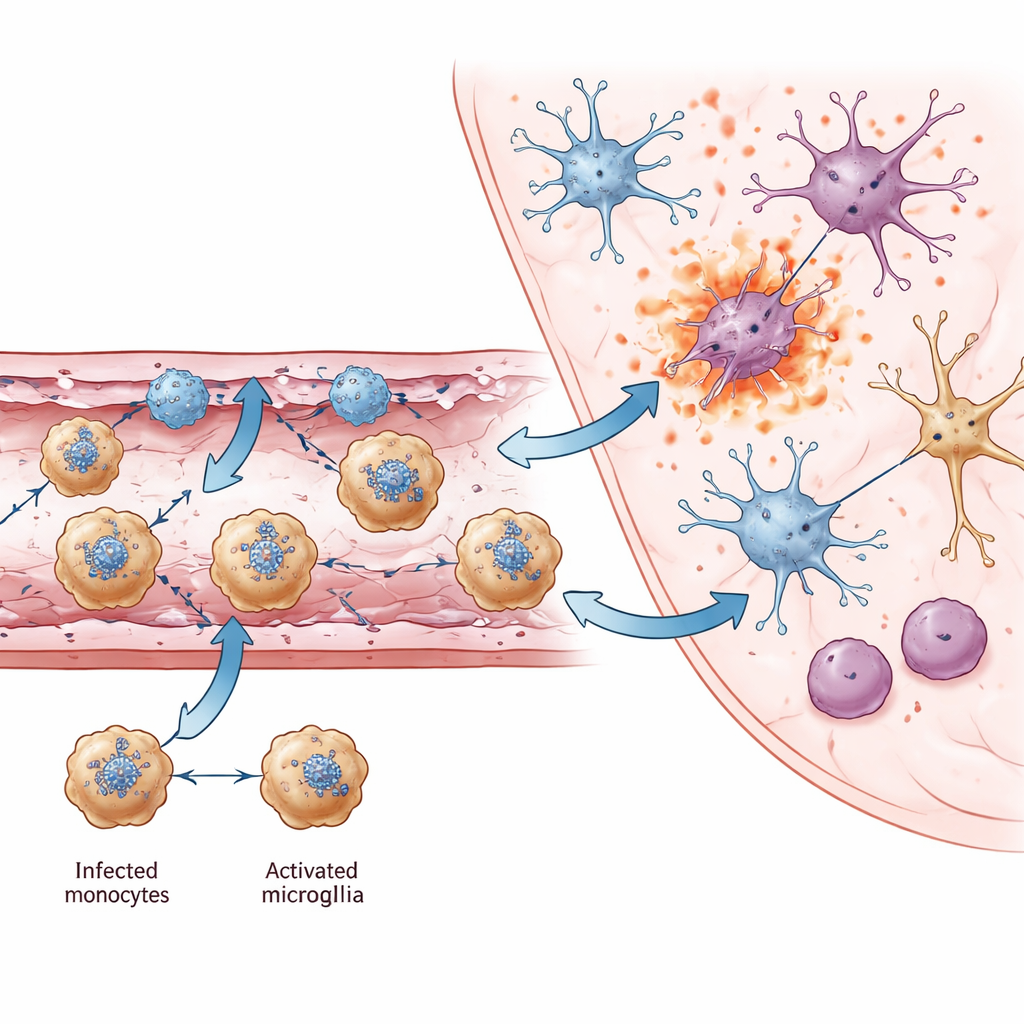
Del daño vascular local a la lesión cerebral generalizada
A medida que la infección progresó, las células residentes del cerebro también cambiaron. Las microglías, centinelas inmunitarios innatos del cerebro, pasaron a un estado activado marcado por una quimiocina llamada Ccl12 y por una intensa actividad de genes antivirales. Aunque estos cambios ayudan a combatir el virus, también coincidieron con la pérdida de genes implicados en las sinapsis, el aprendizaje y la memoria. En regiones fuertemente infectadas como el tálamo, distintos subtipos neuronales que dieron positivo para ARN viral mostraron señales elevadas de piroptosis y necroptosis, lo que apunta a la muerte celular inflamatoria como causa clave de la pérdida neuronal. En múltiples regiones cerebrales, los autores identificaron genes neuronales comunes cuya reducción de actividad también se ha asociado con problemas cognitivos y motores en otras enfermedades cerebrales, lo que sugiere una base molecular compartida para las discapacidades a largo plazo observadas en los supervivientes.
Qué significa esto para tratamientos futuros
Para un lector no experto, el mensaje central es que la encefalitis japonesa no es solo la historia de un virus atacando neuronas. Es también la historia de monocitos infectados y de células vasculares especializadas que forman una alianza dañina en los límites del cerebro. Juntos aflojan la barrera hematoencefálica, atraen oleadas de células inmunitarias y desencadenan formas inflamatorias de muerte celular que se irradian desde los vasos hacia el tejido cerebral. Al identificar a estos actores clave —los monocitos positivos para Ly6c2 y las células endoteliales positivas para Ackr1—, el estudio sugiere nuevas dianas terapéuticas: fármacos que reduzcan quimiocinas específicas, bloqueen el receptor Ackr1 o limiten el reclutamiento de monocitos y la piroptosis podrían mitigar el daño cerebral más severo mientras permiten que funcionen las defensas antivirales.
Cita: Ou, Z., Wang, Z., Chen, Q. et al. Spatial transcriptomics uncovers vasculature-centered cellular interactions driving Japanese encephalitis progression in a mouse model. Nat Commun 17, 4089 (2026). https://doi.org/10.1038/s41467-026-70047-5
Palabras clave: encefalitis japonesa, inflamación cerebral, barrera hematoencefálica, monocitos, transcriptómica espacial