Clear Sky Science · ar
علم النسخ المكانية يكشف تفاعلات خلوية متمحورة حول الأوعية الدموية تدفع تقدم التهاب الدماغ الياباني في نموذج فأري
لماذا تهمنا هذه الدراسة عن عدوى الدماغ
التهاب الدماغ الياباني مرض فيروسي يُنتقل عن طريق البعوض ويمكن أن يترك الناجين يعانون من مشاكل دائمة في الحركة والذاكرة، لا سيما الأطفال. ومع ذلك، يفتقر الأطباء إلى أدوية تستهدف الفيروس مباشرة أو الالتهاب الضار الذي يثيره في الدماغ. تستعمل هذه الدراسة تقنية رسم خرائط قوية لمراقبة، تقريباً خلية بخلية، كيف يتحرك الفيروس وخلايا الجهاز المناعي عبر دماغ الفأر. ومن خلال ذلك تكشف عن شراكة مفاجئة بين الأوعية الدموية والخلايا المناعية المتجولة تفسر كيف تصبح هذه العدوى مدمرة جداً.
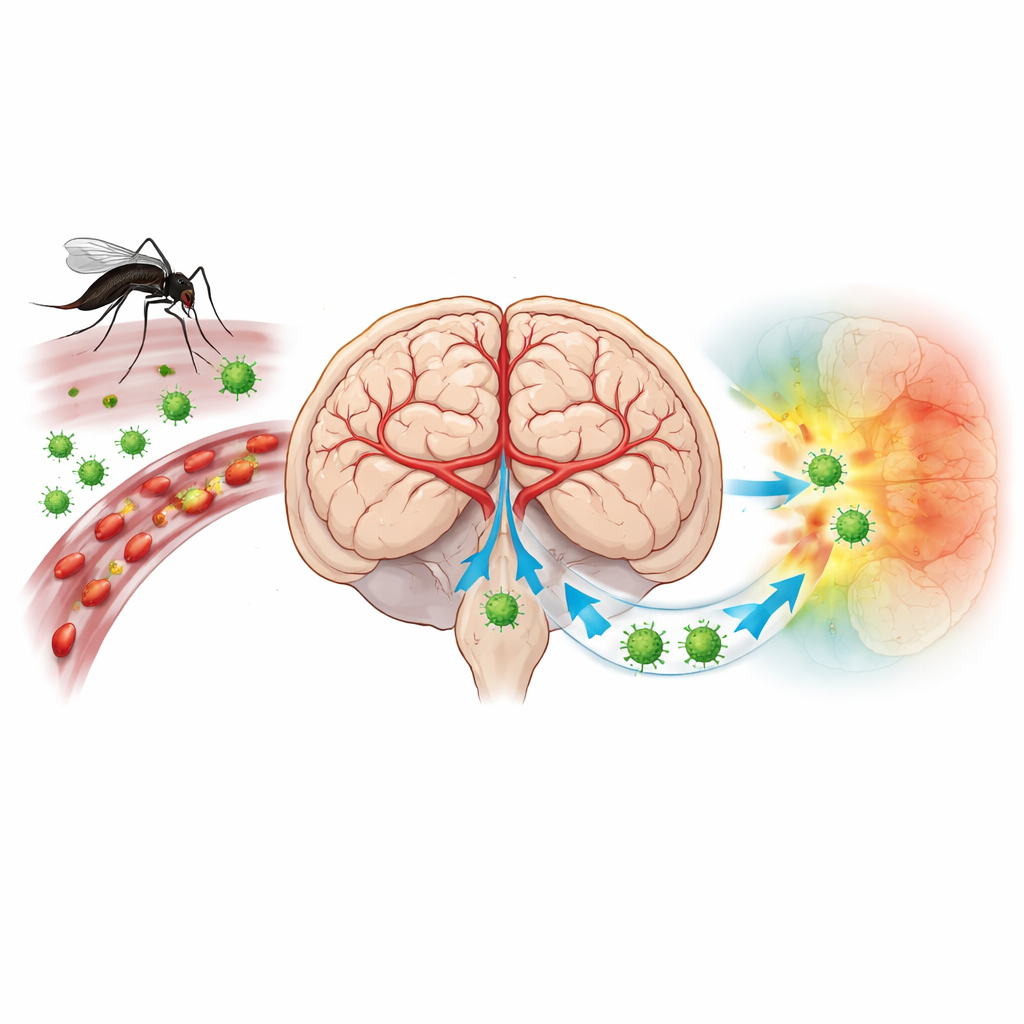
فيروس يحول دفاعات الدماغ إلى ضده
فيروس التهاب الدماغ الياباني (JEV) ينتقل عن طريق البعوض ويهدد أكثر من ثلاثة مليارات شخص عبر آسيا وغرب المحيط الهادئ. معظم الإصابات لا تظهر أعراض، لكن عندما يصل الفيروس إلى الدماغ يمكن أن يسبب حمى شديدة ونوبات وفقدان وعي. تقلل اللقاحات الخطر، لكن كثيرين يبقون غير محميين، ولا يوجد علاج مضاد للفيروس محدد. لطالما اشتبه العلماء أن طريقة دخول خلايا المناعة إلى الدماغ وكيفية تفاعلها مع الأوعية الدموية الدماغية لها دور محوري في المرض. ومع ذلك، لم تكن الطرق التقليدية قادرة بسهولة على إظهار أي الخلايا بالضبط كانت مصابة وكيف كانت مرتبة ضمن بنية الدماغ الرقيقة.
خريطة جزيئية للعدوى في المكان والزمان
أصاب الباحثون فئراناً أنثى بفيروس JEV وفحصوا أدمغتها في الأيام 3 و5 و7 بعد العدوى، لتغطية مرحلة ارتفاع مستويات الفيروس وظهور الأعراض الشديدة. استخدموا تقنية تُدعى النسخ المكانية، التي تقرأ أي الجينات نشطة في آلاف النقاط الصغيرة عبر شريحة رقيقة من الدماغ، مع الحفاظ على موقع كل نقطة داخل النسيج. سمحت مجسات مخصصة لهم بكشف كل من الرنا الماوسي والفيروسي على نفس الشريحة. من خلال دمج هذه الخرائط مع أطالس الدماغ ومرجعيات نوع الخلايا، بنوا أطلساً مكانياً زمنياً: أي مناطق الدماغ يفضلها الفيروس، أي أنواع الخلايا يصيب، وكيف تتكشف الاستجابات المناعية المحلية.
الأوعية الدموية كبوابات ومضخّمة للاستجابة
أظهر الأطلس أن JEV يظهر أولاً في جزء صغير من نسيج الدماغ ثم يمتد ليشمل بشكل واسع المَيْنِصِف والمِخِّية (القشرة المخية). وما كان أكثر لفتاً هو أماكن ظهور أقوى الإشارات المناعية: امتداداً على طول الأوعية الدموية، خاصة في الأغشية الرقيقة (الأغشية المحيطة بالدماغ) وفي الضفيرة المشيمية، النسيج الذي يساهم في تكوين السائل الدماغي الشوكي. هنا تنشط شعبة خاصة من الخلايا البطانية — الخلايا التي تبطن الأوعية الدموية — والمعلمة بمستقبل يُدعى Ackr1. أنتجت هذه الخلايا الكثير من الكيموكينات، جزيئات تجذب خلايا المناعة، وفعلت جينات مرتبطة بالالتهاب بينما خفضت نشاط جينات تحافظ على الوصلات المحكمة، الأختام التي تحافظ على سلامة الحاجز الدماغي الوعائي. وفي الوقت نفسه، أكدت تجارب صبغة أن الحاجز قد أصبح بالفعل متسرباً.
الوحيدات (مونوسايت): الأحصنة الطروادة ومعزِّزات الإشارة
من بين جميع خلايا المناعة التي دخلت الدماغ، برز نوع واحد: مجموعة من الوحيدات الإيجابية لـ Ly6c2. أظهرت الخرائط المكانية والقياس الخلوي بالتدفق أن هذه الخلايا كثيراً ما كانت مصابة بـ JEV، مما يجعلها ناقلين محتملين ينقلون الفيروس عبر الأوعية المتضررة إلى الدماغ — تماماً كالحصان الطروادي. ولم تكتفِ بنقل الفيروس. أنتجت هذه الوحيدات كميات كبيرة من الإنترفيرون-غاما، رسول مناعي قوي عادة ما يرتبط بالخلايا التائية والخلايا القاتلة الطبيعية. يُعرف الإنترفيرون-غاما بمساهمته في تطهير الفيروسات لكنه أيضاً يزيد من تلف الحاجز الدماغي الوعائي. وجدت الدراسة أن الوحيدات تجمعت بالقرب من الخلايا البطانية الإيجابية لـ Ackr1 وتواصَلَت معها عبر عدة كيموكينات، مُشكِّلة حلقة تغذية راجعة جذبت المزيد من خلايا المناعة. حول هذه الأوعية، أظهرت العديد من الخلايا — بما فيها الوحيدات نفسها — بصمات جزيئية لأشكال تفجُّرية من موت الخلايا (بايروبتوزيس ونِكروبْتوزيس) التي تفرغ محتويات ملتهبة في النسيج المحيط.
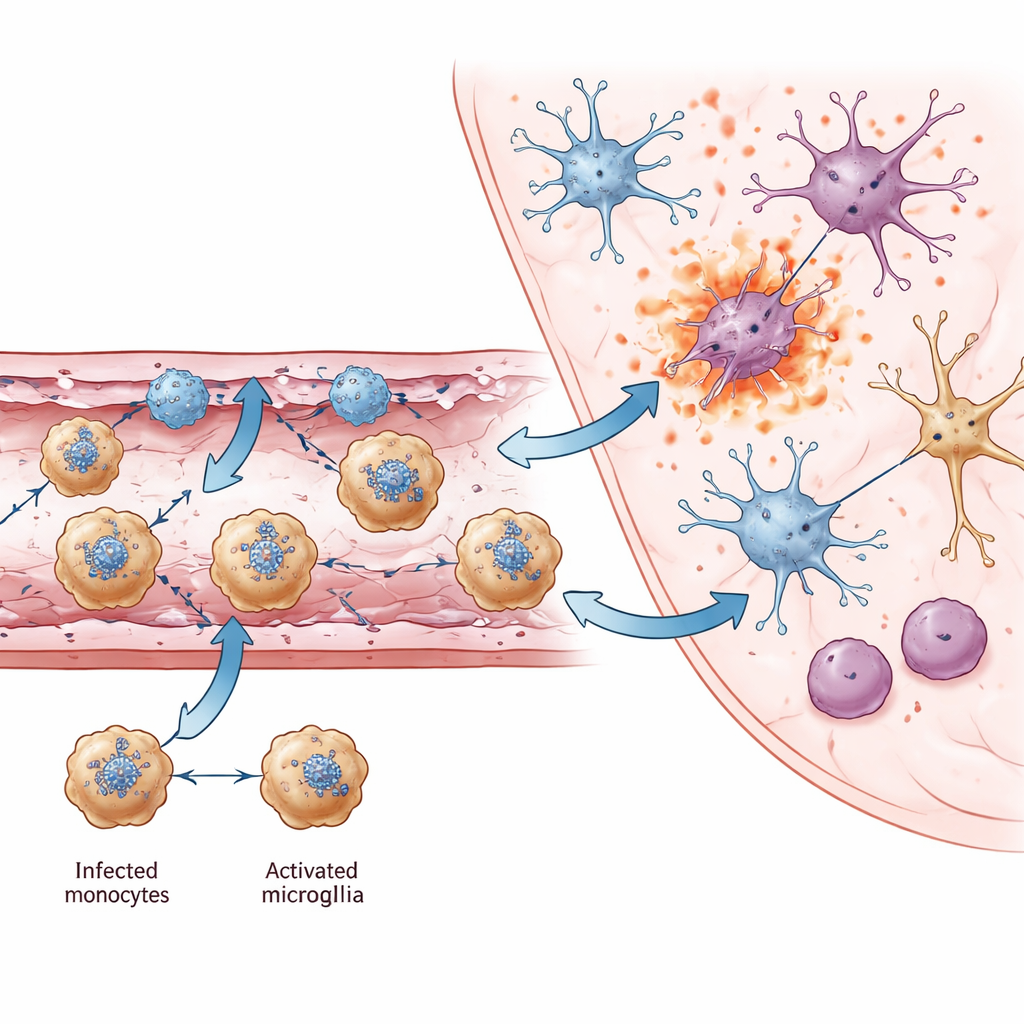
من تلف وعائي محلي إلى إصابة دماغية واسعة
مع تقدم العدوى، تغيرت أيضاً خلايا الدماغ المقيمة. تحولت الخلايا النخاعية الصغيرة (الميكروغليا)، الحارسات المناعية الفطرية للدماغ، إلى حالة مفعلة ميزها تعبير عن كيموكين يسمى Ccl12 ونشاط قوي للجينات المضادة للفيروسات. وبينما تساعد هذه التغيرات في محاربة الفيروس، ترافقت أيضاً مع فقدان جينات مشاركة في المشابك والتعلم والذاكرة. في مناطق مصابة بشدة مثل المَيْنِصِف، أظهرت أنماط فرعية مختلفة من الخلايا العصبية الإيجابية للرنا الفيروسي إشارات متزايدة للبايروبتوزيس والنِكروبْتوزيس، مما يشير إلى أن موت الخلايا الالتهابي هو سبب رئيسي لفقدان الخلايا العصبية. عبر مناطق دماغية متعددة، حدَّد المؤلفون جينات عصبية مشتركة انخفض نشاطها والتي رُبط انخفاضها أيضاً بمشاكل إدراكية وحركية في أمراض دماغية أخرى، ما يوحي بوجود أساس جزيئي مشترك للعجز طويل الأمد الذي يُرى لدى الناجين.
ما الدلالة العلاجية لهذا
بالنسبة إلى القارئ العام، الرسالة الجوهرية هي أن التهاب الدماغ الياباني ليس مجرد قصة فيروس يهاجم الخلايا العصبية. إنها أيضاً قصة وحيدات مصابة وخلايا وعائية متخصصة تشكل تحالفاً ضاراً عند حدود الدماغ. معاً يضعفون الحاجز الدماغي الوعائي، يجتذبون موجات من خلايا المناعة، ويثيرون أشكالاً التهابية من موت الخلايا التي تنتشر من الأوعية إلى نسيج الدماغ. من خلال تحديد هؤلاء اللاعبين الرئيسيين — الوحيدات الإيجابية لـ Ly6c2 والخلايا البطانية الإيجابية لـ Ackr1 — تقترح الدراسة زوايا علاجية جديدة: أدوية تقلل كيموكينات محددة، تحجب مستقبل Ackr1، أو تحد من تجنيد الوحيدات والبايروبتوزيس قد تخفف من أسوأ الأضرار الدماغية مع السماح للدفاعات المضادة للفيروسات بالعمل.
الاستشهاد: Ou, Z., Wang, Z., Chen, Q. et al. Spatial transcriptomics uncovers vasculature-centered cellular interactions driving Japanese encephalitis progression in a mouse model. Nat Commun 17, 4089 (2026). https://doi.org/10.1038/s41467-026-70047-5
الكلمات المفتاحية: التهاب الدماغ الياباني, التهاب الدماغ, الحاجز الدماغي الوعائي, الوحيدات (مونوسايت), النسخ المكانية