Clear Sky Science · tr
Hücresel etkileşimleri damar merkezli açığa çıkaran mekânsal transkriptomik, fare modelinde Japon ensefaliti ilerleyişini ortaya koyuyor
Bu beyin enfeksiyonu çalışması neden önemli
Japon ensefaliti, sivrisineklerle bulaşan bir beyin enfeksiyonudur ve özellikle çocuklarda hayatta kalanlarda ömür boyu süren hareket ve hafıza sorunlarına yol açabilir. Buna rağmen hekimlerin virüsü doğrudan hedef alan ya da beyinde tetiklediği zararlı iltihabı düzelten ilaçları hâlâ yok. Bu çalışma, virüsün ve vücudun kendi bağışıklık hücrelerinin fare beyninde neredeyse hücre hücre nasıl yayıldığını izlemek için güçlü bir haritalama teknolojisi kullanıyor. Böylece hastalığın bu kadar yıkıcı hale gelmesini açıklamaya yardımcı olan, damarlar ile dolaşan bağışıklık hücreleri arasında beklenmedik bir ortaklığı ortaya koyuyor.
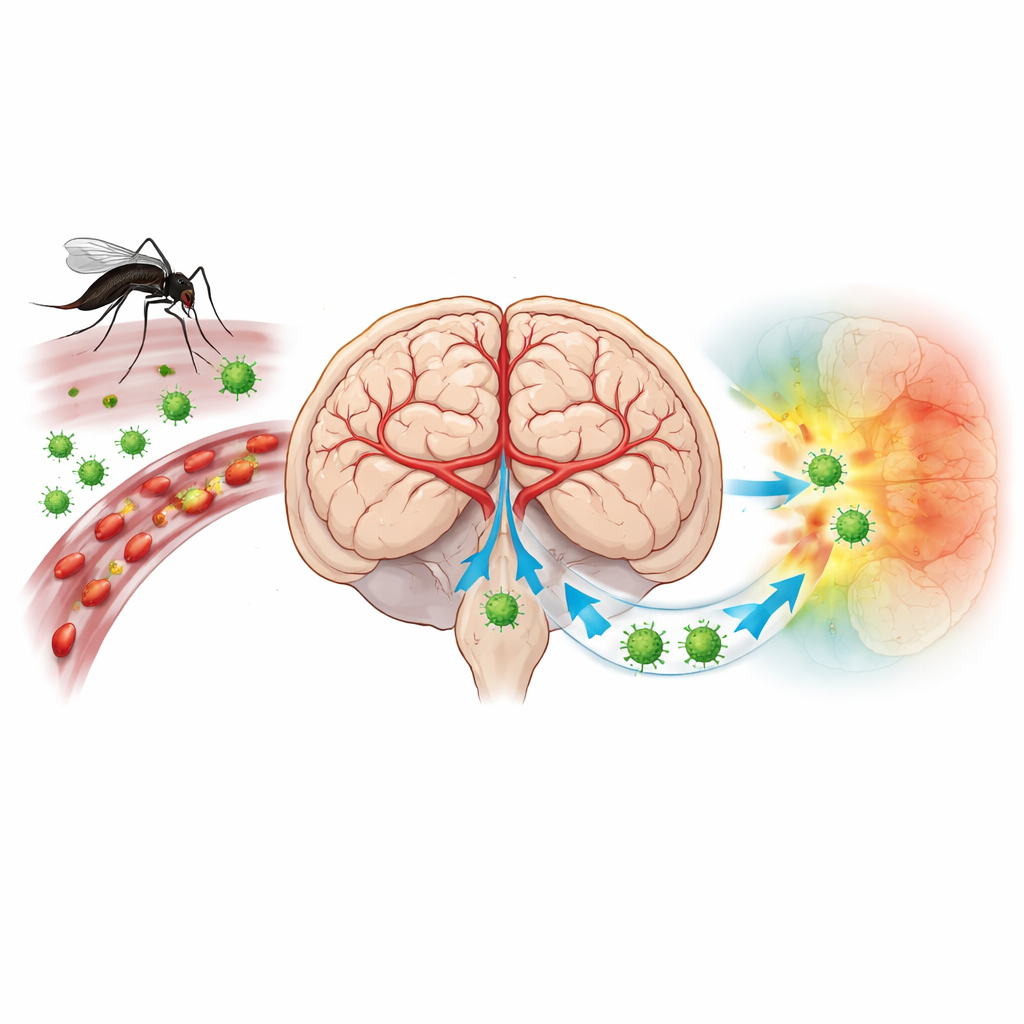
Beyninin savunmasını kendi aleyhine çeviren bir virüs
Japon ensefaliti virüsü (JEV) sivrisinekler tarafından taşınır ve Asya ile Batı Pasifik’te üç milyardan fazla insanı tehdit eder. Çoğu enfeksiyon belirtisizdir, ancak virüs beyne ulaştığında yüksek ateş, nöbetler ve koma gibi ağır belirtilere neden olabilir. Aşılar riski azaltır, ancak birçok insan korunmamış durumda ve spesifik bir antiviral tedavi yoktur. Bilim insanları uzun zamandır bağışıklık hücrelerinin beyne giriş yolları ve bu hücrelerin beyin kan damarlarıyla nasıl etkileştiğinin hastalıkta merkezi bir rol oynadığını şüphe etmişlerdir. Ancak geleneksel yöntemler tam olarak hangi hücrelerin enfekte olduğunu ve bunların beynin hassas mimarisinde nasıl düzenlendiğini kolayca gösteremiyordu.
Zaman ve mekânda enfeksiyonun moleküler haritası
Araştırmacılar dişi fareleri JEV ile enfekte etti ve beyinlerini enfeksiyondan sonra 3., 5. ve 7. günlerde inceledi; bu zaman aralığı virüs seviyelerinin yükselmesini ve şiddetli belirtilerin başlamasını kapsıyor. Mekânsal transkriptomik adı verilen bir teknoloji kullandılar; bu yöntem, ince bir beyin kesitindeki binlerce küçük noktada hangi genlerin aktif olduğunu okurken her noktanın doku içindeki yerini koruyor. Özel problar aynı deneyde hem fare hem de viral RNA’yı tespit etmelerini sağladı. Bu haritaları beyin atlasları ve hücre tipi referanslarıyla birleştirerek zamansal-mekânsal bir atlas oluşturdular: virüsün hangi beyin bölgelerini tercih ettiği, hangi hücre tiplerini enfekte ettiği ve yerel bağışıklık yanıtlarının nasıl geliştiği.
Açılan kapılar ve güçlendiren damarlar
Atlas, JEV’nin önce beyin dokusunun küçük bir bölümünde ortaya çıktığını, ardından talamus ve serebral korteksi yoğun biçimde kapsayacak şekilde genişlediğini gösterdi. Daha çarpıcı olan, en güçlü bağışıklık sinyallerinin nerede göründüğüydü: kan damarları boyunca, özellikle beyni saran ince zarlar (meninksler) ve beyin-omurilik sıvısının yapımında rol oynayan koroid pleksus dokusunda. Burada Ackr1 adlı bir reseptörle işaretlenen özel bir endotelyal hücre alt türü yüksek düzeyde aktive oldu. Bu hücreler birçok kemokin üretti — yani bağışıklık hücrelerini çeken moleküller — ve iltihapla ilişkili genleri açarken, kan–beyin bariyerinin bütünlüğünü sağlayan sıkı bağlantıları (tight junction) koruyan genlerin ifadesini bastırdı. Aynı zamanda, bir boya ile yapılan testler bariyerin gerçekten sızgan hale geldiğini doğruladı.
Monositler: Truva atları ve sinyal güçlendiriciler
Beyne giren tüm bağışıklık hücreleri arasında öne çıkan bir popülasyon vardı: Ly6c2-pozitif monositler. Mekânsal haritalar ve akım sitometrisi bu hücrelerin sıklıkla JEV ile enfekte olduğunu gösterdi; bu da onları hasarlı damarlar aracılığıyla virüsü beyne taşıyan muhtemel taşıyıcılar — Truva atları — haline getiriyor. Bunlar sadece virüsü taşımakla kalmıyordu. Bu monositler, genellikle T hücreleri ve doğal öldürücü hücrelerle ilişkilendirilen güçlü bir bağışıklık habercisi olan interferon-gama ürettiler. Interferon-gama virüsleri temizlemeye yardımcı olabilir ancak aynı zamanda kan–beyin bariyeri hasarını da kötüleştirebilir. Çalışma, monositlerin Ackr1-pozitif endotelyal hücrelerin yakınında kümelendiğini ve onları birçok kemokin aracılığıyla iletişim kurarak daha fazla bağışıklık hücresini çeken bir geri besleme döngüsü oluşturduğunu buldu. Bu damarların çevresinde, monositler de dahil olmak üzere birçok hücre, çevre dokuya iltihaplı içerik saçan patlayıcı hücre ölümü formu (piropitoz ve nekroptoz) moleküler imzaları gösteriyordu.
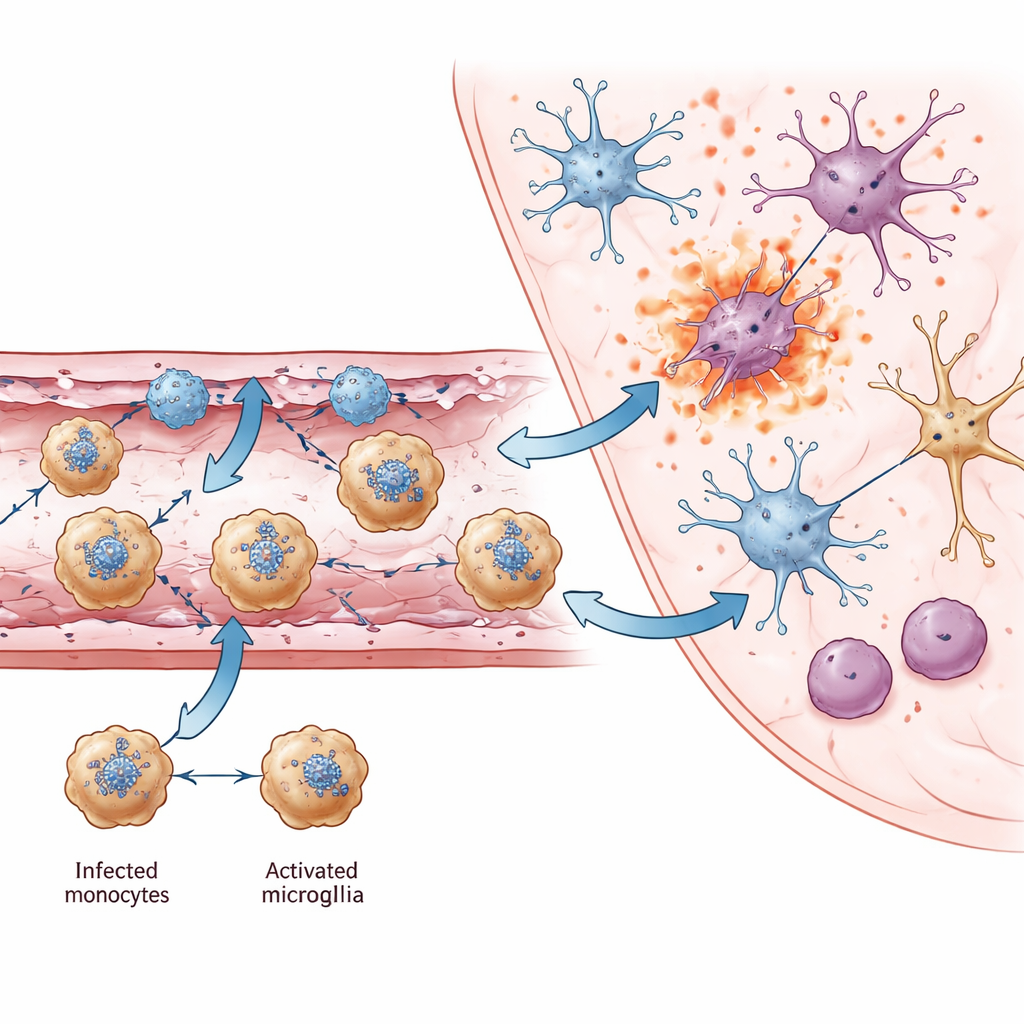
Yerel vasküler hasardan yaygın beyin yaralanmasına
Enfeksiyon ilerledikçe, yerleşik beyin hücreleri de değişti. Beynin doğuştan gelen immün nöbetçileri olan mikroglialar, Ccl12 adlı bir kemokinle işaretlenen ve güçlü antiviral gen aktivitesiyle tanımlanan aktifleşmiş bir duruma geçti. Bu değişiklikler virüsle mücadeleye yardımcı olurken, aynı zamanda sinapslar, öğrenme ve hafıza ile ilişkili genlerin kaybıyla da örtüştü. Talamus gibi yoğun enfekte bölgelerde viral RNA pozitif çıkan farklı nöron alt tipleri piropitoz ve nekroptoz sinyallerinde yükselme gösterdi; bu da nöron kaybının ana nedeni olarak iltihaplı hücre ölümünü işaret ediyor. Birden fazla beyin bölgesinde yazarlar, etkinlikleri azalmış ve diğer beyin hastalıklarında bilişsel ve motor sorunlarla ilişkilendirilmiş ortak nöron genlerini tanımladı; bu da hayatta kalanlarda görülen uzun dönem sakatlıklar için ortak bir moleküler temel olduğunu düşündürüyor.
Gelecekteki tedaviler için çıkarımlar
Bir düz okuyucu için temel mesaj, Japon ensefalitinin sadece virüsün nöronları saldırması hikâyesi olmadığıdır. Aynı zamanda enfekte monositlerin ve uzmanlaşmış damar hücrelerinin beyin sınırlarında zararlı bir ittifak kurmasının da hikâyesidir. Birlikte kan–beyin bariyerini gevşetir, dalgalar halinde bağışıklık hücrelerini çeker ve damarlardan beyin dokusuna yayılan iltihaplı hücre ölümü formlarını tetiklerler. Ly6c2-pozitif monositleri ve Ackr1-pozitif endotelyal hücreleri hedefleyerek bu kilit oyuncuları belirleyen çalışma, yeni terapötik yaklaşımlar öneriyor: belirli kemokinleri azaltan, Ackr1 reseptörünü engelleyen veya monosit alımını ve piropitozu sınırlayan ilaçlar, antiviral savunmalar çalışırken en kötü beyin hasarını azaltabilir.
Atıf: Ou, Z., Wang, Z., Chen, Q. et al. Spatial transcriptomics uncovers vasculature-centered cellular interactions driving Japanese encephalitis progression in a mouse model. Nat Commun 17, 4089 (2026). https://doi.org/10.1038/s41467-026-70047-5
Anahtar kelimeler: Japon ensefaliti, beyin iltihabı, kan–beyin bariyeri, monositler, mekânsal transkriptomik