Clear Sky Science · sv
Spatial transkriptomik avslöjar kärlnära cellulära interaktioner som driver japansk encefalit i en musmodell
Varför denna studie av hjärninfektion är viktig
Japansk encefalit är en myggburen hjärninfektion som kan lämna överlevande med livslånga rörelse- och minnessvårigheter, särskilt barn. Läkare saknar fortfarande läkemedel som direkt riktar sig mot viruset eller den skadliga inflammation det utlöser i hjärnan. Denna studie använder en kraftfull kartläggningsteknik för att i praktiken se, nästan cell för cell, hur viruset och kroppens egna immunceller rör sig genom musens hjärna. Genom detta avslöjar den ett överraskande samspel mellan blodkärl och kringströvande immunceller som hjälper förklara hur sjukdomen blir så förödande.
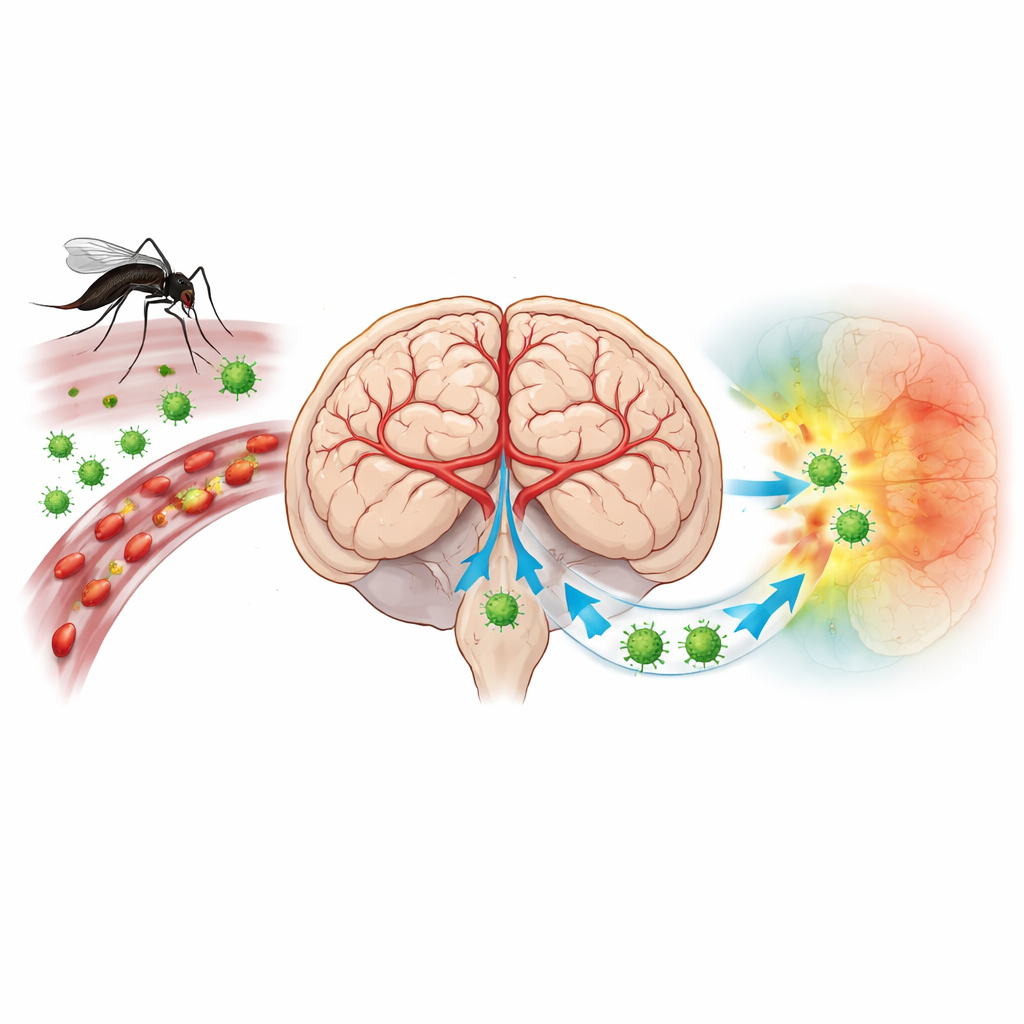
Ett virus som vänder hjärnans försvar mot sig själv
Japansk encefalitvirus (JEV) sprids via myggor och hotar mer än tre miljarder människor i Asien och Stilla havet. De flesta infektioner är tysta, men när viruset når hjärnan kan det orsaka hög feber, kramper och koma. Vacciner minskar risken, men många är fortfarande oskyddade och det finns ingen specifik antiviral behandling. Forskare har länge misstänkt att hur immunceller tar sig in i hjärnan och hur de interagerar med hjärnans blodkärl är centralt för sjukdomen. Traditionella metoder kunde dock inte enkelt visa exakt vilka celler som var infekterade och hur de var arrangerade i hjärnans känsliga arkitektur.
En molekylär karta av infektionen i rum och tid
Forskarna infekterade honor av musstam med JEV och undersökte deras hjärnor på dag 3, 5 och 7 efter infektion, vilket täcker uppgången i virusnivåer och insjuknandets början. De använde en teknik som kallas spatial transkriptomik, som läser av vilka gener som är aktiva vid tusentals små punkter över ett tunt hjärnskikt, samtidigt som positionen i vävnaden bevaras. Anpassade prober gjorde det möjligt att detektera både mus- och virus-RNA på samma snitt. Genom att kombinera dessa kartor med hjärnatlaser och celltypsreferenser byggde de en spatiotemporär atlas: vilka hjärnregioner viruset föredrar, vilka celltyper det infekterar och hur lokala immunsvar utvecklas.
Blodkärl som portar och förstärkare
Atlasen visade att JEV först dyker upp i en liten del av hjärnvävnaden för att sedan expandera och starkt involvera thalamus och hjärnbarken. Ännu mer slående var var de kraftigaste immunsignalerna uppträdde: längs blodkärl, särskilt i de tunna hinnorna (meningierna) som omsluter hjärnan och i plexus choroideus, vävnaden som hjälper till att bilda cerebrospinalvätska. Här aktiverades en speciell undergrupp av endotelceller—celler som bekläder blodkärl—markerade av en receptor kallad Ackr1. Dessa celler producerade många kemokiner, molekyler som lockar immunceller, och slog på gener kopplade till inflammation samtidigt som de nedreglerade gener som upprätthåller täta fogar, tätningarna som håller blod–hjärnbarriären intakt. Samtidigt bekräftade tester med ett färgämne att barriären faktiskt blivit läck.
Monocyter: trojanska hästar och signalhöjare
Bland alla immunceller som trängde in i hjärnan utmärkte sig en population Ly6c2-positiva monocyter. Spatiala kartor och flödescytometri visade att dessa celler ofta var infekterade av JEV, vilket gör dem till troliga bärare som för viruset över skadade kärl in i hjärnan—ungefär som en trojansk häst. De gjorde mer än bara transportera viruset. Dessa monocyter producerade stora mängder interferon-gamma, en potent immunbudbärare vanligtvis förknippad med T-celler och natural killer-celler. Interferon-gamma är känt för att hjälpa till att rensa virus men också för att förvärra skador på blod–hjärnbarriären. Studien fann att monocyter klustrade nära Ackr1-positiva endotelceller och kommunicerade med dem via flera kemokiner, vilket bildade en återkopplingsslinga som drog in ännu fler immunceller. Runt dessa kärl visade många celler—inklusive monocyterna själva—molekylära signaturer för explosiva former av celldöd (pyroptos och nekroptos) som spillde inflammatoriskt innehåll ut i omgivande vävnad.
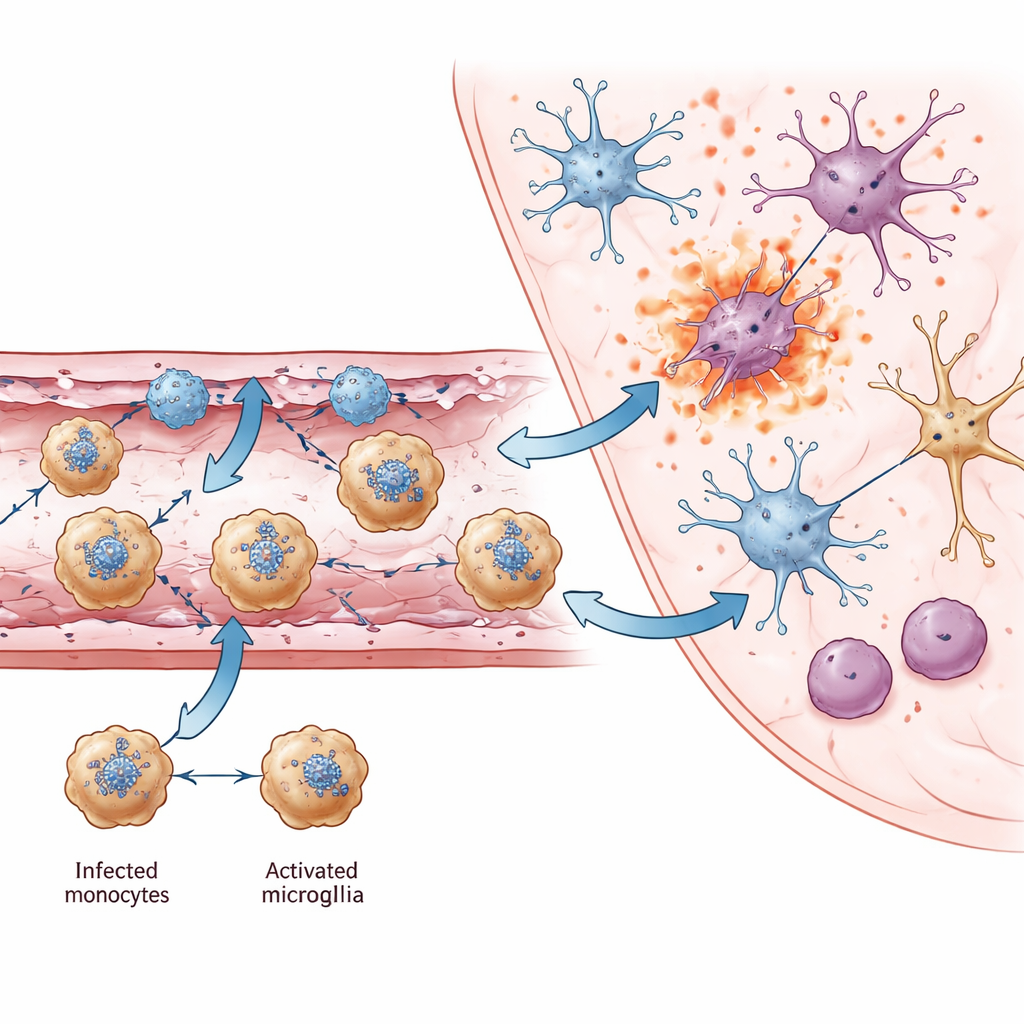
Från lokal vaskulär skada till utbredd hjärnskada
När infektionen fortskred förändrades också hjärnans egna celler. Mikroglia, hjärnans medfödda immunsentineler, skiftade till ett aktiverat tillstånd markerat av en kemokin kallad Ccl12 och av stark antiviral genaktivitet. Medan dessa förändringar hjälper till att bekämpa viruset sammanföll de också med en förlust av gener som är inblandade i synapser, inlärning och minne. I kraftigt infekterade regioner som thalamus visade olika neuronundergrupper som testade positivt för virus-RNA förhöjda signaler för pyroptos och nekroptos, vilket pekar på inflammatorisk celldöd som en nyckelorsak till neuronförlust. I flera hjärnregioner identifierade författarna gemensamma neurongener vars minskade aktivitet också har kopplats till kognitiva och motoriska problem i andra hjärnsjukdomar, vilket tyder på en delad molekylär grund för de långsiktiga funktionsnedsättningar som ses hos överlevande.
Vad detta betyder för framtida behandlingar
För en lekman är huvudbudskapet att japansk encefalit inte enbart handlar om ett virus som angriper neuroner. Det är också en berättelse om infekterade monocyter och specialiserade blodkärlsceller som bildar en skadlig allians vid hjärnans gränser. Tillsammans luckrar de upp blod–hjärnbarriären, drar till sig vågor av immunceller och utlöser inflammatoriska dödsformer som sprider sig från kärlen ut i hjärnvävnaden. Genom att peka ut dessa nyckelspelare—Ly6c2-positiva monocyter och Ackr1-positiva endotelceller—föreslår studien nya terapeutiska angreppspunkter: läkemedel som minskar specifika kemokiner, blockerar Ackr1-receptorn eller begränsar monocytrekrytering och pyroptos skulle potentiellt kunna dämpa den värsta hjärnskadan samtidigt som antivirala försvar får verka.
Citering: Ou, Z., Wang, Z., Chen, Q. et al. Spatial transcriptomics uncovers vasculature-centered cellular interactions driving Japanese encephalitis progression in a mouse model. Nat Commun 17, 4089 (2026). https://doi.org/10.1038/s41467-026-70047-5
Nyckelord: Japansk encefalit, hjärn inflammation, blod–hjärnbarriär, monocyter, spatial transkriptomik