Clear Sky Science · pt
Transcriptômica espacial revela interações celulares centradas na vasculatura que impulsionam a progressão da encefalite japonesa em um modelo de camundongo
Por que este estudo sobre infecção cerebral é importante
A encefalite japonesa é uma infecção cerebral transmitida por mosquitos que pode deixar sobreviventes com problemas permanentes de movimento e memória, especialmente crianças. Ainda assim, os médicos não dispõem de medicamentos que atuem diretamente contra o vírus ou contra a inflamação danosa que ele desencadeia no cérebro. Este estudo usa uma tecnologia de mapeamento poderosa para observar, quase célula a célula, como o vírus e as próprias células imunes do corpo se movem pelo cérebro de camundongos. Ao fazê-lo, revela uma parceria surpreendente entre vasos sanguíneos e células imunes migratórias que ajuda a explicar por que a doença se torna tão destrutiva.
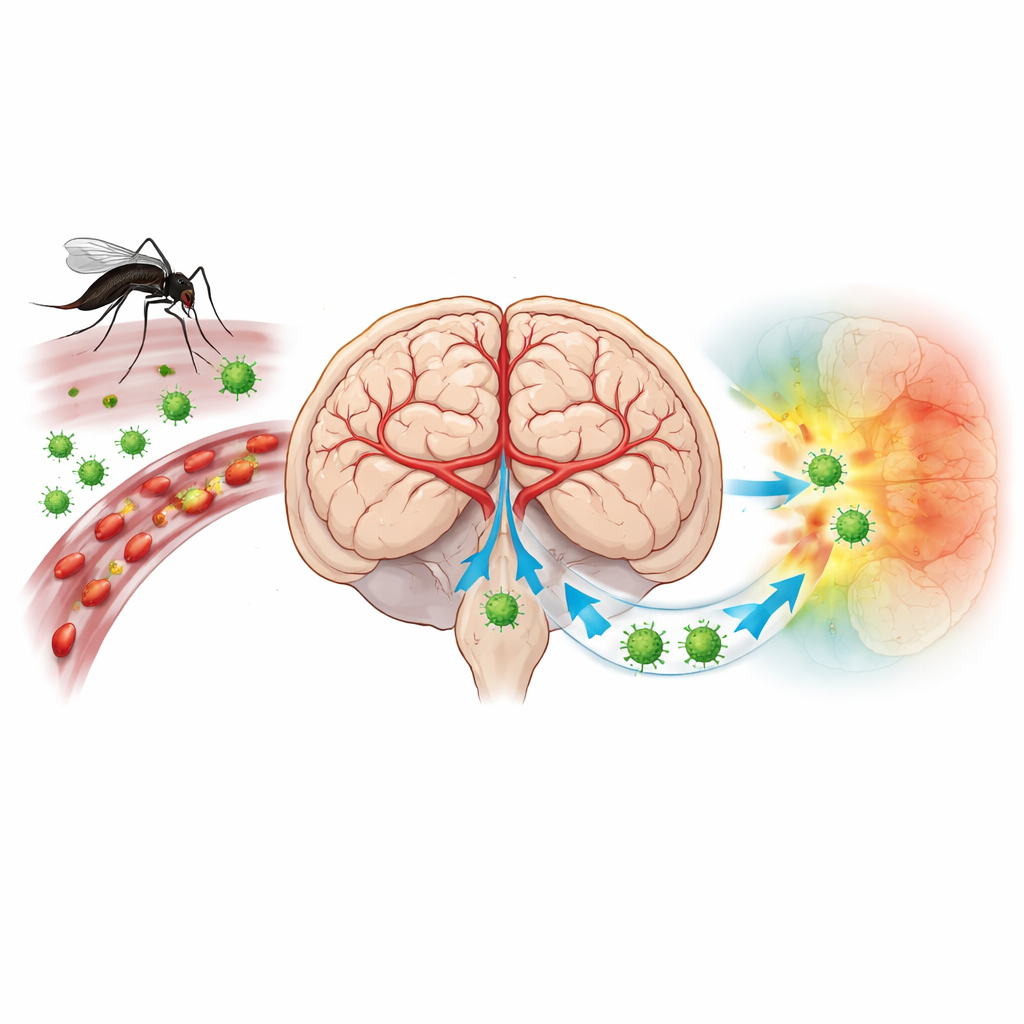
Um vírus que volta as defesas do cérebro contra si mesmo
O vírus da encefalite japonesa (JEV) é transmitido por mosquitos e ameaça mais de três bilhões de pessoas na Ásia e no Pacífico Ocidental. A maioria das infecções é assintomática, mas quando o vírus atinge o cérebro pode causar febre alta, convulsões e coma. Vacinas reduzem o risco, mas muitas pessoas continuam desprotegidas, e não existe tratamento antiviral específico. Cientistas há muito suspeitam que a forma como células imunes entram no cérebro e como interagem com os vasos sanguíneos cerebrais é central para a doença. No entanto, métodos tradicionais não conseguiam mostrar facilmente quais células exatas estavam infectadas e como elas se organizavam na delicada arquitetura cerebral.
Um mapa molecular da infecção no espaço e no tempo
Os pesquisadores infectaram camundongos fêmeas com JEV e examinaram seus cérebros nos dias 3, 5 e 7 após a infecção, cobrindo o aumento dos níveis virais e o início dos sintomas graves. Eles usaram uma tecnologia chamada transcriptômica espacial, que lê quais genes estão ativos em milhares de pontos minúsculos por uma fina fatia cerebral, preservando a posição de cada ponto no tecido. Sondas customizadas permitiram detectar tanto RNA do camundongo quanto do vírus na mesma lâmina. Ao combinar esses mapas com atlas cerebrais e referências de tipos celulares, construíram um atlas espaço-temporal: quais regiões do cérebro o vírus prefere, quais tipos celulares ele infecta e como as respostas imunes locais se desenrolam.
Vasos sanguíneos como portões e amplificadores
O atlas mostrou que o JEV aparece inicialmente em uma pequena fração do tecido cerebral e depois se expande para envolver fortemente o tálamo e o córtex cerebral. Ainda mais marcante foi onde os sinais imunes mais fortes surgiram: ao longo dos vasos sanguíneos, especialmente nas membranas finas (meninges) que envolvem o cérebro e no plexo coróide, um tecido que ajuda a produzir o líquido cefalorraquidiano. Ali, um subtipo especial de células endoteliais — células que revestem os vasos — marcado por um receptor chamado Ackr1 ficou altamente ativado. Essas células produziram muitas quimiocinas, moléculas que atraem células imunes, e ativaram genes ligados à inflamação enquanto reduziam genes que mantêm as uniões apertadas, os selos que preservam a integridade da barreira hematoencefálica. Ao mesmo tempo, testes com um corante confirmaram que a barreira de fato havia se tornado permeável.
Monócitos: cavalos de Troia e amplificadores de sinal
Entre todas as células imunes que entram no cérebro, uma se destacou: uma população de monócitos Ly6c2-positivos. Mapas espaciais e citometria de fluxo mostraram que essas células frequentemente estavam infectadas com JEV, tornando-as prováveis transportadoras que levam o vírus através de vasos danificados para o interior do cérebro — muito parecido com um cavalo de Troia. Elas fizeram mais do que transportar o vírus. Esses monócitos produziram grandes quantidades de interferon-gama, uma potente molécula sinalizadora imune normalmente associada a células T e células natural killer. O interferon-gama é conhecido por ajudar a eliminar vírus, mas também por agravar danos na barreira hematoencefálica. O estudo encontrou que monócitos se agrupavam perto de células endoteliais Ackr1-positivas e se comunicavam com elas por meio de múltiplas quimiocinas, formando um circuito de retroalimentação que atraía ainda mais células imunes. Ao redor desses vasos, muitas células — incluindo os próprios monócitos — exibiam assinaturas moleculares de formas explosivas de morte celular (piropoptose e necroptose) que derramam conteúdos inflamatórios no tecido circundante.
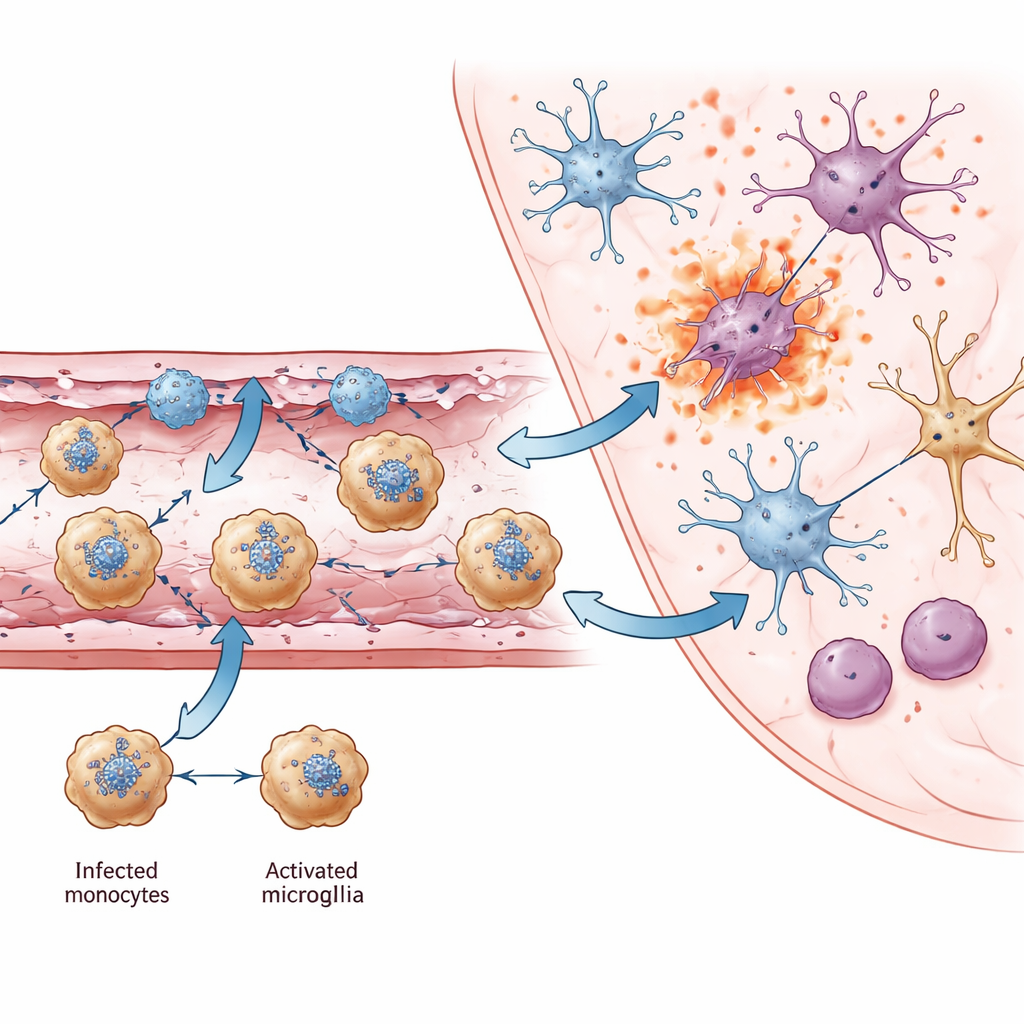
Do dano vascular local à lesão cerebral generalizada
À medida que a infecção progrediu, células residentes do cérebro também mudaram. Microglia, os vigilantes da imunidade inata cerebral, passaram para um estado ativado marcado por uma quimiocina chamada Ccl12 e por forte atividade de genes antivirais. Embora essas mudanças ajudem a combater o vírus, também coincidiram com a perda de genes envolvidos em sinapses, aprendizagem e memória. Em regiões fortemente infectadas, como o tálamo, diferentes subtipos neuronais que testaram positivo para RNA viral mostraram sinais aumentados de piropoptose e necroptose, apontando para a morte celular inflamatória como uma causa-chave da perda neuronal. Em múltiplas regiões cerebrais, os autores identificaram genes neuronais comuns cuja redução de atividade também foi associada a problemas cognitivos e motores em outras doenças cerebrais, sugerindo uma base molecular compartilhada para as deficiências de longo prazo observadas em sobreviventes.
O que isso significa para tratamentos futuros
Para um leitor leigo, a mensagem central é que a encefalite japonesa não é apenas uma história de um vírus atacando neurônios. É também a história de monócitos infectados e de células vasculares especializadas formando uma aliança danosa nas fronteiras do cérebro. Juntos, eles afrouxam a barreira hematoencefálica, atraem ondas de células imunes e desencadeiam formas inflamatórias de morte celular que se irradiam dos vasos para o tecido cerebral. Ao identificar esses atores-chave — monócitos Ly6c2-positivos e células endoteliais Ackr1-positivas — o estudo sugere novas abordagens terapêuticas: drogas que reduzam quimiocinas específicas, bloqueiem o receptor Ackr1 ou limitem o recrutamento de monócitos e a piropoptose poderiam, potencialmente, atenuar os piores danos cerebrais enquanto permitem que as defesas antivirais atuem.
Citação: Ou, Z., Wang, Z., Chen, Q. et al. Spatial transcriptomics uncovers vasculature-centered cellular interactions driving Japanese encephalitis progression in a mouse model. Nat Commun 17, 4089 (2026). https://doi.org/10.1038/s41467-026-70047-5
Palavras-chave: encefalite japonesa, inflamação cerebral, barreira hematoencefálica, monócitos, transcriptômica espacial