Clear Sky Science · pl
Transkryptomika przestrzenna ujawnia ośrodkowe wokół naczyń interakcje komórkowe napędzające postęp zapalenia mózgu japońskiego w modelu myszy
Dlaczego to badanie zakażenia mózgu ma znaczenie
Zapalenie mózgu japońskie przenoszone przez komary może pozostawić osoby ocalone z dożywotnimi problemami ruchowymi i z pamięcią, zwłaszcza u dzieci. Mimo to lekarze wciąż nie dysponują lekami bezpośrednio celującymi wirusa ani szkodliwych reakcji zapalnych w mózgu. W tym badaniu wykorzystano potężną technologię mapowania, aby obserwować niemal komórka po komórce, jak wirus i własne komórki układu odpornościowego przemieszczają się w mózgu myszy. Dzięki temu ujawniono zaskakujące współdziałanie między naczyniami krwionośnymi a wędrującymi komórkami odpornościowymi, które pomaga wyjaśnić, jak choroba staje się tak destrukcyjna.
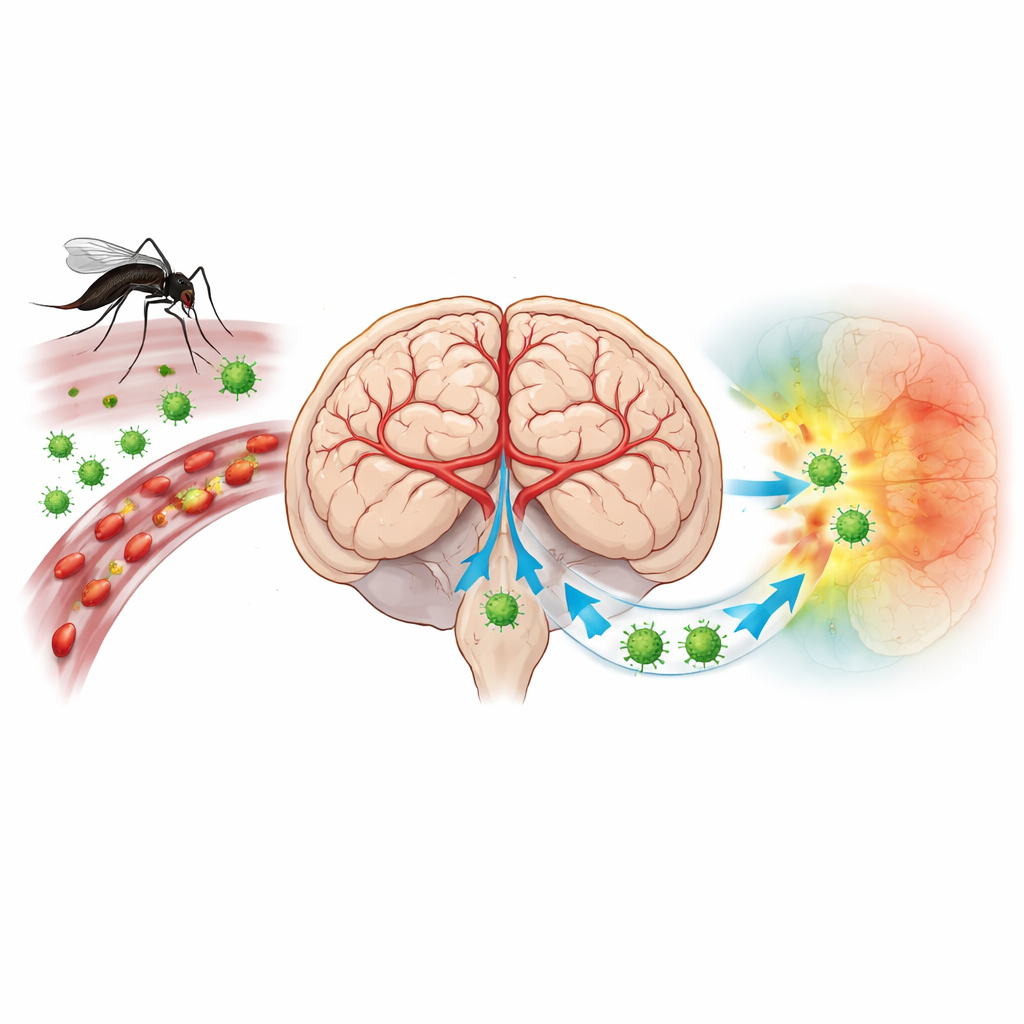
Wirus, który obróci obronę mózgu przeciwko niemu
Wirus zapalenia mózgu japońskiego (JEV) przenoszony jest przez komary i zagraża ponad trzem miliardom ludzi w Azji i regionie Zachodniego Pacyfiku. Większość zakażeń przebiega bezobjawowo, ale gdy wirus dociera do mózgu, może wywołać wysoką gorączkę, drgawki i śpiączkę. Szczepienia zmniejszają ryzyko, ale wiele osób nadal nie jest chronionych, a brak jest specyficznego leczenia przeciwwirusowego. Naukowcy od dawna podejrzewają, że to, w jaki sposób komórki odpornościowe wchodzą do mózgu i jak wchodzą w interakcje z naczyniami mózgu, jest kluczowe dla choroby. Jednak tradycyjne metody nie pozwalały łatwo pokazać, które dokładnie komórki były zakażone i jak były rozmieszczone w delikatnej architekturze mózgu.
Molekularna mapa zakażenia w przestrzeni i czasie
Naukowcy zakażili samice myszy JEV i badali ich mózgi w dniach 3., 5. i 7. po zakażeniu, obejmując wzrost poziomów wirusa i pojawienie się ciężkich objawów. Użyli technologii zwanej transkryptomiką przestrzenną, która odczytuje, które geny są aktywne w tysiącach drobnych punktów na cienkim skrawku mózgu, zachowując jednocześnie informacje o położeniu każdego punktu w tkance. Niestandardowe sondy pozwoliły wykryć zarówno RNA myszy, jak i wirusa na tym samym preparacie. Łącząc te mapy z atlasami mózgu i referencjami typów komórek, zbudowali atlas czasoprzestrzenny: które obszary mózgu wirus preferuje, które typy komórek zakaża i jak rozwijają się miejscowe reakcje odpornościowe.
Naczynia krwionośne jako bramy i wzmacniacze
Atlas pokazał, że JEV najpierw pojawia się w niewielkiej części tkanki mózgowej, po czym rozszerza się, silnie angażując wzgórze i korę mózgową. Jeszcze bardziej uderzające było to, gdzie pojawiały się najsilniejsze sygnały odpornościowe: wzdłuż naczyń krwionośnych, szczególnie w cienkich błonach (oponach) otaczających mózg oraz w splotach naczyniówkowych, tkance uczestniczącej w produkcji płynu mózgowo-rdzeniowego. W tych miejscach wyspecjalizowany podtyp komórek śródbłonka — komórki wyściełające naczynia — oznaczony receptorem o nazwie Ackr1 wykazywał silną aktywację. Komórki te produkowały wiele chemokin przyciągających komórki odpornościowe oraz włączały geny związane z zapaleniem, jednocześnie wyciszając geny utrzymujące połączenia ścisłe, uszczelniające barierę krew–mózg. Równocześnie testy z użyciem barwnika potwierdziły, że bariera stała się rzeczywiście przeciekająca.
Monocyty: koniki trojańskie i wzmacniacze sygnału
Wśród wszystkich komórek odpornościowych wchodzących do mózgu wyróżniała się jedna populacja: monocyty pozytywne dla Ly6c2. Mapy przestrzenne i cytometria przepływowa wykazały, że te komórki często były zakażone JEV, co czyni je prawdopodobnymi nosicielami transportującymi wirusa przez uszkodzone naczynia do mózgu — niczym koń trojański. Robiły one więcej niż tylko przewoziły wirusa. Monocyty te produkowały duże ilości interferonu gamma, silnego przekaźnika immunologicznego zwykle kojarzonego z limfocytami T i komórkami NK. Interferon gamma pomaga usuwać wirusy, lecz także nasila uszkodzenia bariery krew–mózg. Badanie wykazało, że monocyty skupiały się w pobliżu śródbłonka Ackr1-pozytywnego i komunikowały się z nim poprzez liczne chemokiny, tworząc pętlę sprzężenia zwrotnego, która przyciągała kolejne komórki odpornościowe. Wokół tych naczyń wiele komórek — w tym same monocyty — wykazywało molekularne sygnatury wybuchowych form śmierci komórkowej (piroptoza i nekroptoza), które wypuszczają zapalne składniki do otaczającej tkanki.
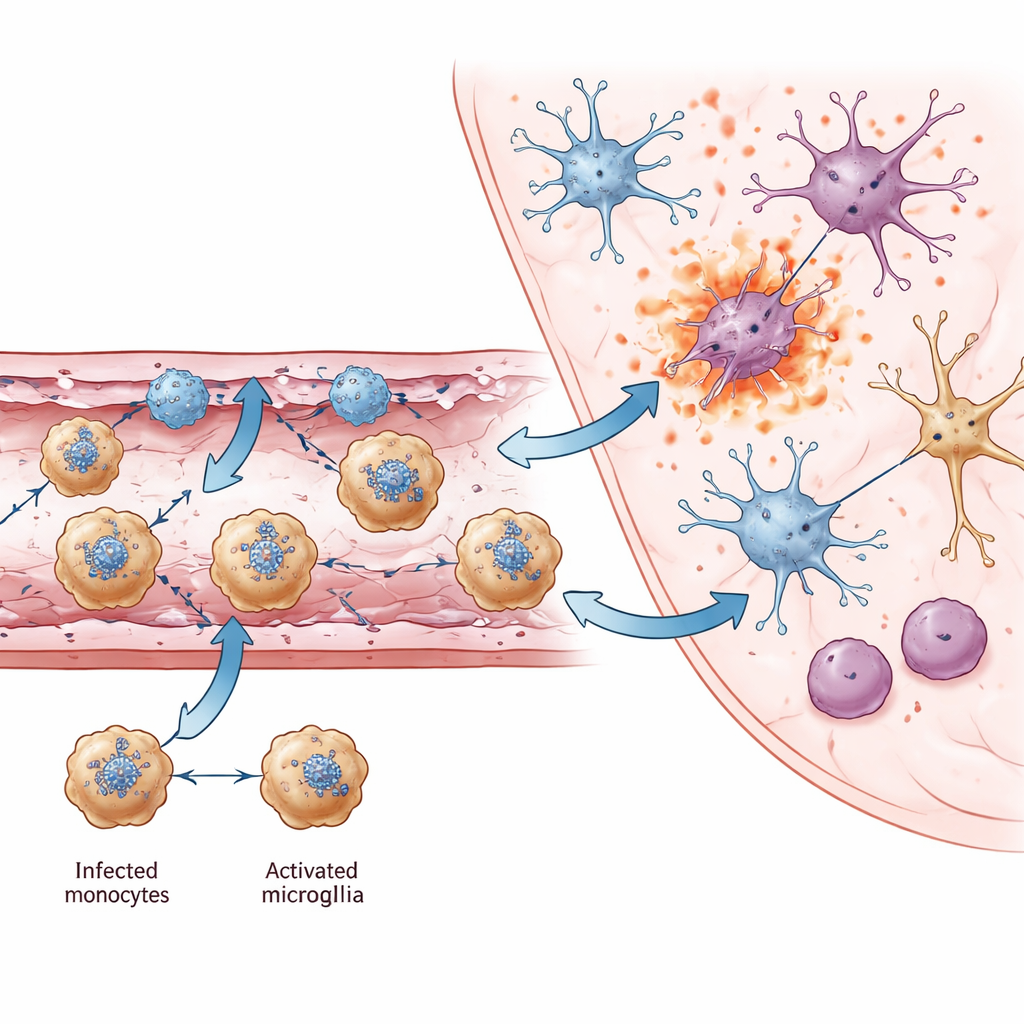
Od miejscowego uszkodzenia naczyń do rozległego urazu mózgu
W miarę postępu zakażenia zmieniały się także komórki rezydujące w mózgu. Mikroglej, wrodzeni strażnicy odpornościowe mózgu, przeszedł w stan aktywacji oznaczony chemokiną Ccl12 i silną aktywnością genów przeciwwirusowych. Chociaż te zmiany pomagają zwalczać wirusa, zbiegały się one z utratą ekspresji genów zaangażowanych w synapsy, uczenie się i pamięć. W silnie zakażonych obszarach, takich jak wzgórze, różne podtypy neuronów pozytywnych pod kątem RNA wirusa wykazywały podwyższone sygnały piroptozy i nekroptozy, wskazując na zapalną śmierć komórek jako kluczową przyczynę utraty neuronów. W wielu regionach mózgu autorzy zidentyfikowali wspólne geny neuronalne, których obniżona aktywność była również powiązana z problemami poznawczymi i ruchowymi w innych chorobach mózgu, sugerując wspólną molekularną podstawę długoterminowych niepełnosprawności obserwowanych u ocalałych.
Co to oznacza dla przyszłych terapii
Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że zapalenie mózgu japońskie to nie tylko historia wirusa atakującego neurony. To także opowieść o zakażonych monocytach i wyspecjalizowanych komórkach naczyń krwionośnych tworzących szkodliwy sojusz na granicach mózgu. Razem rozluźniają barierę krew–mózg, przyciągają fale komórek odpornościowych i wywołują zapalne formy śmierci komórkowej, które rozchodzą się od naczyń do tkanki mózgowej. Wskazując na tych kluczowych aktorów — monocyty Ly6c2-dodatnie i śródbłonek Ackr1-dodatni — badanie sugeruje nowe strategie terapeutyczne: leki redukujące konkretne chemokiny, blokujące receptor Ackr1 lub ograniczające rekrutację monocytów i piroptozę mogłyby potencjalnie złagodzić najsilniejsze uszkodzenia mózgu, pozwalając jednocześnie działaniu mechanizmów przeciwwirusowych.
Cytowanie: Ou, Z., Wang, Z., Chen, Q. et al. Spatial transcriptomics uncovers vasculature-centered cellular interactions driving Japanese encephalitis progression in a mouse model. Nat Commun 17, 4089 (2026). https://doi.org/10.1038/s41467-026-70047-5
Słowa kluczowe: zapalenie mózgu japońskie, zapalenie mózgu, bariera krew–mózg, monocyty, transkryptomika przestrzenna