Clear Sky Science · de
Räumliche Transkriptomik enthüllt vaskulär-zentrierte Zellinteraktionen, die den Verlauf der japanischen Enzephalitis in einem Mausmodell antreiben
Warum diese Studie zur Hirninfektion wichtig ist
Die japanische Enzephalitis ist eine durch Mücken übertragene Hirninfektion, die Überlebende, insbesondere Kinder, mit lebenslangen Bewegungs- und Gedächtnisstörungen zurücklassen kann. Dennoch fehlen Ärzten bislang Medikamente, die direkt das Virus oder die schädliche Entzündung im Gehirn bekämpfen. Diese Studie nutzt eine leistungsfähige Kartierungstechnologie, um nahezu zellgenau zu verfolgen, wie sich das Virus und die körpereigenen Immunzellen durch das Mausgehirn bewegen. Dadurch zeigt sie eine überraschende Zusammenarbeit zwischen Blutgefäßen und umherwandernden Immunzellen, die erklärt, warum die Krankheit so zerstörerisch werden kann.
Ein Virus, das die Abwehr des Gehirns gegen sich selbst kehrt
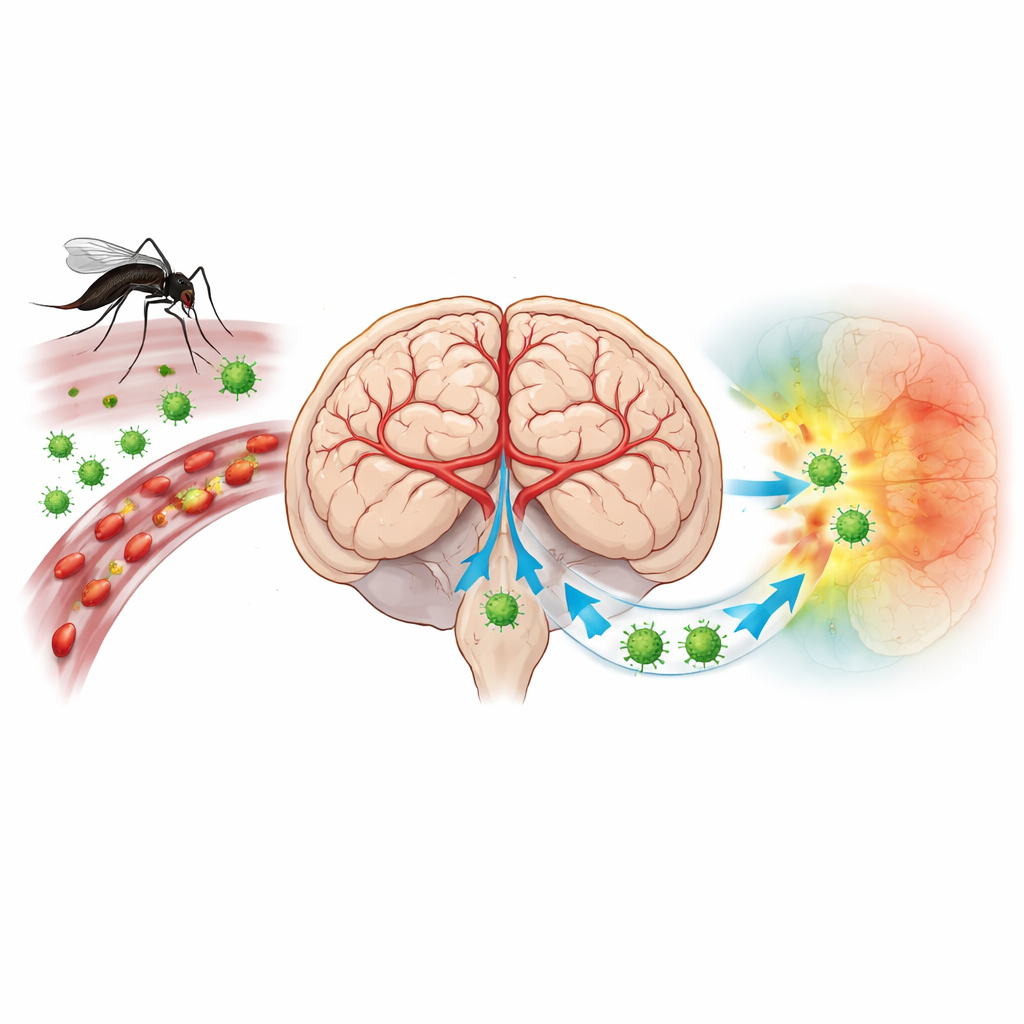
Das Japanische-Enzephalitis-Virus (JEV) wird von Mücken übertragen und bedroht mehr als drei Milliarden Menschen in Asien und dem westlichen Pazifikraum. Die meisten Infektionen verlaufen ohne Symptome, doch sobald das Virus das Gehirn erreicht, kann es hohes Fieber, Krampfanfälle und Koma auslösen. Impfstoffe verringern das Risiko, doch viele Menschen sind weiterhin ungeschützt, und es gibt keine spezifische antivirale Therapie. Wissenschaftler vermuteten schon lange, dass die Art und Weise, wie Immunzellen ins Gehirn gelangen und wie sie mit den Blutgefäßen des Gehirns interagieren, zentral für die Erkrankung ist. Traditionelle Methoden konnten jedoch kaum exakt zeigen, welche Zellen infiziert sind und wie sie in der feinen Architektur des Gehirns angeordnet sind.
Eine molekulare Karte der Infektion in Raum und Zeit
Die Forscher infizierten weibliche Mäuse mit JEV und untersuchten ihre Gehirne an den Tagen 3, 5 und 7 nach der Infektion, also während des Anstiegs der Viruslast und dem Einsetzen schwerer Symptome. Sie verwendeten eine Technologie namens räumliche Transkriptomik, die auftausend kleinen Punkten in einem dünnen Hirnschnitt abliest, welche Gene aktiv sind, während die Lage jedes Punktes im Gewebe erhalten bleibt. Maßgeschneiderte Sonden ermöglichten es, sowohl Maus- als auch Virus-RNA auf derselben Probe nachzuweisen. Durch die Kombination dieser Karten mit Hirnatlanten und Zelltyp-Referenzen stellten sie ein spatiotemporales Atlas zusammen: welche Hirnregionen das Virus bevorzugt, welche Zelltypen es infiziert und wie sich lokale Immunantworten entfalten.
Blutgefäße als Tore und Verstärker
Der Atlas zeigte, dass JEV zunächst in einem kleinen Bruchteil des Hirngewebes auftaucht und sich dann stark auf Thalamus und Kortex ausweitet. Noch auffälliger war, wo die stärksten Immunreaktionen auftraten: entlang von Blutgefäßen, besonders in den dünnen Häuten (Meningen), die das Gehirn umgeben, und im Plexus chorioideus, einem Gewebe, das die Liquorflüssigkeit mitbildet. Hier wurde ein spezieller Endothelzell‑Subtyp — Zellen, die Blutgefäße auskleiden — markiert durch den Rezeptor Ackr1, besonders stark aktiviert. Diese Zellen produzierten viele Chemokine, Moleküle, die Immunzellen anziehen, und schalteten Gene hoch, die mit Entzündung verbunden sind, während sie Gene herunterfuhren, die für die Aufrechterhaltung dichter Zellverbindungen (tight junctions) verantwortlich sind, also der Dichtung der Blut‑Hirn‑Schranke. Zeitgleich bestätigten Färbetests, dass die Schranke tatsächlich undicht geworden war.
Monozyten: trojanische Pferde und Signalverstärker
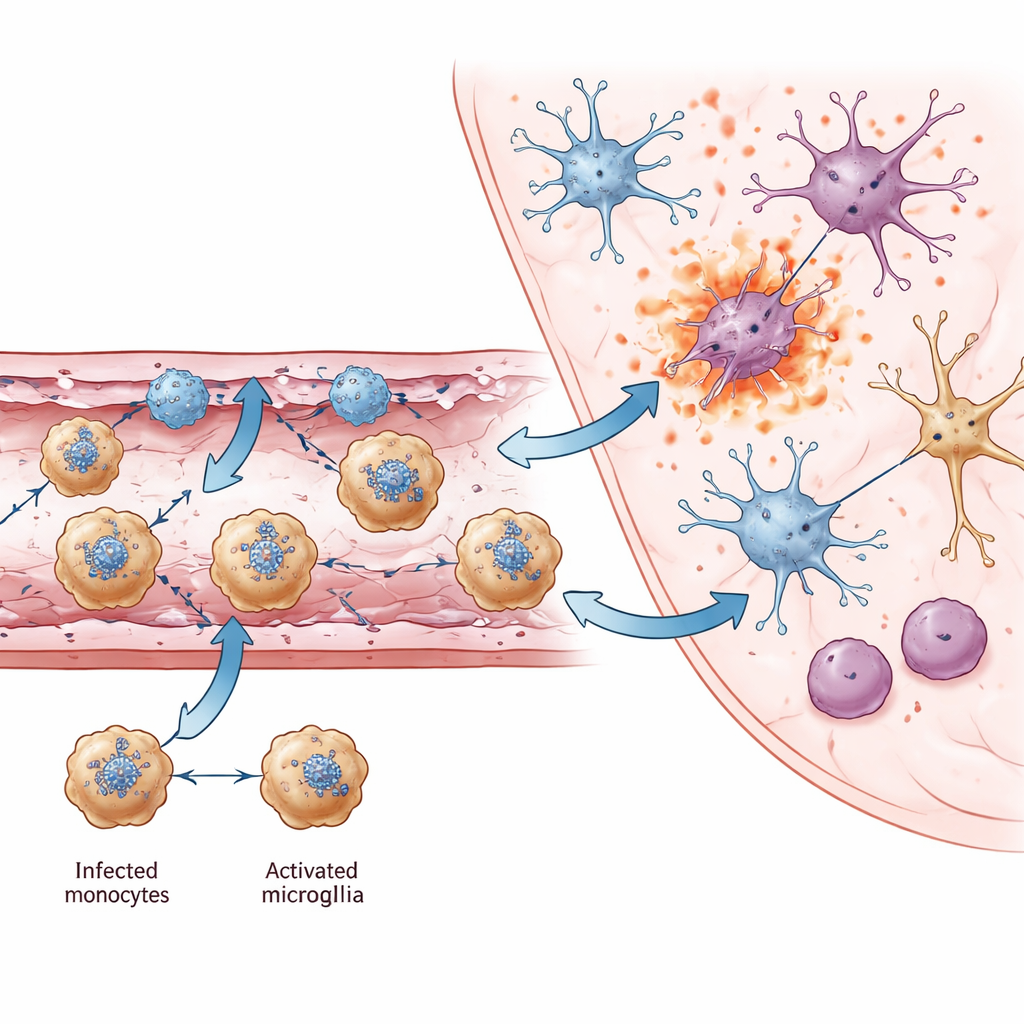
Unter allen in das Gehirn einströmenden Immunzellen stach eine Population hervor: Ly6c2-positive Monozyten. Räumliche Karten und Durchflusszytometrie zeigten, dass diese Zellen häufig mit JEV infiziert waren, was sie zu wahrscheinlichen Überträgern macht, die das Virus über beschädigte Gefäße ins Gehirn schleusen — ähnlich einem trojanischen Pferd. Sie transportierten nicht nur das Virus: Diese Monozyten produzierten große Mengen Interferon‑gamma, einen starken Immunbotenstoff, der üblicherweise mit T‑Zellen und natürlichen Killerzellen assoziiert ist. Interferon‑gamma kann bei der Virusbeseitigung helfen, verschlechtert aber auch die Schädigung der Blut‑Hirn‑Schranke. Die Studie fand, dass Monozyten sich nahe Ackr1-positiven Endothelzellen ansammelten und über mehrere Chemokine mit ihnen kommunizierten, wodurch eine Rückkopplungsschleife entstand, die noch mehr Immunzellen anzog. Um diese Gefäße zeigten viele Zellen — darunter auch die Monozyten selbst — molekulare Signaturen explosionsartiger Formen des Zelltods (Pyroptose und Nekroptose), die entzündliche Inhalte in das umgebende Gewebe freisetzen.
Von lokalem vaskulären Schaden zu weitreichender Hirnschädigung
Mit dem Fortschreiten der Infektion veränderten sich auch die residenten Gehirnzellen. Mikroglia, die angeborenen Immunwächter des Gehirns, wechselten in einen aktivierten Zustand, gekennzeichnet durch das Chemokin Ccl12 und eine starke antivirale Genaktivität. Während diese Veränderungen bei der Bekämpfung des Virus helfen, gingen sie zugleich mit einem Verlust von Genen einher, die an Synapsen, Lernen und Gedächtnis beteiligt sind. In stark infizierten Regionen wie dem Thalamus zeigten verschiedene virale RNA‑positive Neuronenuntertypen verstärkte Signale von Pyroptose und Nekroptose, was darauf hindeutet, dass entzündlicher Zelltod ein zentraler Grund für Neuronenverlust ist. In mehreren Hirnregionen identifizierten die Autoren gemeinsame neuronale Gene, deren verminderte Aktivität auch mit kognitiven und motorischen Problemen bei anderen Hirnerkrankungen in Verbindung gebracht wurde, was auf eine gemeinsame molekulare Grundlage für die langfristigen Behinderungen bei Überlebenden hinweist.
Was das für künftige Therapien bedeutet
Für eine allgemein interessierte Leserschaft ist die Kernbotschaft: Die japanische Enzephalitis ist nicht nur die Geschichte eines Virus, das Neuronen angreift. Sie ist auch die Geschichte infizierter Monozyten und spezialisierter Gefäßzellen, die an den Rändern des Gehirns eine schädliche Allianz bilden. Gemeinsam lockern sie die Blut‑Hirn‑Schranke, ziehen Wellen von Immunzellen an und lösen entzündliche Todesformen aus, die sich von den Gefäßen ins Hirngewebe ausbreiten. Indem die Studie diese Schlüsselakteure — Ly6c2-positive Monozyten und Ackr1-positive Endothelzellen — identifiziert, legt sie neue therapeutische Ansätze nahe: Wirkstoffe, die spezifische Chemokine reduzieren, den Ackr1‑Rezeptor blockieren oder die Monozytenrekrutierung und Pyroptose begrenzen, könnten das schlimmste Ausmaß der Hirnschädigung abschwächen und zugleich antivirale Abwehrmechanismen erhalten.
Zitation: Ou, Z., Wang, Z., Chen, Q. et al. Spatial transcriptomics uncovers vasculature-centered cellular interactions driving Japanese encephalitis progression in a mouse model. Nat Commun 17, 4089 (2026). https://doi.org/10.1038/s41467-026-70047-5
Schlüsselwörter: Japanische Enzephalitis, Gehirnentzündung, Blut-Hirn-Schranke, Monozyten, räumliche Transkriptomik