Clear Sky Science · nl
Ruimtelijke transcriptomica onthult vasculatuur-centrische cellulaire interacties die de progressie van Japanse encefalitis in een muismodel aandrijven
Waarom deze studie naar herseninfecties ertoe doet
Japanse encefalitis is een door muggen overgedragen herseninfectie die overlevenden, vooral kinderen, levenslange bewegings- en geheugenproblemen kan bezorgen. Toch ontbreken artsen nog steeds medicijnen die rechtstreeks het virus of de schadelijke ontsteking in de hersenen aanpakken. Deze studie gebruikt een krachtige kaarttechnologie om bijna cel voor cel te volgen hoe het virus en de eigen immuuncellen van het lichaam zich door de muizenhersenen verplaatsen. Daarmee onthult ze een verrassende samenwerking tussen bloedvaten en rondzwervende immuuncellen die helpt verklaren waarom de ziekte zo destructief wordt.
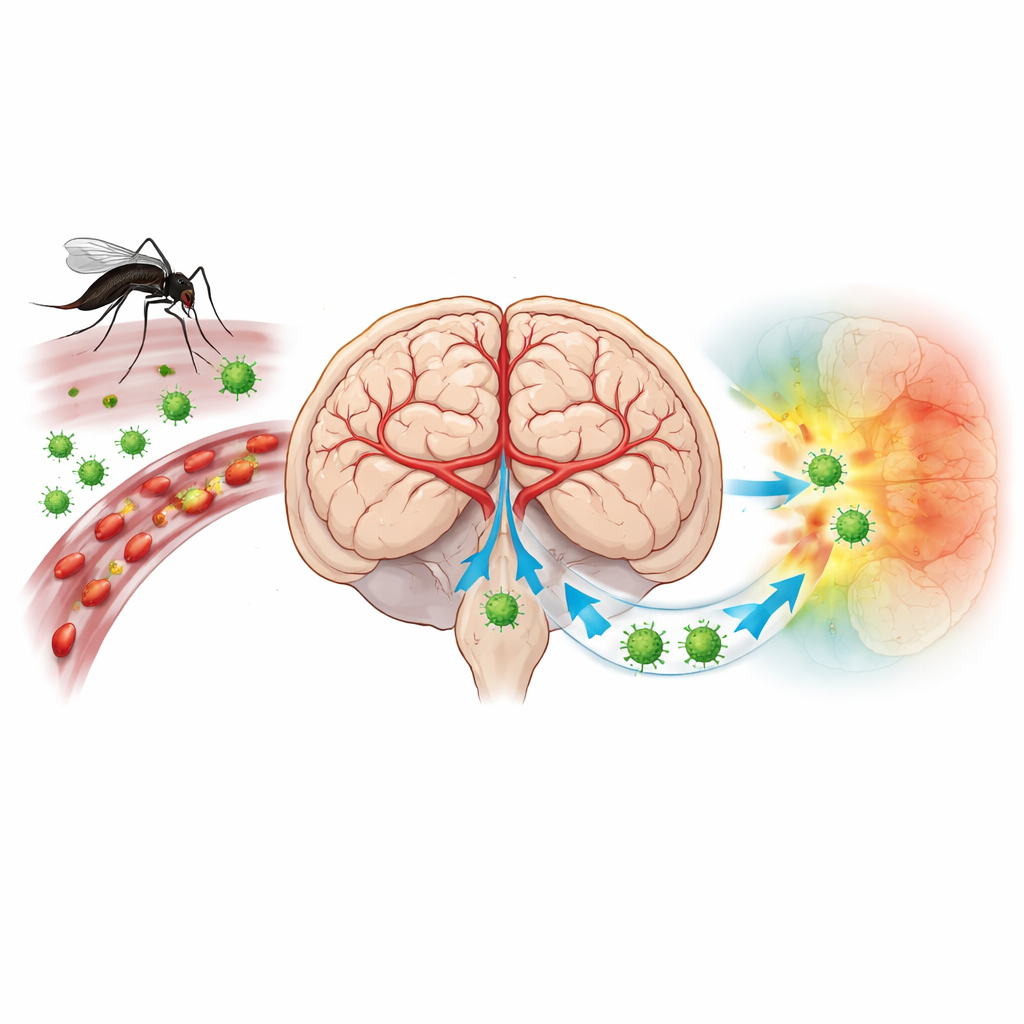
Een virus dat de verdediging van de hersenen tegen zichzelf keert
Het Japanse encefalitisvirus (JEV) wordt door muggen overgedragen en bedreigt meer dan drie miljard mensen in Azië en de Westelijke Stille Oceaan. De meeste infecties verlopen zonder symptomen, maar wanneer het virus de hersenen bereikt kan het hoge koorts, aanvallen en coma veroorzaken. Vaccins verkleinen het risico, maar veel mensen blijven onbeschermd en er is geen specifieke antivirale behandeling. Wetenschappers vermoeden al langer dat de manier waarop immuuncellen de hersenen binnenkomen en hoe ze samenwerken met hersenbloedvaten centraal staat in de ziekte. Traditionele methoden konden echter niet eenvoudig aantonen welke exacte cellen geïnfecteerd waren en hoe ze gerangschikt waren in de fragiele architectuur van de hersenen.
Een moleculaire kaart van infectie in ruimte en tijd
De onderzoekers infecteerden vrouwelijke muizen met JEV en onderzochten hun hersenen op dag 3, 5 en 7 na infectie, waarmee ze de stijging van virusniveaus en het begin van ernstige symptomen besloegen. Ze gebruikten een technologie genaamd ruimtelijke transcriptomica, die afleest welke genen actief zijn op duizenden kleine punten over een dunne hersenplaat, terwijl de locatie van elk punt in het weefsel behouden blijft. Aangepaste sondes stelden hen in staat zowel muis- als viraal RNA op hetzelfde preparaat te detecteren. Door deze kaarten te combineren met hersenatlassen en celtype-referenties bouwden ze een spatiotemporaal atlas: welke hersengebieden het virus prefereert, welke celtypen het infecteren, en hoe lokale immuunreacties zich ontvouwen.
Bloedvaten als poorten en versterkers
De atlas toonde dat JEV eerst in een klein deel van het hersenweefsel verschijnt en vervolgens uitbreidt naar een sterke betrokkenheid van de thalamus en de hersenschors. Nog opvallender was waar de sterkste immuunsignalen opdoken: langs bloedvaten, vooral in de dunne membranen (meninges) die de hersenen omhullen en in het plexus choroideus, weefsel dat helpt bij de aanmaak van hersenvocht. Hier raakte een speciaal subtype endotheelcellen—de cellen die bloedvaten bekleden—gemarkeerd door een receptor genaamd Ackr1 sterk geactiveerd. Deze cellen produceerden veel chemokinen, moleculen die immuuncellen aantrekken, en zetten genen aan die met ontsteking te maken hebben terwijl ze genen uitschakelden die de nauwe verbindingen (tight junctions) onderhouden, de afdichtingen die de bloed-hersenbarrière intact houden. Tegelijkertijd bevestigden testen met een kleurstof dat de barrière inderdaad lekkend was geworden.
Monocyten: Trojaanse paarden en signaalversterkers
Onder alle immuuncellen die de hersenen binnendringen stak er één bovenuit: een populatie Ly6c2-positieve monocyten. Ruimtelijke kaarten en flowcytometrie toonden dat deze cellen vaak door JEV waren geïnfecteerd, waardoor ze waarschijnlijk dragers zijn die het virus via beschadigde vaten de hersenen in vervoeren—vergelijkbaar met een Trojaans paard. Ze deden meer dan alleen het virus transporteren. Deze monocyten produceerden grote hoeveelheden interferon-gamma, een krachtig immuunboodschapper die meestal aan T-cellen en natural killer-cellen wordt toegeschreven. Interferon-gamma helpt weliswaar virussen opruimen, maar verslechtert ook beschadiging van de bloed-hersenbarrière. De studie vond dat monocyten zich clusteren nabij Ackr1-positieve endotheelcellen en met hen communiceren via meerdere chemokinen, waarmee een feedbacklus ontstaat die nog meer immuuncellen aantrekt. Rond deze vaten vertoonden veel cellen—including monocyten zelf—moleculaire kenmerken van explosieve vormen van celdood (pyroptose en necroptose) die ontstekingsinhoud in het omliggende weefsel sproeien.
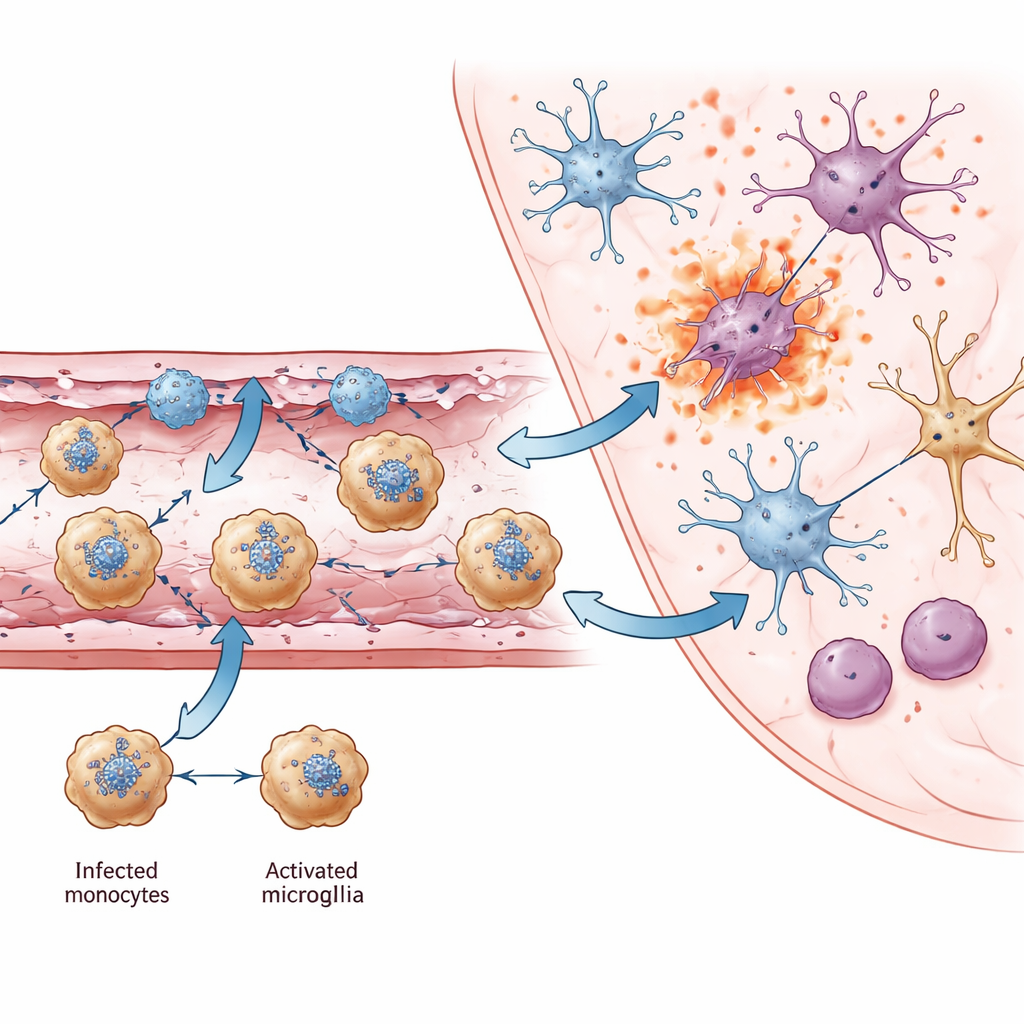
Van lokale vasculaire schade naar wijdverspreide hersenbeschadiging
Naarmate de infectie vorderde veranderden ook residente hersencellen. Microglia, de aangeboren immuunwachters van de hersenen, schakelden over naar een geactiveerde toestand gekenmerkt door een chemokine genaamd Ccl12 en door sterke antivirale genactiviteit. Hoewel deze veranderingen helpen het virus te bestrijden, gingen ze ook samen met verlies van genen die betrokken zijn bij synapsen, leren en geheugen. In sterk geïnfecteerde regio’s zoals de thalamus vertoonden verschillende neurontypes die positief testten voor viraal RNA verhoogde signalen van pyroptose en necroptose, wat wijst op inflammatoire celdood als een belangrijke oorzaak van neuronverlies. In meerdere hersengebieden identificeerden de auteurs gemeenschappelijke neuronaire genen waarvan verminderde activiteit ook gerelateerd is aan cognitieve en motorische problemen bij andere hersenaandoeningen, wat wijst op een gedeelde moleculaire basis voor de langdurige beperkingen bij overlevenden.
Wat dit betekent voor toekomstige behandelingen
Voor een lezer zonder vakachtergrond is de kernboodschap dat Japanse encefalitis niet alleen het verhaal is van een virus dat neuronen aanvalt. Het is ook het verhaal van geïnfecteerde monocyten en gespecialiseerde bloedvatcellen die aan de grenzen van de hersenen een schadelijk verbond vormen. Samen verslappen ze de bloed-hersenbarrière, lokken ze golven van immuuncellen en veroorzaken ze inflammatoire vormen van celdood die vanuit vaten in het hersenweefsel uitstralen. Door deze sleutelfiguren—Ly6c2-positieve monocyten en Ackr1-positieve endotheelcellen—aan te wijzen, suggereert de studie nieuwe therapeutische invalshoeken: medicijnen die specifieke chemokinen verminderen, de Ackr1-receptor blokkeren of de aanvoer van monocyten en pyroptose beperken, zouden mogelijk de ergste hersenschade kunnen afremmen terwijl antivirale afweer in stand blijft.
Bronvermelding: Ou, Z., Wang, Z., Chen, Q. et al. Spatial transcriptomics uncovers vasculature-centered cellular interactions driving Japanese encephalitis progression in a mouse model. Nat Commun 17, 4089 (2026). https://doi.org/10.1038/s41467-026-70047-5
Trefwoorden: Japanse encefalitis, hersenontsteking, bloed-hersenbarrière, monocyten, ruimtelijke transcriptomica