Clear Sky Science · zh
来自雄性小鼠的造血干细胞表观遗传谱鉴定出KDR和PU.1为衰老转录组与热量限制反应的调控因子
为什么少吃可能会重塑我们的血液
不致营养不良的热量限制已被证明能延长许多动物的寿命,有些人甚至为了活得更久而采取严格的饮食。但少吃也会削弱免疫系统。本研究提出了一个简单而重要的问题:长期减少热量如何改变骨髓中不断重建我们血液和免疫系统的干细胞?这些变化能否在保护机体的同时维持这些细胞的“年轻”状态?
小鼠研究设计
研究者使用雄性小鼠,部分小鼠自由进食,另一部分从成年早期开始终生实行约40%热量限制。有些被限制热量的小鼠随后恢复自由进食,以观察其血液系统恢复的速度。研究组测量了血细胞计数、检查了骨髓中的细胞群,并对稀有的造血干细胞进行了基因表达和表观遗传标记的谱系分析——这些化学标签位于DNA和蛋白上,帮助控制基因的开启与关闭。
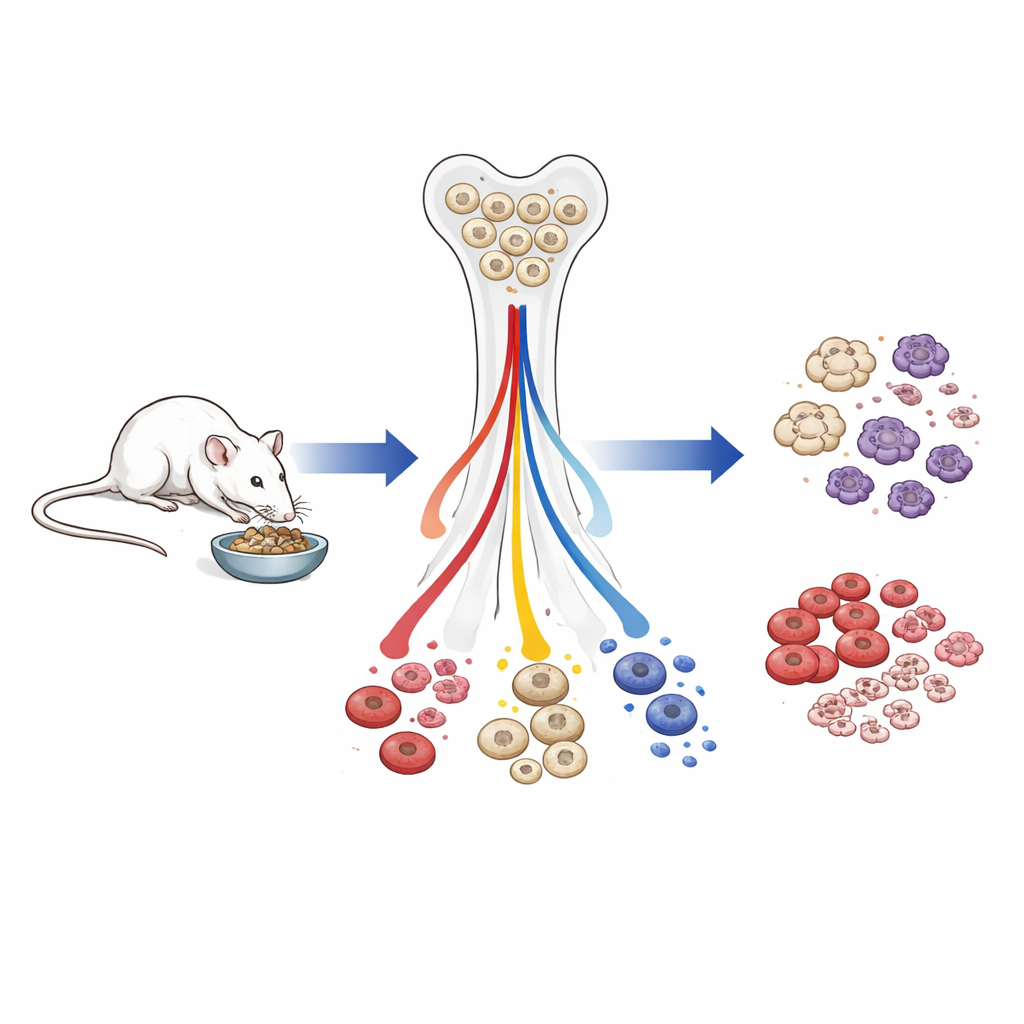
总体白细胞减少,但维持生存所需细胞
在大部分生命都受热量限制的老年小鼠中,外周血中白细胞总数下降。先天和适应性免疫细胞均减少,但幅度不同。与生存直接相关的细胞——载氧的红细胞、止血所需的血小板以及作为前线防御的髓系细胞(如粒细胞)——相对得到保留。相比之下,淋巴系细胞,尤以支持抗体应答的B细胞为甚,从骨髓的早期祖细胞到外周成熟细胞都显著减少。当热量受限的动物仅重新喂养四周后,白细胞计数和脾脏大小大多恢复,淋巴系生成激增,表明许多变化是可快速逆转的。
干细胞更努力工作并选择不同命运
出人意料的是,在食物短缺下血液层级顶端的干细胞并未变得更休眠;相反,它们的细胞周期更活跃。详细的基因表达分析显示,在热量受限时,这些干细胞下调了与长期自我更新相关的程序,提升了与短期干细胞和产生髓系及红系谱系的祖细胞相关的基因。换言之,干细胞被推动在短期内更努力地工作以维持关键的生存细胞类型,而牺牲了自身慢速更新或产生淋巴系细胞的能力。然而,尽管额外工作量增加,它们的整体基因活动模式更接近年轻干细胞而非衰老干细胞。
通过表观遗传开关重置衰老程序
研究团队接着探查为什么少吃能使老年干细胞在分子上看起来更年轻。他们绘制了两种常见组蛋白标记的分布,这两类标记通常分别促进或抑制基因活性。尽管这两种标记在热量受限的干细胞中总体下降,但一小部分与衰老相关的基因获得了抑制性标记并失去了激活性标记。其中两种基因特别突出:Kdr,编码血管生成信号的受体;以及Bmpr1a,另一种细胞表面受体。在热量限制下,这两基因更为紧密地被关闭。当研究者在正常喂养的老年干细胞中实验性降低Kdr和Bmpr1a并将这些细胞移植到受体小鼠时,移植细胞采纳了类似热量受限干细胞的基因表达模式,提示这些受体有助于驱动衰老程序,并可通过表观遗传方式被调节。
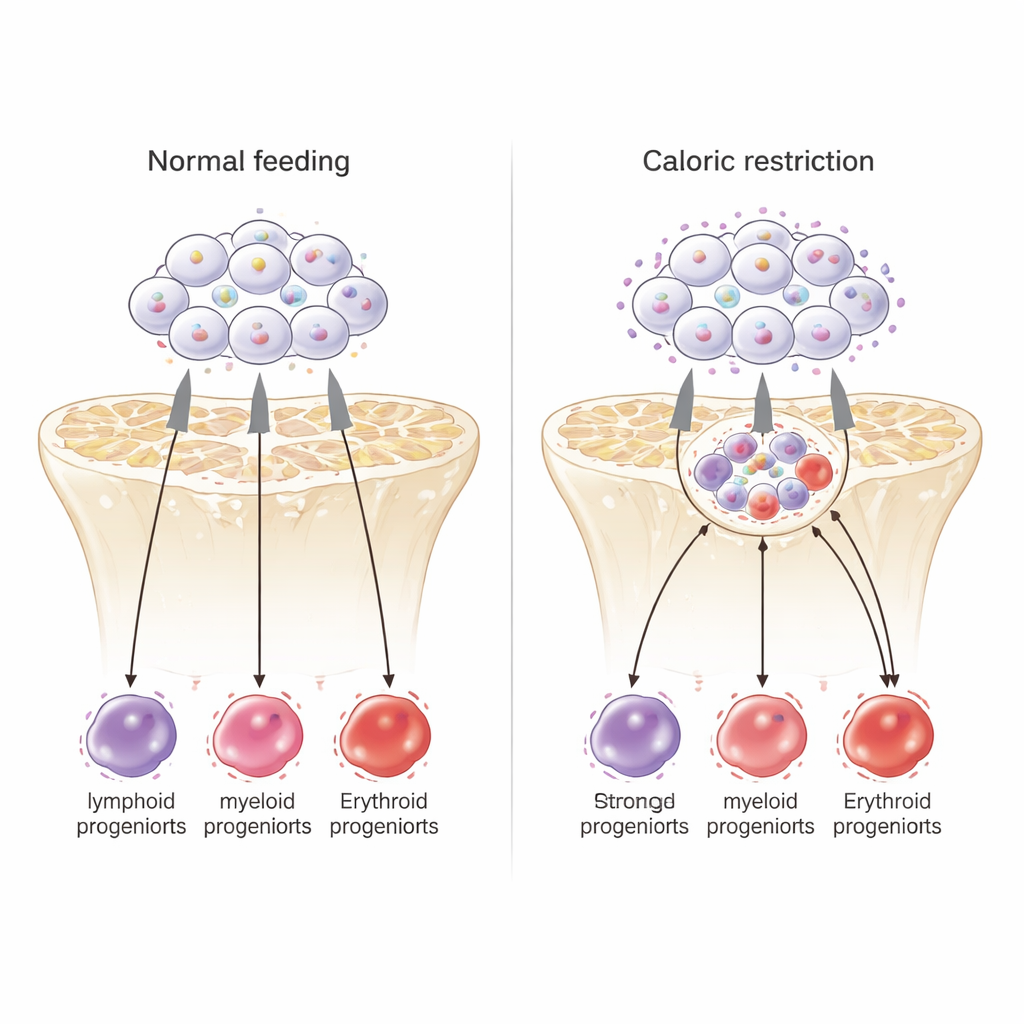
一个内部“交通指挥官”调整反应
为找出内部控制点,科学家们研究了干细胞基因组中DNA的可及性以及关键转录因子PU.1的结合位点。在热量限制下,许多DNA区域变得更开放并显示出更强的PU.1结合。这些PU.1结合位点附近的基因富集于细胞周期控制以及引导细胞走向红细胞和其他髓系命运的通路,而与深度干细胞静止相关的基因则趋于被抑制。约一半在Kdr被敲低时有反应的基因在其附近有PU.1存在,并且PU.1自身也在Kdr基因附近结合,暗示存在反馈回路。综合这些数据,PU.1被置于一个内部“交通指挥官”的位置:在降低KDR信号的背景下,它将衰老的干细胞重新导向一种类似热量受限的青年态,偏重于产生有利于生存的血细胞。
对健康老龄化的意义
这项工作为长期热量减少如何影响我们的造血工厂描绘了一幅细致的图景。在雄性小鼠中,少吃促使干细胞优先产生红细胞、血小板和快速反应的免疫细胞,同时抑制抗体产生细胞,这可能解释了严格饮食下对感染应答减弱的现象。与此同时,诸如Kdr等基因处的定向表观遗传改变和PU.1活性的转移,有助于在这些干细胞中维持更年轻的基因程序。尽管该研究在小鼠且仅限雄性,但结果表明未来的疗法可能旨在模拟热量限制对造血干细胞有益的分子效应——无需极端节食或牺牲免疫保护。
引用: Zong, L., Park, B., Tekin-Turhan, F. et al. Epigenetic profiling of hematopoietic stem cells from male mice identifies KDR and PU.1 as regulators of aging transcriptome and caloric restriction response. Nat Commun 17, 2978 (2026). https://doi.org/10.1038/s41467-026-69718-0
关键词: 热量限制, 造血干细胞, 免疫衰老, 表观遗传学, PU.1 与 KDR