Clear Sky Science · nl
Epigenetische profilering van hematopoëtische stamcellen van mannelijke muizen identificeert KDR en PU.1 als regelaars van het verouderings-transcriptoom en de reactie op calorierestrictie
Waarom minder eten ons bloed kan hervormen
Het verminderen van calorie-inname zonder ondervoeding is in veel diersoorten aangetoond de levensduur te verlengen, en sommige mensen volgen strikte diëten in de hoop langer te leven. Maar minder eten kan ook het immuunsysteem verzwakken. Deze studie stelt een eenvoudige maar belangrijke vraag: hoe verandert langdurige calorierestrictie de stamcellen in het beenmerg die constant ons bloed en immuunsysteem vernieuwen, en kunnen die veranderingen deze cellen "jong" houden terwijl ze ons toch beschermen?
Opzet van de muizenstudie
De onderzoekers werkten met mannelijke muizen die óf vrij aten óf hun hele leven een dieet kregen met ongeveer 40% minder calorieën, beginnend in de vroege volwassenheid. Sommige calorierestrictie-muizen mochten later weer vrij eten om te zien hoe snel hun bloedstelsel zich herstelde. Het team mat bloedwaarden, onderzocht celpopulaties in het beenmerg en bracht genactiviteit en epigenetische merkers in kaart—chemische tags op DNA en eiwitten die helpen bepalen welke genen aan staan—in de zeldzame hematopoëtische stamcellen die alle bloedcellen voortbrengen.
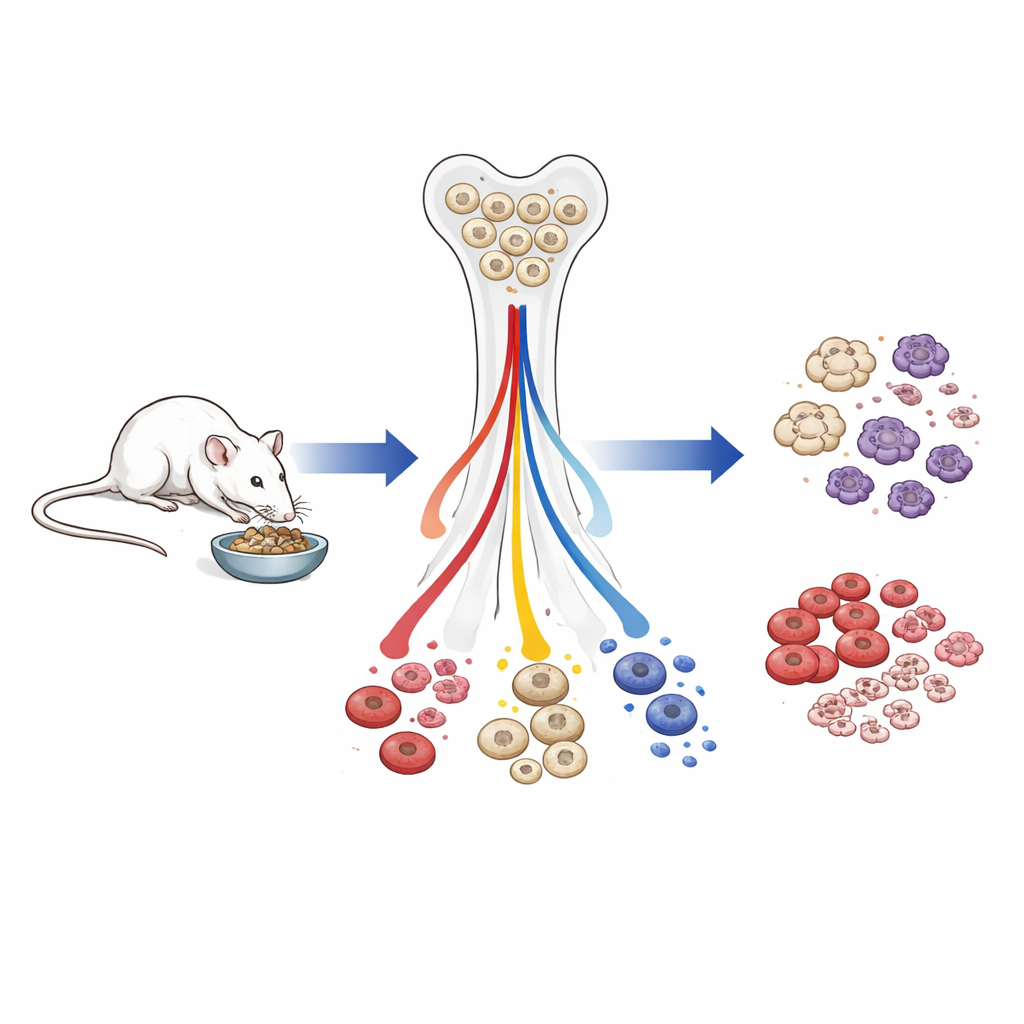
Minder totale witte bloedcellen, maar overlevingscellen beschermd
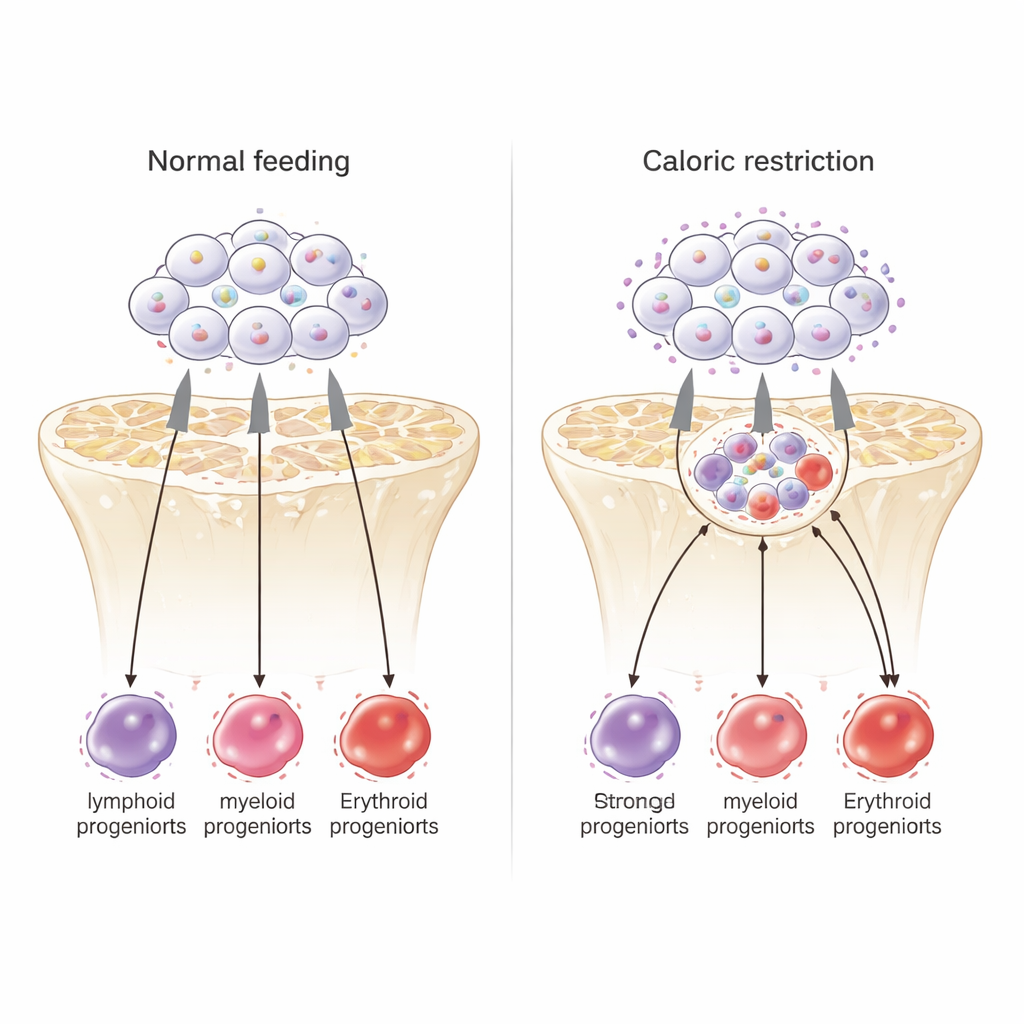
Bij oudere muizen die het grootste deel van hun leven minder calorieën hadden gekregen, daalde het totale aantal witte bloedcellen in de bloedbaan. Zowel de aangeboren als de adaptieve immuuncellen namen af, maar niet in gelijke mate. Cellen die belangrijk zijn voor directe overleving—rode bloedcellen die zuurstof vervoeren, bloedplaatjes die stollen, en frontlinie myeloïde verdedigers zoals granulocyten—bleken relatief behouden. Daarentegen waren lymfoïde cellen, met name B-cellen die antilichaamreacties ondersteunen, sterk verminderd vanaf vroege voorlopercellen in het beenmerg tot volwassen cellen in het bloed. Toen calorierestrictie-muizen vier weken werden bijgevoederd, herstelden witte bloedcellen en miltmaat grotendeels en nam de productie van lymfoïde cellen sterk toe, wat laat zien dat veel van deze veranderingen snel omkeerbaar zijn.
Stamcellen werken harder en kiezen andere loten
Verrassend genoeg werden de stamcellen bovenaan de bloedhiërarchie onder voedseltekort niet meer dormant; in plaats daarvan deelden ze actiever. Gedetailleerde genexpressieanalyses toonden dat deze stamcellen bij calorierestrictie programma’s voor langdurige zelfvernieuwing naar beneden schroefden en genen voor kortetermijnstamcellen en voorlopercellen die myeloïde en rode bloedlijnen maken, omhoog zetten. Met andere woorden: de stamcellen werden op korte termijn gedwongen harder te werken om cruciale overlevingsceltypen op peil te houden, ten koste van hun langzame vernieuwing of de productie van lymfoïde cellen. Toch leek het algehele patroon van genactiviteit meer op dat van jonge stamcellen dan op dat van oude.
Verouderen terugzetten via epigenetische schakelaars
Het team onderzocht vervolgens hoe minder eten oude stamcellen moleculair jonger kan laten lijken. Ze brachten twee veelvoorkomende histonmerken in kaart die doorgaans genactiviteit bevorderen of onderdrukken. Hoewel beide merkers globaal verminderd waren in calorierestrictie-stamcellen, verwierf een kleine set verouderingsgeassocieerde genen een onderdrukkend merkje en verloor een activerend merkje. Twee genen sprongen eruit: Kdr, dat codeert voor een receptor voor bloedvatgroeisignalen, en Bmpr1a, een andere celmembraanreceptor. Onder calorierestrictie waren beide genen strakker afgezet. Wanneer de onderzoekers Kdr en Bmpr1a experimenteel verlaagden in verouderde stamcellen van normaal gevoede muizen en deze cellen in ontvangers transplanteerden, namen de cellen een genexpressiepatroon aan dat leek op dat van calorierestrictie-stamcellen, wat suggereert dat deze receptoren het verouderingsprogramma aansturen en epigenetisch bijgesteld kunnen worden.
Een interne verkeersleider zet de reactie bij
Om interne controles te vinden onderzochten de wetenschappers hoe toegankelijk het DNA was over het stamcelgenoom en waar een sleutelfactor voor transcriptie, PU.1, gebonden was. Bij calorierestrictie werden veel DNA-regio’s opener en toonde PU.1 sterkere binding. Genen nabij deze PU.1-sites waren verrijkt voor celdelingscontrole en voor paden die cellen naar rode bloed- en andere myeloïde loten sturen, terwijl genen geassocieerd met diepe stamcelrust geneigd waren te worden onderdrukt. Ongeveer de helft van de genen die reageerden toen Kdr werd verlaagd, had PU.1 in de buurt, en PU.1 bindde zelf dicht bij het Kdr-gen, wat wijst op een feedbacklus. Gezamenlijk plaatsen deze data PU.1 als een interne verkeersleider die, in de context van verlaagde KDR-signalisatie, verouderende stamcellen heroriënteert naar een calorierestrictie-achtig, jeugdiger stadium dat prioriteit geeft aan overlevingsgerichte bloedcellen.
Wat dit betekent voor gezond ouder worden
Dit werk schetst een genuanceerd beeld van hoe langdurige caloriereductie onze bloedfabriek beïnvloedt. Bij mannelijke muizen dwingt minder eten stamcellen ertoe prioriteit te geven aan de aanmaak van rode cellen, bloedplaatjes en snel reagerende immuuncellen, terwijl antilichaamproducerende cellen worden tegengehouden—wat mogelijk verzwakte infectieresponsen onder strikte diëten verklaart. Tegelijkertijd helpen zorgvuldig gerichte epigenetische veranderingen bij genen zoals Kdr en verschuivingen in PU.1-activiteit een jeugdiger genprogramma in deze stamcellen te behouden. Hoewel de studie in muizen en alleen bij mannen is uitgevoerd, suggereert ze dat toekomstige therapieën zouden kunnen proberen de gunstige moleculaire effecten van calorierestrictie op bloedvormende stamcellen na te bootsen—zonder extreme diëten of inboet aan immuunbescherming.
Bronvermelding: Zong, L., Park, B., Tekin-Turhan, F. et al. Epigenetic profiling of hematopoietic stem cells from male mice identifies KDR and PU.1 as regulators of aging transcriptome and caloric restriction response. Nat Commun 17, 2978 (2026). https://doi.org/10.1038/s41467-026-69718-0
Trefwoorden: calorierestrictie, hematopoëtische stamcellen, immuungeleiding, epigenetica, PU.1 en KDR