Clear Sky Science · ja
オスマウスの造血幹細胞のエピジェネティックプロファイリングが、加齢トランスクリプトームとカロリー制限応答の調節因子としてKDRとPU.1を同定する
なぜ摂取カロリーを減らすと血液が変わるのか
栄養失調に陥らない範囲でのカロリー制限は多くの動物で寿命を延ばすことが示されており、長生きを期待して厳格な食事を続ける人もいます。しかし、摂取カロリーを減らすことは免疫系を弱めることもあります。本研究は単純だが重要な問いを扱います:長期的なカロリー制限は、常に血液や免疫系を再生している骨髄中の幹細胞をどのように変え、その変化はこれらの細胞を「若く」保ちながら私たちを守ることに役立つか、という点です。
マウスでの実験デザイン
研究者らは、自由摂食の群と、成人初期から生涯にわたり約40%カロリーを減らした食事にしたオスのマウスを用いました。カロリー制限群の一部は後に再び自由に摂食させ、造血系がどのくらい速く回復するかを調べました。チームは血球数を測定し、骨髄内の細胞集団を解析し、希少な造血幹細胞における遺伝子発現とエピジェネティックマーク(遺伝子のオン・オフを制御するDNAやタンパク質上の化学的タグ)をプロファイルしました。
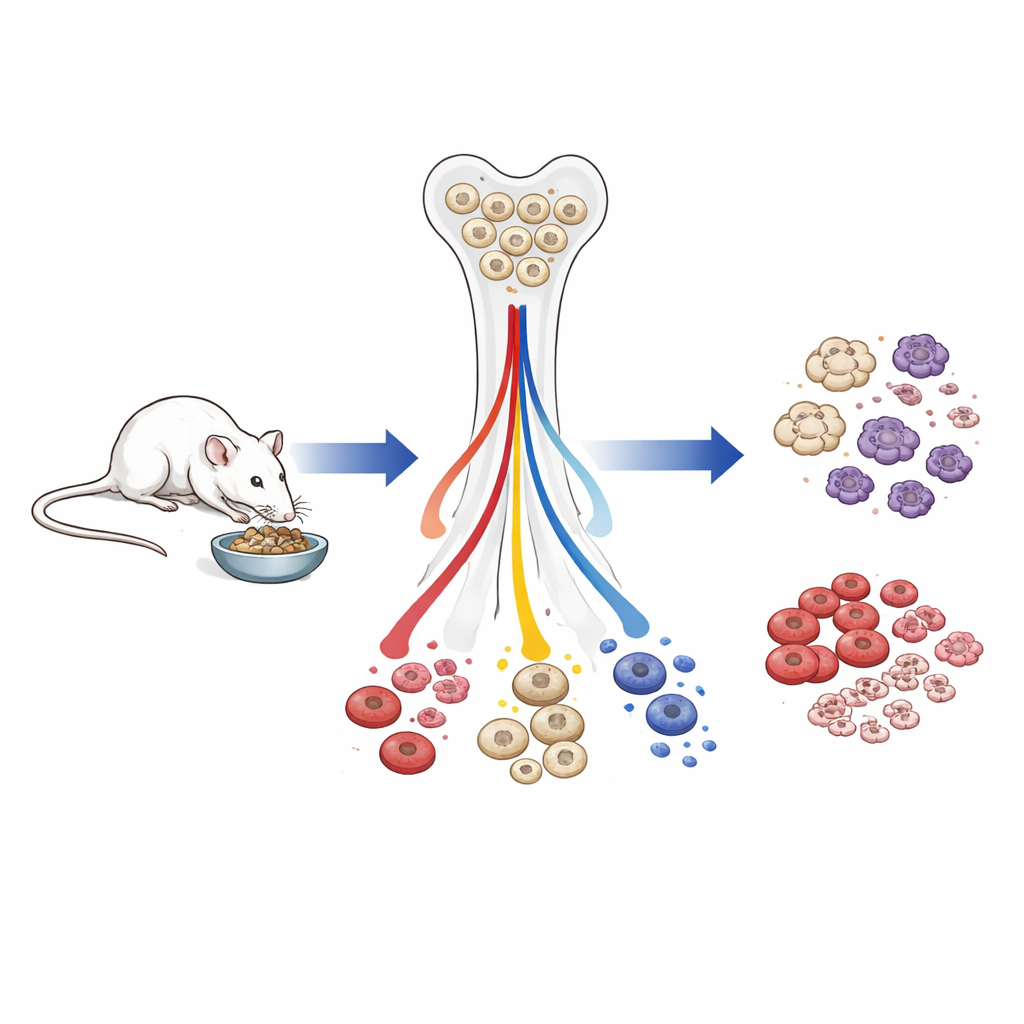
白血球総数は減るが、生存に重要な細胞は守られる
大部分の生涯をカロリー制限で過ごした高齢マウスでは、血流中の全体的な白血球数が低下しました。自然免疫と獲得免疫の両方の細胞が減少しましたが、均等ではありませんでした。酸素を運ぶ赤血球、血液を凝固させる血小板、好中球などの前線の骨髄系(ミエロイド)防御細胞といった即時の生存に重要な細胞は比較的保たれていました。一方、抗体応答を支えるB細胞を含むリンパ系細胞は、骨髄の初期前駆細胞から血中の成熟細胞に至るまで強く減少していました。カロリー制限マウスを4週間再給餌すると、白血球数や脾臓サイズは大部分が回復し、リンパ系の産生は急増しました。これらの変化の多くは迅速に可逆的であることを示しています。
幹細胞はより活発に働き、運命を変える
驚くべきことに、血液階層の最上位にある幹細胞は食物不足で休眠化するのではなく、むしろより活発に細胞周期を回していました。詳細な遺伝子発現解析により、カロリー制限下ではこれらの幹細胞が長期的な自己複製に関連するプログラムを抑え、短期的な幹細胞やミエロイド系や赤血球系列を作る前駆細胞に関連する遺伝子を上げていることが明らかになりました。言い換えれば、幹細胞は生存に重要な細胞型を短期的に維持するためにより多く働くよう押され、その代償として自らをゆっくり更新したりリンパ系細胞を生み出したりする能力が減じられています。それでも、追加の労力にもかかわらず、それらの全体的な遺伝子発現パターンは老化した幹細胞よりむしろ若い幹細胞に近い様子を示していました。
エピジェネティックなスイッチで老化プログラムをリセット
次に、なぜ食事を減らすと老化した幹細胞が分子的に若く見えるようになるのかを調べました。研究者らは一般に遺伝子活性を促進または抑制する2種類のヒストンマークをマッピングしました。両方のマークはカロリー制限下の幹細胞で全体的に減少していましたが、少数の老化関連遺伝子は抑制マークを獲得し、活性化マークを失っていました。その中で際立っていたのが、血管成長シグナルの受容体をコードするKdrと、別の細胞表面受容体であるBmpr1aでした。カロリー制限下ではこれら両方の遺伝子がより強く抑えられていました。研究者らが通常の食餌で飼育した高齢マウスの幹細胞でKdrとBmpr1aを実験的に低下させ、その細胞を移植すると、移植後の細胞はカロリー制限群の幹細胞に似た遺伝子発現パターンを示しました。これはこれらの受容体が老化プログラムを駆動し、エピジェネティックに調整可能であることを示唆します。
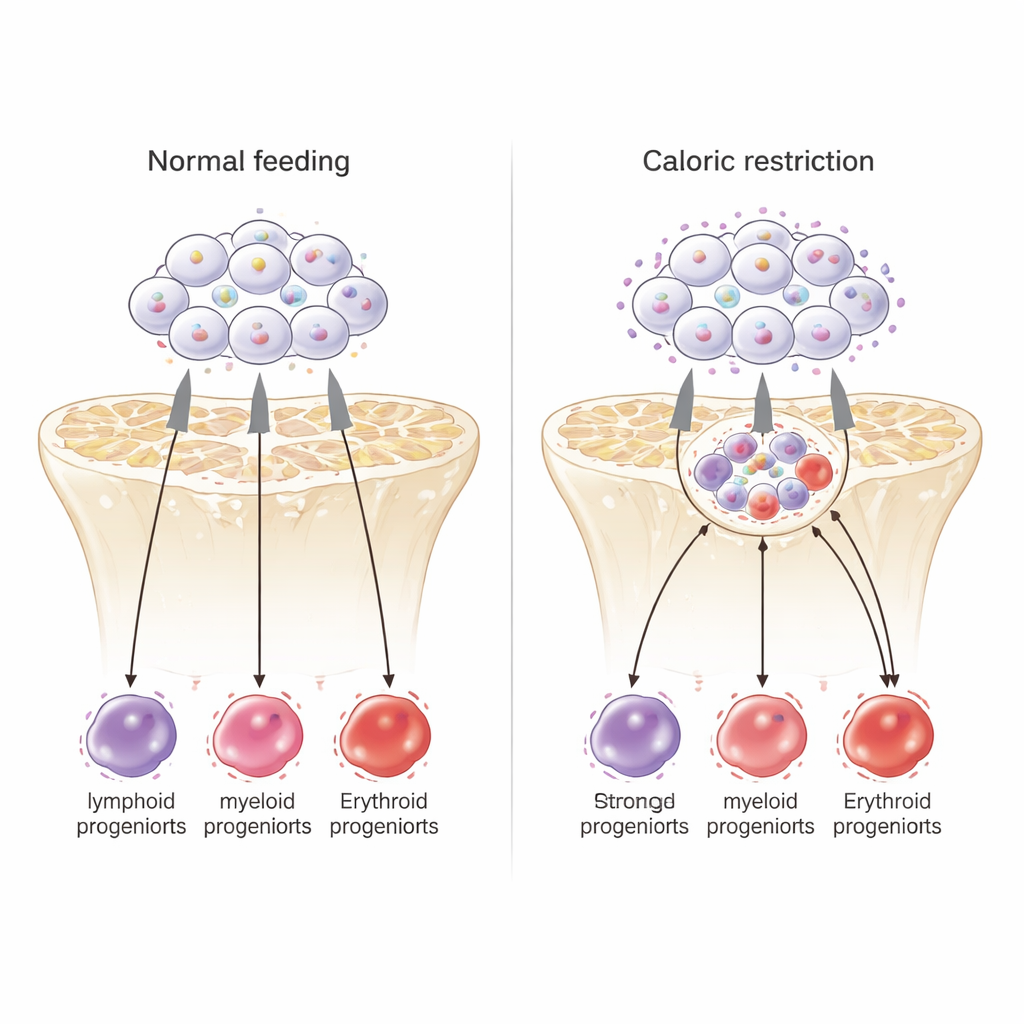
応答を調整する内部の交通整理役
内部の制御点を明らかにするために、科学者らは幹細胞ゲノム全体でDNAのアクセスしやすさと、重要な転写因子PU.1がどこに結合しているかを調べました。カロリー制限下では多くのDNA領域がより開かれ、PU.1の結合が強まっている部分がありました。これらのPU.1結合部位近傍の遺伝子は細胞周期制御や赤血球やその他のミエロイド運命へ向かう経路に富み、一方で深い幹細胞の休眠に関する遺伝子は抑制される傾向がありました。Kdrをノックダウンした際に応答を示した遺伝子の約半分は近傍にPU.1が存在し、PU.1自身もKdr遺伝子の近くに結合しており、フィードバックループの存在を示唆しています。これらのデータは、PU.1を内部の交通整理役として位置づけ、KDRシグナルが低下した文脈でPU.1が老化した幹細胞をカロリー制限下の若々しい状態へ、つまり生存志向の血液細胞を優先する方向へ再配分することを示しています。
健康的な加齢への示唆
この研究は長期的なカロリー制限が血液工場に与える影響について微妙な像を描き出します。オスのマウスでは、摂取カロリーの削減が幹細胞に赤血球、血小板、迅速に作用する免疫細胞の産生を優先させる一方で、抗体を作る細胞の抑制を招き、厳格な食事が感染に対する応答を弱める理由を説明する可能性があります。同時に、Kdrのような遺伝子に対する狙いを定めたエピジェネティック変化やPU.1活性の変化が、これら幹細胞のより若々しい遺伝子プログラムを維持するのに役立ちます。本研究はマウス、かつオスのみで行われた点に留意が必要ですが、将来的には極端な食事や免疫保護の犠牲を伴わずに、造血幹細胞に対するカロリー制限の有益な分子的影響を模倣する治療法を目指す可能性を示唆しています。
引用: Zong, L., Park, B., Tekin-Turhan, F. et al. Epigenetic profiling of hematopoietic stem cells from male mice identifies KDR and PU.1 as regulators of aging transcriptome and caloric restriction response. Nat Commun 17, 2978 (2026). https://doi.org/10.1038/s41467-026-69718-0
キーワード: カロリー制限, 造血幹細胞, 免疫の加齢, エピジェネティクス, PU.1 と KDR