Clear Sky Science · de
Epigenetische Profilierung hämatopoetischer Stammzellen männlicher Mäuse identifiziert KDR und PU.1 als Regulatoren des Alterns‑Transkriptoms und der Reaktion auf Kalorienrestriktion
Warum weniger Essen unser Blut umgestalten könnte
Eine moderate Kalorienreduktion ohne Unterernährung verlängert in vielen Tierarten die Lebensspanne, und manche Menschen folgen strengen Diäten in der Hoffnung, länger zu leben. Gleichzeitig kann weniger Essen das Immunsystem schwächen. Diese Studie stellt eine einfache, aber wichtige Frage: Wie verändert langfristige Kalorienreduktion die Stammzellen im Knochenmark, die unser Blut und Immunsystem ständig erneuern, und können diese Veränderungen dazu beitragen, diese Zellen „jung“ zu halten und gleichzeitig Schutzfunktionen zu bewahren?
Versuchsaufbau in Mäusen
Die Forschenden arbeiteten mit männlichen Mäusen, die entweder ad libitum fraßen oder ab dem jungen Erwachsenenalter lebenslang eine um etwa 40 % reduzierte Kalorienzufuhr erhielten. Einige kalorienreduzierte Tiere durften später wieder frei fressen, um zu testen, wie schnell sich ihr Blutsystem erholt. Das Team bestimmte Blutwerte, untersuchte Zellpopulationen im Knochenmark und erfasste Genaktivität sowie epigenetische Markierungen — chemische Tags an DNA und Proteinen, die steuern, welche Gene aktiviert werden — in den seltenen hämatopoetischen Stammzellen, aus denen alle Blutzellen hervorgehen.
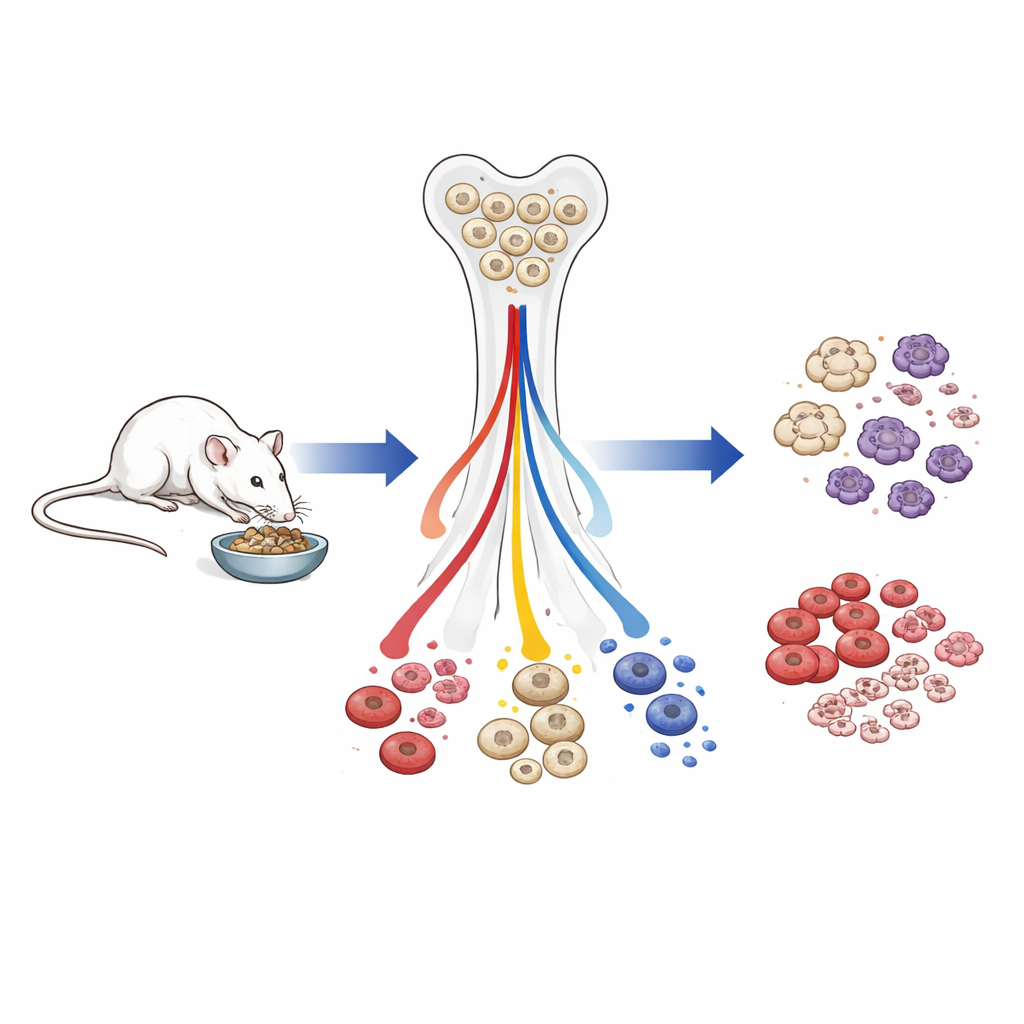
Weniger Gesamtleukozyten, aber Überlebenszellen werden geschützt
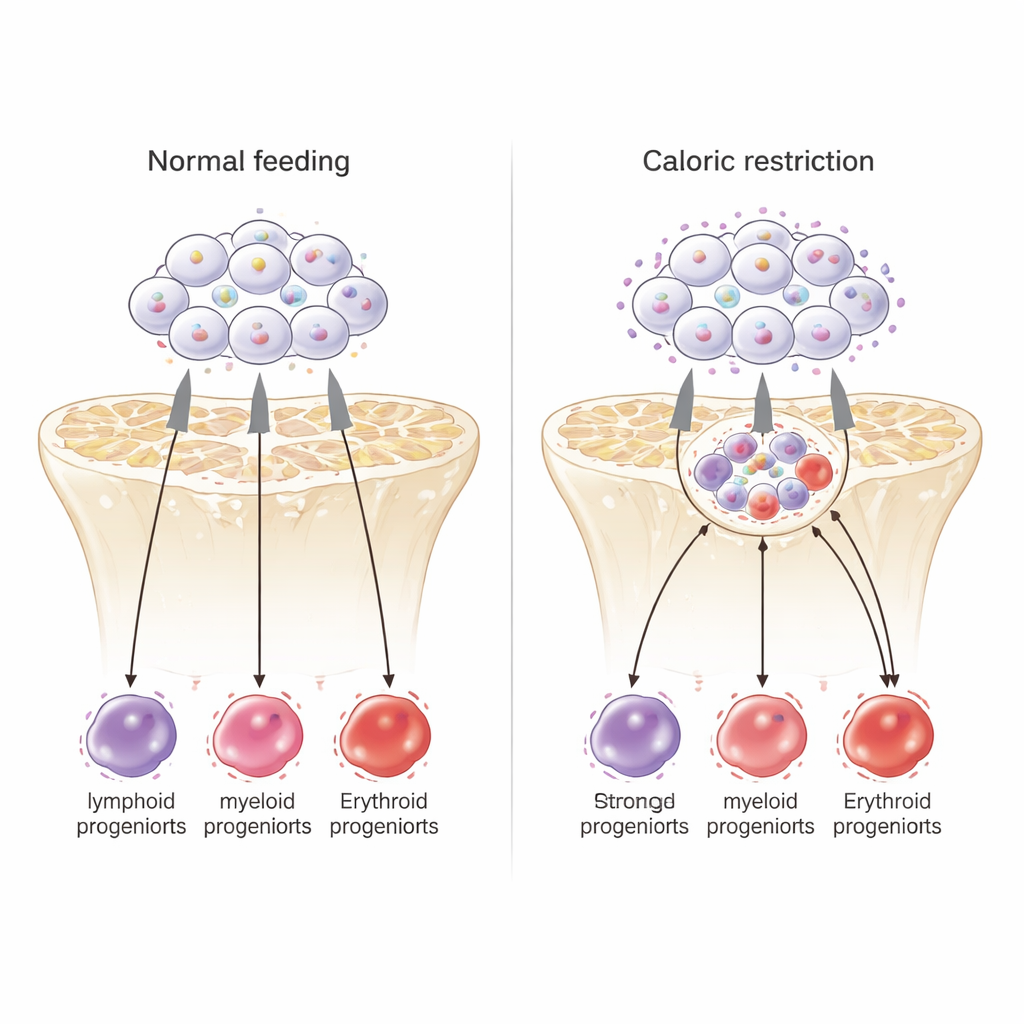
Bei älteren Mäusen, die den Großteil ihres Lebens weniger Kalorien aufgenommen hatten, fielen die Gesamtzahlen weißer Blutzellen im Blut. Sowohl angeborene als auch adaptive Immunzellen nahmen ab, jedoch nicht gleichmäßig. Für das sofortige Überleben wichtige Zelltypen — rote Blutkörperchen, die Sauerstoff transportieren; Thrombozyten, die Blutungen stillen; und frontline-myeloide Abwehrzellen wie Granulozyten — blieben vergleichsweise erhalten. Im Gegensatz dazu waren lymphoide Zellen, insbesondere B‑Zellen, die Antikörperantworten unterstützen, vom frühen Vorläuferstadium im Knochenmark bis zu reifen Zellen im Blut stark vermindert. Wurden die kalorienreduzierten Tiere nur vier Wochen wieder normal gefüttert, erholten sich Leukozytenzahl und Milzgröße weitgehend, und die lymphoide Produktion stieg stark an, was zeigt, dass viele dieser Veränderungen schnell reversibel sind.
Stammzellen arbeiten härter und wählen andere Schicksale
Überraschenderweise traten die Stammzellen an der Spitze der Bluthierarchie bei Nahrungsentzug nicht stärker in Dormanz; stattdessen teilten sie sich aktiver. Detaillierte Genexpressionsanalysen zeigten, dass diese Stammzellen unter Kalorienrestriktion Programme der langfristigen Selbsterneuerung herunterfuhren und Gene hochregulierten, die mit kurzlebigen Stammzellen und Vorläufern verbunden sind, die myeloide und erythroide Linien produzieren. Anders gesagt: Die Stammzellen wurden kurzfristig dazu gedrängt, härter zu arbeiten, um kritisch wichtige Überlebenszelltypen aufrechtzuerhalten, zulasten ihrer langsamen Selbsterneuerung oder der Produktion lymphoider Zellen. Dennoch ähnelte ihr gesamtes Genaktivitätsmuster eher dem von jungen als von alten Stammzellen.
Alterungsprogramme durch epigenetische Schalter zurücksetzen
Die Forschenden fragten als Nächstes, wie weniger Essen alte Stammzellen molekular jünger erscheinen lassen kann. Sie kartierten zwei verbreitete Histonmarken, die im Allgemeinen Genaktivität fördern beziehungsweise hemmen. Obwohl beide Marken insgesamt in kalorienreduzierten Stammzellen vermindert waren, erhielt eine kleine Gruppe alterungsassoziierter Gene eine repressive Marke und verlor eine aktivierende. Zwei Gene stachen hervor: Kdr, das einen Rezeptor für Gefäßwachstums‑Signale codiert, und Bmpr1a, ein weiterer membranständiger Rezeptor. Unter Kalorienrestriktion wurden beide Gene stärker herunterreguliert. Wenn die Forschenden Kdr und Bmpr1a experimentell in gealterten Stammzellen aus normal gefütterten Mäusen verminderten und diese Zellen transplantierten, nahmen die Zellen ein Genexpressionsmuster an, das dem kalorienreduzierter Stammzellen ähnelte — ein Hinweis darauf, dass diese Rezeptoren das Altersprogramm mitsteuern und epigenetisch ansprechbar sind.
Ein interner Verkehrspolizist steuert die Reaktion
Um interne Kontrollpunkte aufzudecken, untersuchten die Wissenschaftler, wie zugänglich die DNA im gesamten Stammzellgenom war und wo der wichtige Transkriptionsfaktor PU.1 gebunden war. Unter Kalorienrestriktion wurden viele DNA‑Regionen offener und zeigten stärkere PU.1‑Bindung. Gene in der Nähe dieser PU.1‑Stellen waren angereichert für Zellzykluskontrolle und für Wege, die Zellen in Richtung roter Blut- und anderer myeloider Schicksale lenken, während Gene, die mit tiefer Stammzellruhezuständen assoziiert sind, tendenziell reprimiert wurden. Etwa die Hälfte der Gene, die auf Kdr‑Herunterregulierung reagierten, zeigte PU.1 in der Nähe, und PU.1 band selbst in der Nähe des Kdr‑Gens, was auf eine Rückkopplung hindeutet. Zusammen positionieren diese Daten PU.1 als internen Verkehrspolizisten, der im Kontext reduzierter KDR‑Signalgebung alternde Stammzellen in einen kalorienrestriktionsähnlichen, jugendlich wirkenden Zustand umlenkt, der auf überlebensorientierte Blutzellen setzt.
Was das für gesundes Altern bedeutet
Diese Arbeit zeichnet ein nuanciertes Bild davon, wie langfristige Kalorienreduktion unsere Blutproduktion beeinflusst. Bei männlichen Mäusen veranlasst weniger Essen die Stammzellen, vorrangig rote Zellen, Thrombozyten und schnell reagierende Immunzellen zu produzieren, während die Bildung antikörperbildender Zellen eingeschränkt wird — ein möglicher Grund für schwächere Infektionsabwehr unter strengen Diäten. Gleichzeitig helfen gezielte epigenetische Veränderungen an Genen wie Kdr und Verschiebungen in der PU.1‑Aktivität, ein jugendlicheres Genprogramm in diesen Stammzellen zu bewahren. Obwohl die Studie an Mäusen und nur an Männchen durchgeführt wurde, legt sie nahe, dass künftige Therapien darauf abzielen könnten, die vorteilhaften molekularen Effekte der Kalorienrestriktion auf blutbildende Stammzellen nachzuahmen — ohne extreme Diäten oder Einbußen beim Immunschutz.
Zitation: Zong, L., Park, B., Tekin-Turhan, F. et al. Epigenetic profiling of hematopoietic stem cells from male mice identifies KDR and PU.1 as regulators of aging transcriptome and caloric restriction response. Nat Commun 17, 2978 (2026). https://doi.org/10.1038/s41467-026-69718-0
Schlüsselwörter: Kalorienrestriktion, hämatopoetische Stammzellen, Immunalterung, Epigenetik, PU.1 und KDR