Clear Sky Science · ru
Эпигенетический профиль гемопоэтических стволовых клеток у самцов мышей выявляет KDR и PU.1 как регуляторы стареющего транскриптома и ответа на ограничение калорий
Почему меньше есть может изменить нашу кровь
Сокращение калорий без недоедания показало, что удлиняет продолжительность жизни у многих животных, и некоторые люди даже придерживаются строгих диет в надежде жить дольше. Но уменьшение питания также может ослаблять иммунную систему. В этом исследовании поставлен простой, но важный вопрос: как длительное сокращение калорий меняет стволовые клетки костного мозга, которые постоянно восстанавливают нашу кровь и иммунную систему, и могут ли эти изменения помочь сохранять эти клетки «молодыми», одновременно защищая нас?
Как было организовано исследование на мышах
Исследователи работали с самцами мышей, которые либо питались свободно, либо с ранней взрослой жизни содержались на диете с примерно на 40% меньшей калорийностью. Часть животных на ограничении калорий позднее снова переводили на свободное кормление, чтобы посмотреть, как быстро восстанавливается их кроветворная система. Команда измеряла показатели крови, изучала популяции клеток в костном мозге и профилировала активность генов и эпигенетические метки — химические метки на ДНК и белках, которые помогают контролировать включение генов — в редких гемопоэтических стволовых клетках, дающих начало всем клеткам крови.
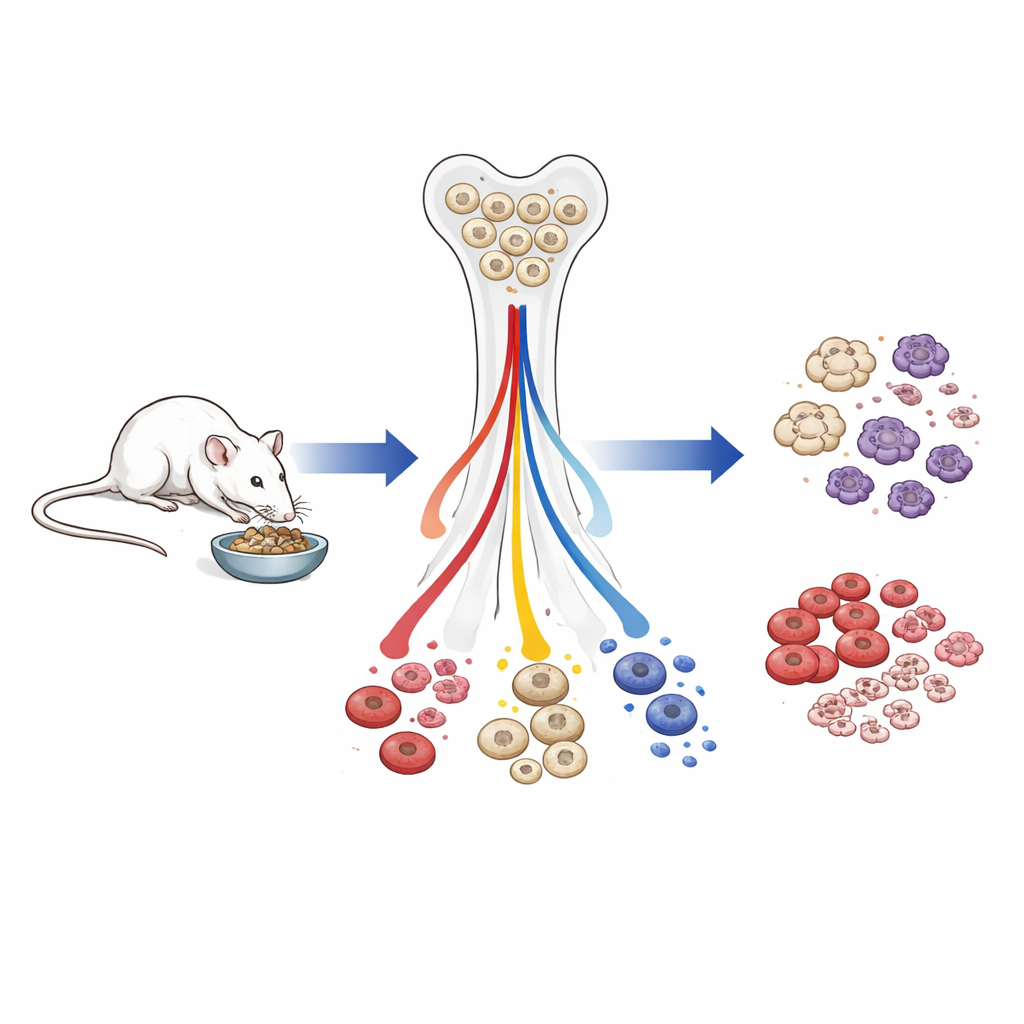
Меньше лейкоцитов в целом, но клетки, отвечающие за выживание, защищены
У старых мышей, большую часть жизни проведших на пониженной калорийности, общее число лейкоцитов в крови снизилось. Падали и клетки врожденного, и адаптивного иммунитета, но не одинаково. Клетки, важные для немедленного выживания — эритроциты, переносящие кислород, тромбоциты, свертывающие кровь, и фронтовые миелоидные защитники, такие как гранулоциты — оказались относительно сохранены. В отличие от них лимфоидные клетки, особенно B-клетки, поддерживающие выработку антител, резко уменьшились начиная с ранних предшественников в костном мозге и до зрелых клеток в крови. Когда животных с ограничением калорий повторно кормили всего четыре недели, количество лейкоцитов и размер селезенки в основном восстановились, а продукция лимфоидных клеток резко возросла, что показывает: многие из этих изменений быстро обратимы.
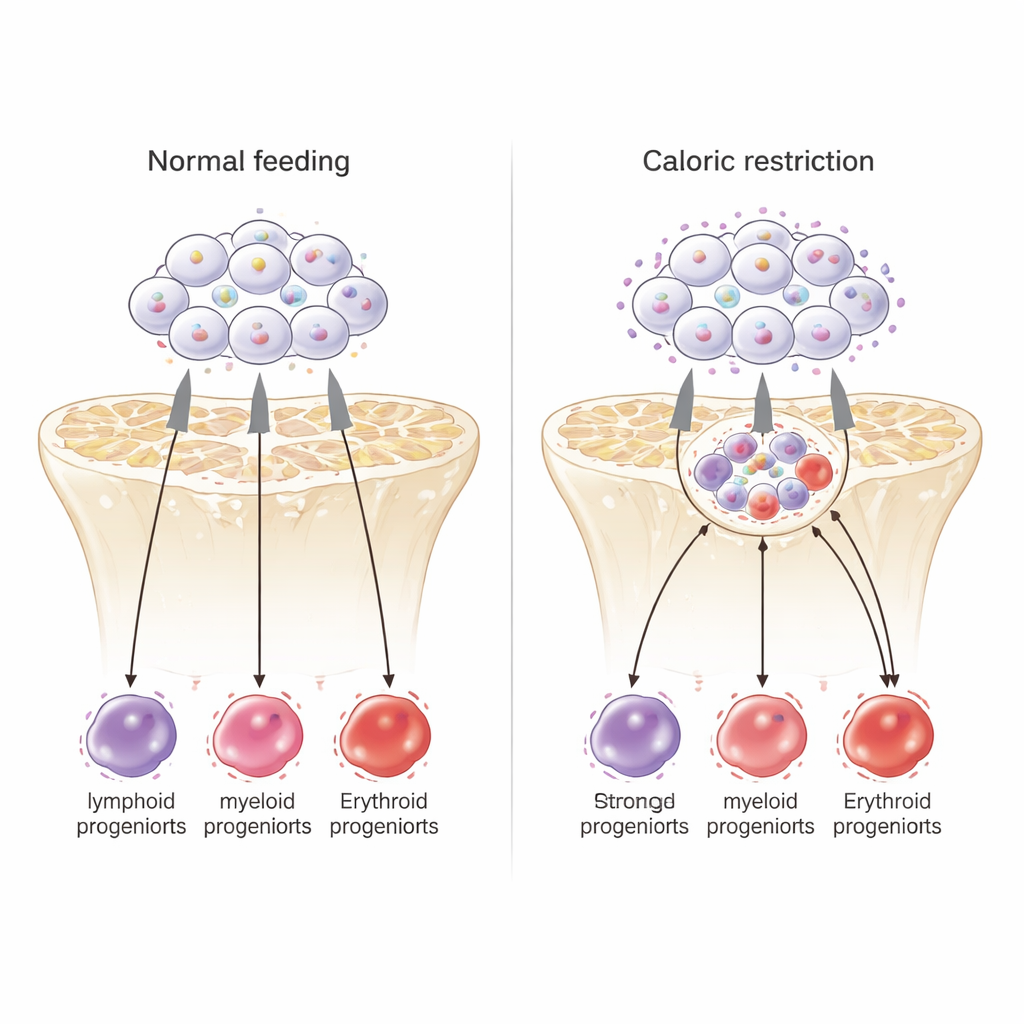
Стволовые клетки работают интенсивнее и выбирают иной путь дифференцировки
Удивительно, но стволовые клетки на вершине иерархии кроветворения не стали более спящими при нехватке пищи; напротив, они активнее входили в цикл. Детальные анализы экспрессии генов показали, что при ограничении калорий эти стволовые клетки ослабляли программы, связанные с долгосрочным самоподдержанием, и усиливали гены, ассоциированные с краткоживущими стволовыми клетками и предшественниками, дающими миелоидные и эритроидные линии. Иными словами, стволовые клетки были вынуждены работать интенсивнее в короткой перспективе, чтобы поддерживать ключевые клетки выживания, за счет медленного самовоспроизведения или генерации лимфоидных клеток. Тем не менее, несмотря на эту дополнительную нагрузку, их общий профиль активности генов больше походил на профиль молодых стволовых клеток, чем старых.
Переключение программ старения через эпигенетические рычаги
Далее команда спросила, как уменьшение питания может делать старые стволовые клетки молекулярно более молодыми. Они картировали две распространенные модификации гистонов, которые обычно активируют или репрессируют активность генов. Хотя обе метки в целом снижались в стволовых клетках при ограничении калорий, небольшой набор генов, ассоциированных со старением, приобрел репрессивную метку и потерял активирующую. Выделялись два гена: Kdr, кодирующий рецептор для сигналов роста кровеносных сосудов, и Bmpr1a, другой рецептор на поверхности клетки. При ограничении калорий оба гена были сильнее заглушены. Когда исследователи экспериментально понижали экспрессию Kdr и Bmpr1a в старых стволовых клетках у мышей с нормальным питанием и пересаживали эти клетки реципиентам, клетки приняли профиль экспрессии, напоминающий клетки при ограничении калорий, что предполагает: эти рецепторы способствуют запуску программы старения и могут быть эпигенетически настроены.
Внутренний регулятор направляет ответ
Чтобы выявить внутренние точки контроля, ученые исследовали доступность ДНК по всему геному стволовых клеток и локализацию ключевого транскрипционного фактора PU.1. При ограничении калорий многие области ДНК становились более открытыми и демонстрировали усиленное связывание PU.1. Гены рядом с этими сайтами PU.1 были обогащены путями контроля клеточного цикла и направляли клетки в сторону эритроидных и других миелоидных судеб, тогда как гены, связанные с глубокой покоящейся фазой стволовых клеток, как правило, репрессировались. Примерно у половины генов, реагировавших на снижение Kdr, рядом обнаруживались сайты PU.1, а сам PU.1 связывался близко к гену Kdr, что намекает на петлю обратной связи. В совокупности эти данные позиционируют PU.1 как внутреннего «регулировщика движения», который в контексте снижения KDR-сигналинга перекрывает курс стареющих стволовых клеток в сторону состояния, напоминающего ограничение калорий и молодость, с приоритетом на клетки, ориентированные на выживание.
Что это значит для здорового старения
Эта работа рисует тонкую картину того, как длительное сокращение калорий влияет на нашу «кроветворную фабрику». У самцов мышей уменьшение питания заставляет стволовые клетки отдать приоритет производству эритроцитов, тромбоцитов и быстро действующих иммунных клеток, одновременно подавляя клетки, продуцирующие антитела — что может объяснять ослабленные ответы на инфекции при строгих диетах. Вместе с тем целенаправленные эпигенетические изменения в генах, таких как Kdr, и сдвиги в активности PU.1 помогают сохранить более молодой генетический профиль этих стволовых клеток. Хотя исследование проведено на мышах и только на самцах, оно указывает на то, что будущие терапии могут попытаться имитировать полезные молекулярные эффекты ограничения калорий на кроветворные стволовые клетки — без необходимости экстремального диетического режима или жертвы иммунной защиты.
Цитирование: Zong, L., Park, B., Tekin-Turhan, F. et al. Epigenetic profiling of hematopoietic stem cells from male mice identifies KDR and PU.1 as regulators of aging transcriptome and caloric restriction response. Nat Commun 17, 2978 (2026). https://doi.org/10.1038/s41467-026-69718-0
Ключевые слова: ограничение калорий, гемопоэтические стволовые клетки, старение иммунной системы, эпигенетика, PU.1 и KDR