Clear Sky Science · sv
Epigenetisk profilering av hematopoetiska stamceller från hanmöss identifierar KDR och PU.1 som regulatorer av åldrande-transkriptomet och svar på kalorirestriktion
Varför minskat ätande kan omforma vårt blod
Att skära ned på kalorier utan att bli undernärd har visat sig förlänga livslängden hos många djur, och vissa människor följer strikta dieter i hopp om att leva längre. Men att äta mindre kan också försvaga immunsystemet. Denna studie ställer en enkel men viktig fråga: hur förändrar långvarig kalorirestriktion stamcellerna i benmärgen som ständigt bygger upp vårt blod och immunsystem, och kan dessa förändringar hjälpa till att hålla dessa celler ”unga” samtidigt som de skyddar oss?
Hur studien genomfördes i möss
Forskarna arbetade med hanmöss som antingen åt fritt eller hölls på en livslång diet med omkring 40 % färre kalorier, från tidig vuxen ålder. Vissa kalorireducerade möss fick senare äta fritt igen för att se hur snabbt deras blodsystem återhämtade sig. Teamet mätte blodvärden, undersökte cellpopulationer i benmärgen och profilerade genaktivitet och epigenetiska markörer — kemiska taggar på DNA och proteiner som hjälper till att reglera vilka gener som är aktiva — i de sällsynta hematopoetiska stamcellerna som ger upphov till alla blodceller.
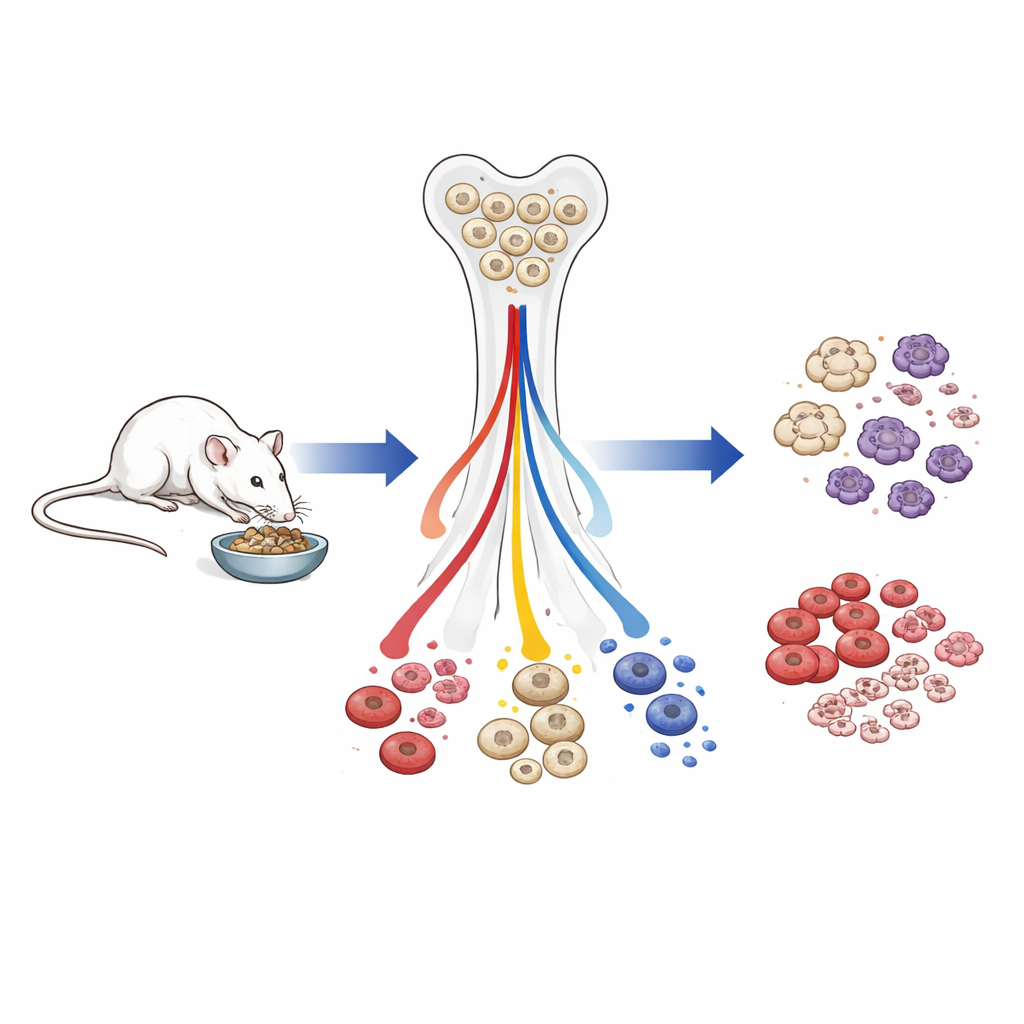
Mindre totalt vita blodkroppar, men överlevnadsceller skyddas
Hos äldre möss som tillbringat större delen av livet på färre kalorier sjönk det totala antalet vita blodkroppar i blodomloppet. Både medfödda och adaptiva immunceller minskade, men inte i samma grad. Celler viktiga för omedelbar överlevnad — röda blodkroppar som transporterar syre, trombocyter som koagulerar blodet, och ledande myeloida försvarare såsom granulocyter — var relativt bevarade. I kontrast minskade lymfoida celler, särskilt B‑celler som stödjer antikroppsreaktioner, kraftigt från tidiga progenitorer i benmärgen ända till mogna celler i blodet. När kalorireducerade djur återfick fri föda under bara fyra veckor återhämtade sig vita blodkroppsvärden och mjältens storlek i stort sett, och lymfoid produktion ökade kraftigt, vilket visar att många av dessa förändringar är snabbt reversibla.
Stamceller arbetar hårdare och väljer andra öden
Överraskande nog blev inte stamcellerna högst upp i blodhierarkin mer dvala under matbrist; istället cyklade de mer aktivt. Detaljerade analyser av genuttryck visade att dessa stamceller vid kalorirestriktion nedreglerade program kopplade till långsiktig självförnyelse och uppreglerade gener associerade med korttidsstamceller och progenitorer som ger upphov till myeloida och röda blodcellslinjer. Med andra ord pressades stamcellerna att arbeta hårdare på kort sikt för att upprätthålla centrala överlevnadscelltyper, på bekostnad av att långsamt förnya sig själva eller generera lymfoida celler. Trots detta extra arbete liknade deras övergripande genaktivitetsmönster mer det hos unga stamceller än hos gamla.
Återställa åldringsprogram via epigenetiska strömbrytare
Teamet frågade nästa hur minskat ätande kan få gamla stamceller att se molekylärt yngre ut. De kartlade två vanliga histonmarkörer som i allmänhet främjar respektive hämmar genaktivitet. Även om båda markörerna globalt sett var minskade i kalorirestrikterade stamceller, fick en liten uppsättning åldersassocierade gener en repressiv markör och förlorade en aktiverande sådan. Två gener stack ut: Kdr, som kodar för en receptor för blodkärlstillväxtsignaler, och Bmpr1a, en annan ytlig receptor. Under kalorirestriktion stängdes båda generna hårdare. När forskarna experimentellt sänkte Kdr och Bmpr1a i åldrade stamceller från normalt matade möss och transplanterade dessa celler till mottagare antog cellerna ett genuttrycksmönster som liknade det hos kalorirestrikterade stamceller, vilket tyder på att dessa receptorer driver åldringsprogrammet och kan ställas om epigenetiskt.
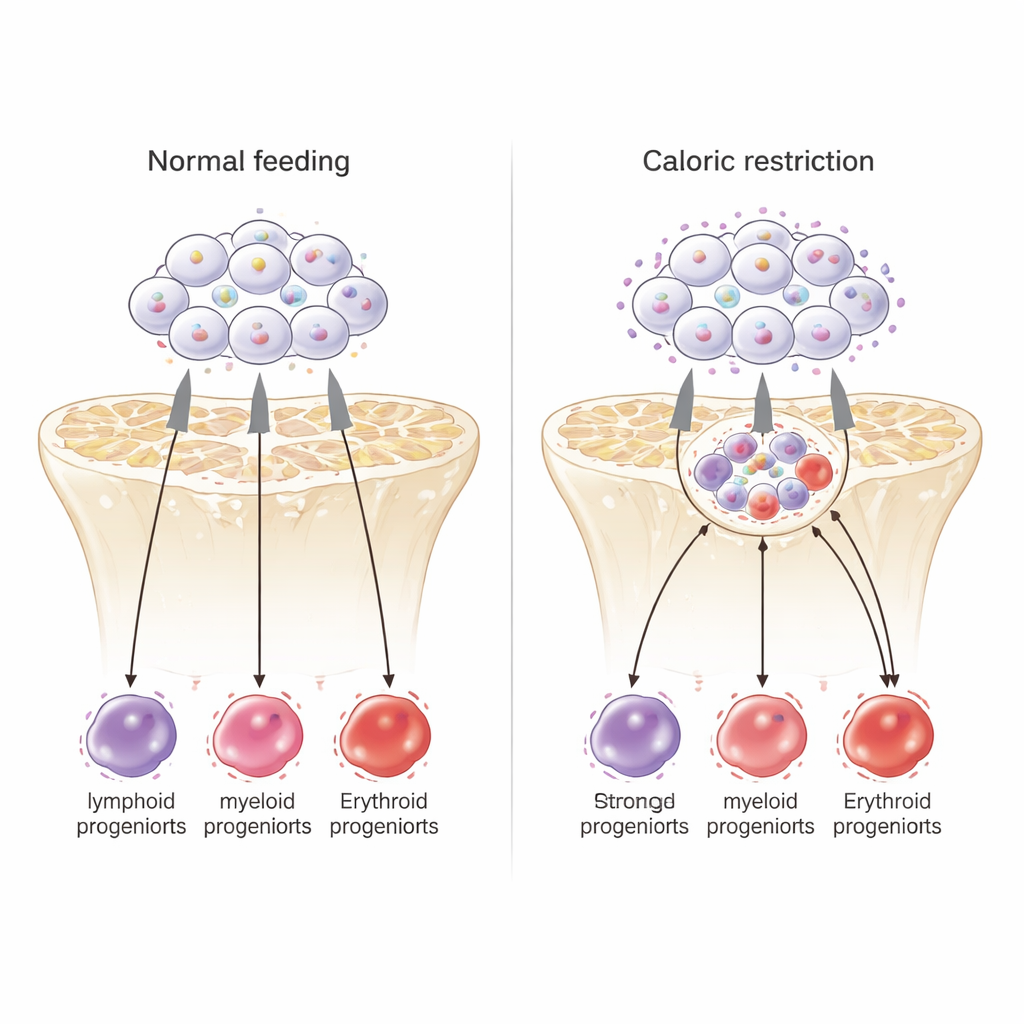
En intern trafikpolis finjusterar svaret
För att hitta interna kontrollpunkter undersökte forskarna hur åtkomligt DNA var över stamcellernas genom och var en nyckeltranskriptionsfaktor, PU.1, satt bunden. Vid kalorirestriktion blev många DNA‑regioner mer öppna och visade starkare PU.1‑bindning. Gener nära dessa PU.1‑ställen var berikade för cellcykelkontroll och för vägar som styr celler mot röda blodceller och andra myeloida öden, medan gener kopplade till djup stamcellsdvala tenderade att vara repressiva. Ungefär hälften av de gener som svarade när Kdr släcktes visade PU.1 i närheten, och PU.1 själv bundet nära Kdr‑genen, vilket antyder en feedback‑slinga. Tillsammans positionerar dessa data PU.1 som en intern trafikpolis som, i sammanhanget av sänkt KDR‑signalering, omdirigerar åldrande stamceller mot ett kalorirestriktionsliknande, ungdomligt tillstånd som gynnar överlevnadsorienterade blodceller.
Vad detta betyder för sund åldring
Detta arbete målar en nyanserad bild av hur långvarig kalorirestriktion påverkar vår blodfabrik. Hos hanmöss driver minskat ätande stamceller att prioritera produktion av röda celler, trombocyter och snabbt verkande immunceller samtidigt som antikroppsproducerande celler hämmas, vilket kan förklara försvagade svar på infektioner under strikta dieter. Samtidigt hjälper noggrant riktade epigenetiska förändringar vid gener som Kdr och skift i PU.1‑aktivitet till att bevara ett mer ungdomligt genprogram i dessa stamceller. Även om studien gjordes i möss och endast på hanar, antyder den att framtida terapier skulle kunna efterlikna de gynnsamma molekylära effekterna av kalorirestriktion på blodbildande stamceller — utan att kräva extrem diet eller offra immunbeskyddet.
Citering: Zong, L., Park, B., Tekin-Turhan, F. et al. Epigenetic profiling of hematopoietic stem cells from male mice identifies KDR and PU.1 as regulators of aging transcriptome and caloric restriction response. Nat Commun 17, 2978 (2026). https://doi.org/10.1038/s41467-026-69718-0
Nyckelord: kalorirestriktion, hematopoetiska stamceller, immunåldring, epigenetik, PU.1 och KDR