Clear Sky Science · it
Profilo epigenetico delle cellule staminali ematopoietiche di topi maschi identifica KDR e PU.1 come regolatori del trascrittoma dell'invecchiamento e della risposta alla restrizione calorica
Perché mangiare meno potrebbe rimodellare il nostro sangue
Ridurre le calorie senza incorrere in malnutrizione si è dimostrato in grado di estendere la durata della vita in numerosi animali, e alcune persone adottano diete rigorose nella speranza di vivere più a lungo. Ma mangiare meno può anche indebolire il sistema immunitario. Questo studio pone una domanda semplice ma importante: in che modo la riduzione calorica a lungo termine modifica le cellule staminali nel midollo osseo che ricostruiscono costantemente il sangue e il sistema immunitario, e tali cambiamenti possono aiutare a mantenere queste cellule “giovani” pur proteggendo l'organismo?
Come è stato impostato lo studio nei topi
I ricercatori hanno lavorato con topi maschi che o mangiavano liberamente o seguivano per tutta la vita una dieta con circa il 40% di calorie in meno, iniziata in giovane età adulta. Alcuni dei topi con restrizione calorica sono stati poi riforniti con cibo libero, per osservare quanto rapidamente il loro sistema ematopoietico si riprendeva. Il team ha misurato i conteggi ematici, esaminato le popolazioni cellulari nel midollo osseo e profilato l'attività genica e i marchi epigenetici — tag chimici su DNA e proteine che aiutano a controllare quali geni sono attivi — nelle rare cellule staminali ematopoietiche che danno origine a tutte le cellule del sangue.
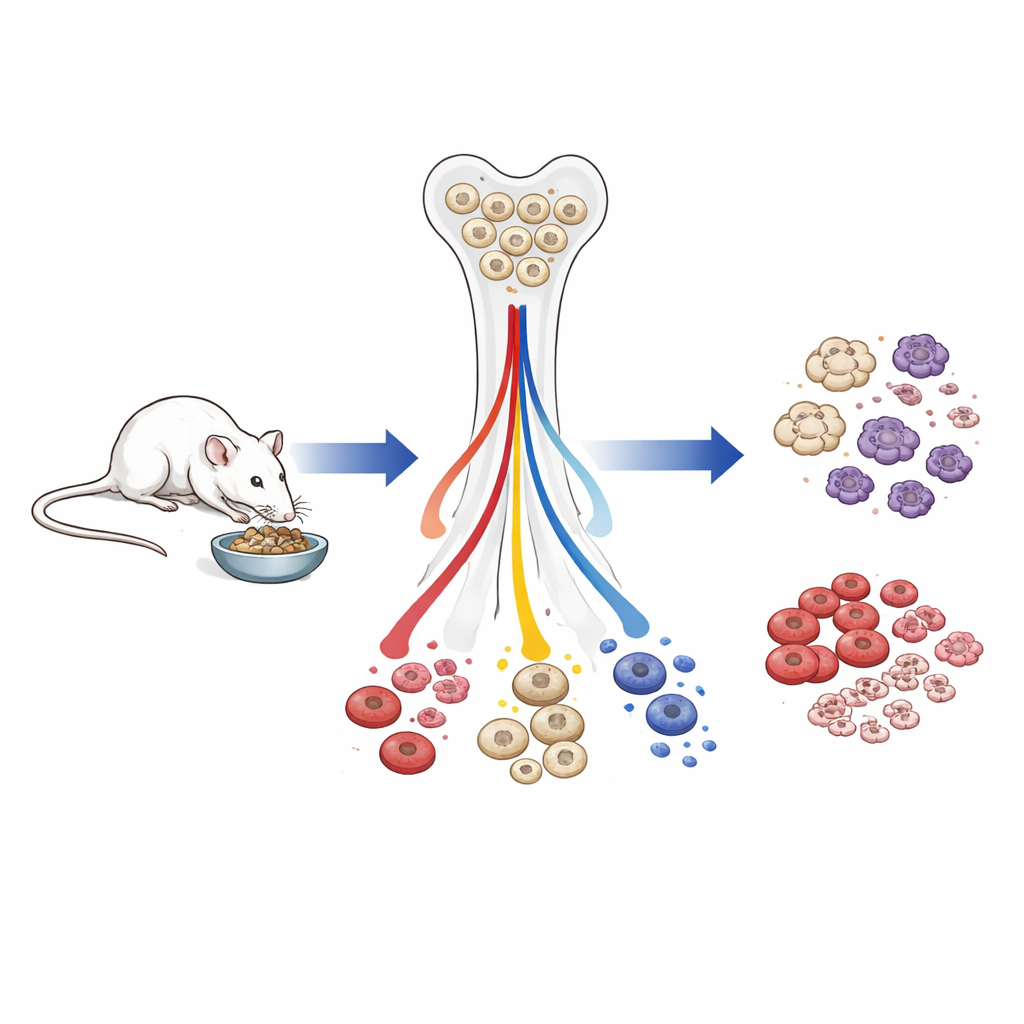
Meno globuli bianchi totali, ma le cellule vitali sono protette
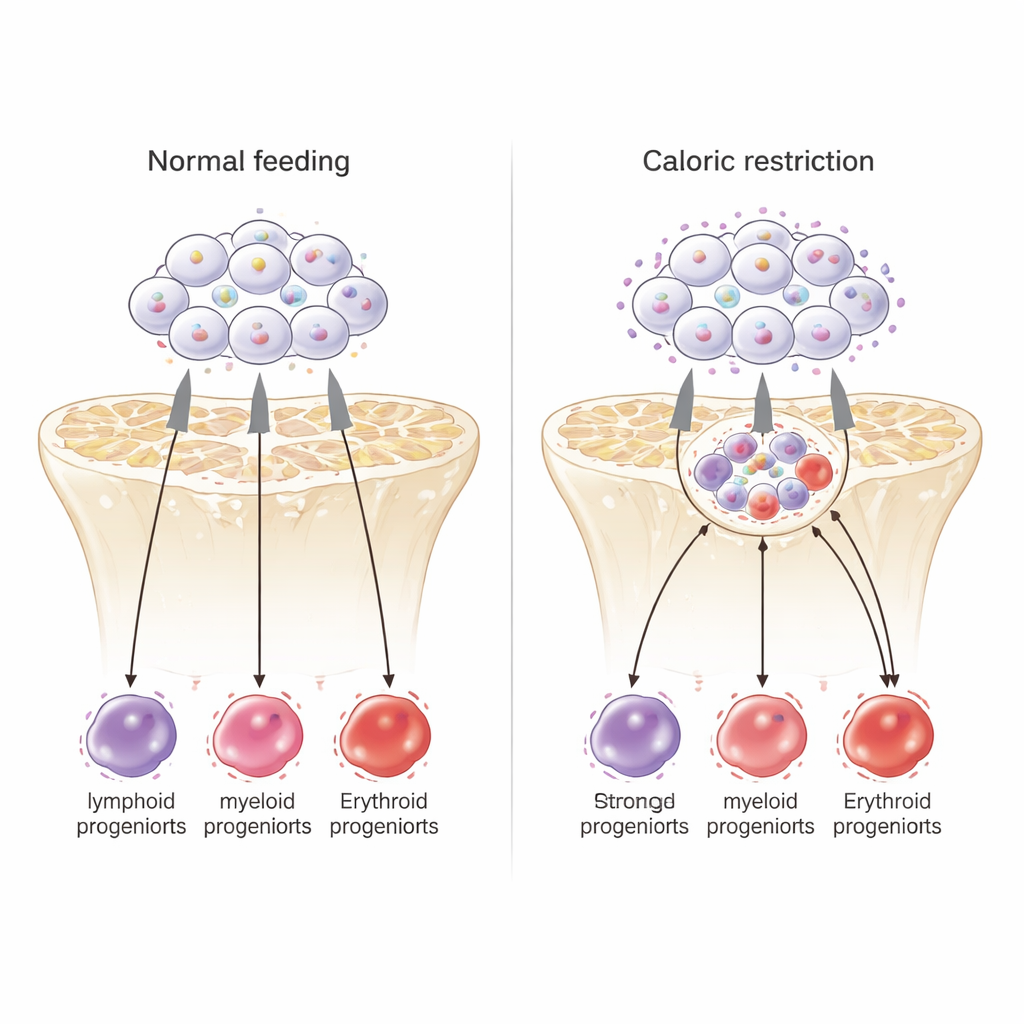
Nei topi anziani che avevano passato la maggior parte della loro vita con meno calorie, il numero complessivo di globuli bianchi nel sangue è diminuito. Sia le cellule della risposta innata sia quelle della risposta adattativa sono calate, ma non allo stesso modo. Le cellule importanti per la sopravvivenza immediata — i globuli rossi che trasportano ossigeno, le piastrine che coagulano il sangue e i difensori mieloidi di prima linea come i granulociti — sono risultate relativamente preservate. Al contrario, le cellule linfoidi, in particolare i linfociti B che sostengono la risposta anticorpale, sono state fortemente ridotte dai progenitori precoci nel midollo osseo fino alle cellule mature nel sangue. Quando gli animali a restrizione calorica sono stati rialimentati per sole quattro settimane, i conteggi dei globuli bianchi e le dimensioni della milza sono in gran parte ritornati, e la produzione linfoide è aumentata, dimostrando che molte di queste modificazioni sono rapidamente reversibili.
Le staminali lavorano di più e scelgono destini diversi
Contro le aspettative, le cellule staminali al vertice della gerarchia ematica non sono diventate più dormienti in condizioni di carenza alimentare; al contrario, hanno aumentato il loro ciclo proliferativo. Analisi dettagliate dell'espressione genica hanno rivelato che, sotto restrizione calorica, queste staminali hanno attenuato programmi legati all'auto-rinnovamento a lungo termine e hanno invece aumentato geni associati a cellule staminali a breve termine e a progenitori che generano lignaggi mieloidi e eritroidi. In altre parole, le staminali sono state spinte a lavorare di più nel breve periodo per mantenere i tipi cellulari critici per la sopravvivenza, a scapito del loro rinnovamento lento o della produzione di cellule linfoidi. Eppure, nonostante questo aumento di attività, il loro profilo complessivo di espressione genica somigliava più a quello di staminali giovani che di staminali vecchie.
Ripristinare i programmi dell'invecchiamento tramite interruttori epigenetici
Il gruppo ha quindi indagato come il mangiare meno potesse rendere le staminali vecchie molecularmente più giovani. Hanno mappato due marchi istonici comuni che in generale promuovono o reprimono l'attività genica. Sebbene entrambi i marchi fossero globalmente ridotti nelle staminali soggette a restrizione calorica, un piccolo insieme di geni associati all'invecchiamento ha guadagnato un marchio repressivo e perso uno attivante. Due geni sono emersi come particolarmente rilevanti: Kdr, che codifica per un recettore dei segnali di crescita dei vasi sanguigni, e Bmpr1a, un altro recettore di superficie cellulare. Sotto restrizione calorica, entrambi i geni risultavano più strettamente silenziati. Quando i ricercatori hanno sperimentalmente ridotto l'espressione di Kdr e Bmpr1a in staminali anziane provenienti da topi alimentati normalmente e hanno trapiantato queste cellule nei riceventi, le cellule hanno adottato un profilo di espressione genica simile a quello delle staminali da animali a restrizione calorica, suggerendo che questi recettori contribuiscono al programma dell'invecchiamento e possono essere modulati epigeneticamente.
Un vigile interno modula la risposta
Per scoprire punti di controllo interni, gli scienziati hanno esaminato l'accessibilità del DNA nel genoma delle staminali e dove si legava un fattore di trascrizione chiave, PU.1. In condizioni di restrizione calorica molte regioni del DNA sono diventate più aperte e hanno mostrato un legame più forte di PU.1. I geni vicini a questi siti di PU.1 risultavano arricchiti per il controllo del ciclo cellulare e per percorsi che indirizzano le cellule verso lignaggi eritroidi e altri fati mieloidi, mentre i geni associati alla profonda quiescenza delle staminali tendevano a essere repressi. Circa la metà dei geni che rispondevano alla riduzione di Kdr mostrava PU.1 nelle vicinanze, e lo stesso PU.1 si legava vicino al gene Kdr, suggerendo un anello di retroazione. Complessivamente, questi dati fanno emergere PU.1 come un vigile interno che, nel contesto di un segnale KDR ridotto, reindirizza le staminali invecchiate verso uno stato simile a quello delle staminali da restrizione calorica, favorevole alla produzione di cellule ematiche orientate alla sopravvivenza.
Cosa significa per un invecchiamento sano
Questo lavoro dipinge un quadro sfumato di come il taglio calorico a lungo termine influenzi la nostra “fabbrica del sangue”. Nei topi maschi, mangiare meno spinge le staminali a dare priorità alla produzione di globuli rossi, piastrine e cellule immunitarie ad azione rapida, pur limitando le cellule produttrici di anticorpi, il che potrebbe spiegare risposte indebolite alle infezioni sotto diete rigide. Allo stesso tempo, cambiamenti epigenetici mirati in geni come Kdr e modifiche nell'attività di PU.1 contribuiscono a preservare un programma genico più giovanile in queste staminali. Sebbene lo studio sia stato condotto nei topi e solo nei maschi, suggerisce che terapie future potrebbero mirare a imitare gli effetti molecolari benefici della restrizione calorica sulle cellule staminali ematopoietiche — senza richiedere diete estreme o sacrificare la protezione immunitaria.
Citazione: Zong, L., Park, B., Tekin-Turhan, F. et al. Epigenetic profiling of hematopoietic stem cells from male mice identifies KDR and PU.1 as regulators of aging transcriptome and caloric restriction response. Nat Commun 17, 2978 (2026). https://doi.org/10.1038/s41467-026-69718-0
Parole chiave: restrizione calorica, cellule staminali ematopoietiche, invecchiamento del sistema immunitario, epigenetica, PU.1 e KDR