Clear Sky Science · pl
Profilowanie epigenetyczne komórek macierzystych układu krwiotwórczego u samców myszy identyfikuje KDR i PU.1 jako regulatorów starzejącego się transkryptomu i odpowiedzi na ograniczenie kalorii
Dlaczego jedzenie mniej może przekształcić naszą krew
Redukcja kalorii bez niedożywienia wydłuża życie u wielu zwierząt, a niektórzy ludzie decydują się na rygorystyczne diety w nadziei na dłuższe życie. Jednak jedzenie mniej może też osłabić układ odpornościowy. W tym badaniu zadano proste, ale istotne pytanie: jak długotrwałe ograniczenie kalorii zmienia komórki macierzyste w szpiku kostnym, które nieustannie odbudowują naszą krew i układ odpornościowy, i czy te zmiany mogą pomagać utrzymać te komórki „młodymi” przy jednoczesnej ochronie organizmu?
Jak zaplanowano eksperyment u myszy
Naukowcy pracowali z samcami myszy, które albo jadły swobodnie, albo były trzymane na dożywotniej diecie o około 40% mniejszej liczbie kalorii, rozpoczynając w wczesnej dorosłości. Niektóre myszy z ograniczoną kalorycznością zostały później ponownie dopuszczone do swobodnego jedzenia, by sprawdzić, jak szybko ich układ krwiotwórczy się odradza. Zespół mierzył liczby krwi, badał populacje komórek w szpiku i profilował aktywność genów oraz znaczniki epigenetyczne — chemiczne etykiety na DNA i białkach, które pomagają kontrolować, które geny są aktywne — w rzadkich komórkach macierzystych hematopoetycznych, dających początek wszystkim komórkom krwi.
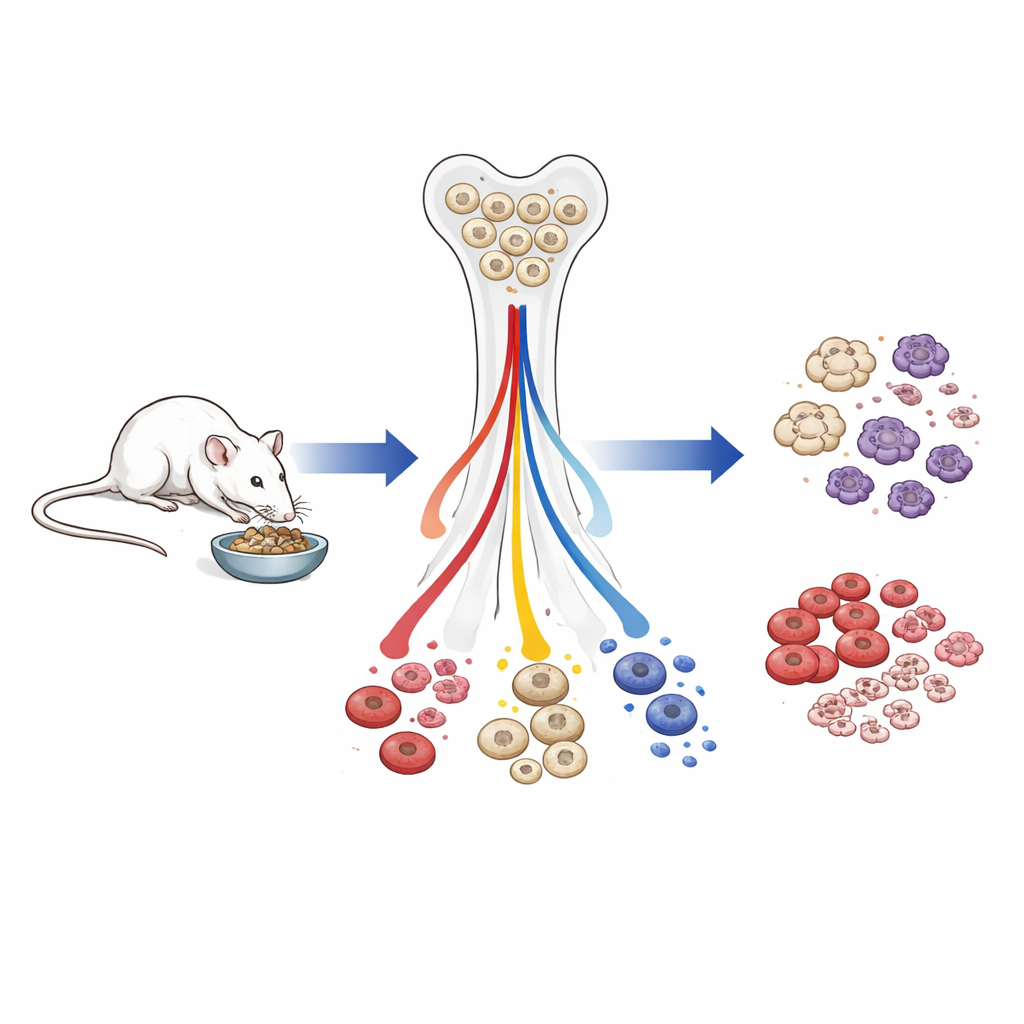
Mniej białych krwinek, ale chronione są komórki kluczowe dla przeżycia
U starszych myszy, które większość życia spędziły na ograniczonej diecie, ogólna liczba białych krwinek we krwi spadła. Zarówno komórki odpornościowe wrodzone, jak i nabyte zmniejszyły się, ale nie w jednakowym stopniu. Komórki ważne dla natychmiastowego przeżycia — erytrocyty przenoszące tlen, płytki krwi biorące udział w krzepnięciu oraz pierwszorzutowi obrońcy mieloidowi, tacy jak granulocyty — były stosunkowo zachowane. Natomiast komórki limfoidalne, zwłaszcza limfocyty B odpowiadające za produkcję przeciwciał, były silnie zredukowane już od wczesnych prekursorów w szpiku aż po dojrzałe komórki we krwi. Gdy zwierzęta na ograniczonej diecie zostały dokarmione przez zaledwie cztery tygodnie, liczba białych krwinek i wielkość śledziony w dużej mierze wróciły do normy, a produkcja limfoidalna gwałtownie wzrosła, co pokazuje, że wiele z tych zmian jest szybko odwracalnych.
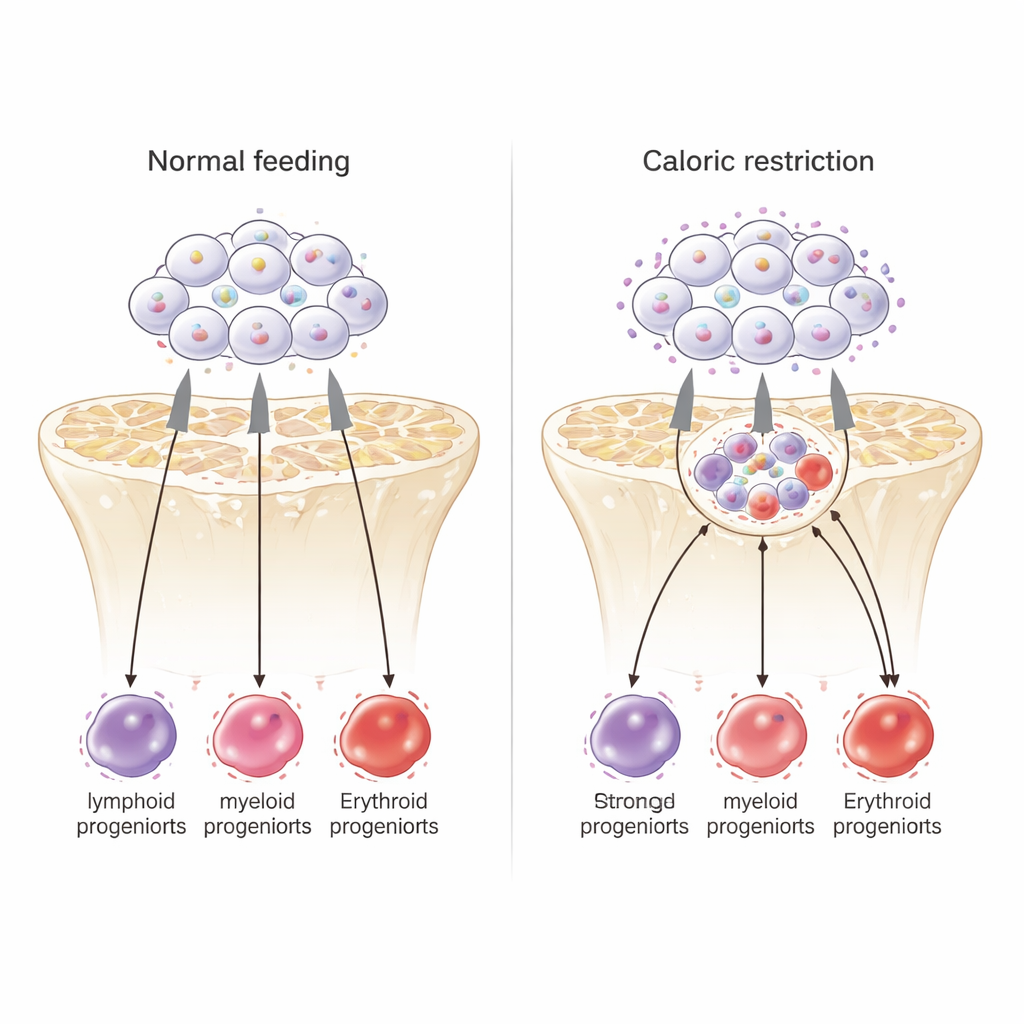
Komórki macierzyste pracują więcej i wybierają inne losy
Zaskakująco, komórki macierzyste na szczycie hierarchii krwiotwórczej nie stały się bardziej uśpione w warunkach niedoboru pokarmu; przeciwnie — częściej wchodziły w cykl komórkowy. Szczegółowe analizy ekspresji genów wykazały, że pod ograniczeniem kalorii te komórki zmniejszyły aktywność programów związanych z długoterminową samoodnową i zwiększyły ekspresję genów powiązanych z krótkoterminowymi komórkami macierzystymi i prekursorami tworzącymi linie mieloidalne i erytrocytarne. Innymi słowy, komórki macierzyste zostały zmuszone do intensywniejszej pracy w krótkim terminie, aby utrzymać kluczowe typy komórek niezbędnych do przeżycia, kosztem powolnej odnowy siebie samych lub wytwarzania komórek limfoidalnych. Mimo tego dodatkowego wysiłku ich ogólny wzorzec aktywności genów przypominał bardziej profil młodych komórek macierzystych niż starych.
Resetowanie programów starzenia przez epigenetyczne przełączniki
Zespół zapytał następnie, jak ograniczenie kalorii może sprawić, że stare komórki macierzyste wyglądają molekularnie młodziej. Zmapowali dwa powszechne modyfikatory histonowe, które zazwyczaj promują lub tłumią aktywność genów. Chociaż oba markery były globalnie zmniejszone w komórkach macierzystych z diety ograniczającej kalorie, niewielki zestaw genów powiązanych ze starzeniem zyskał znak represyjny i stracił aktywujący. Dwa wyróżniały się: Kdr, który koduje receptor dla sygnałów wzrostu naczyń krwionośnych, oraz Bmpr1a, inny receptor obecny na powierzchni komórek. Pod ograniczeniem kalorii oba geny były silniej wyciszone. Gdy badacze eksperymentalnie obniżyli poziomy Kdr i Bmpr1a w postarzałych komórkach macierzystych z myszy karmionych normalnie i przeszczepili te komórki do biorców, przyjęły one wzorzec ekspresji genów podobny do komórek z ograniczoną kalorycznością, co sugeruje, że te receptory napędzają program starzenia i można je epigenetycznie regulować.
Wewnętrzny „policjant ruchu” reguluje odpowiedź
Aby odkryć wewnętrzne punkty kontrolne, naukowcy zbadali dostępność DNA w całym genomie komórek macierzystych oraz miejsca wiązania kluczowego czynnika transkrypcyjnego PU.1. Pod ograniczeniem kalorii wiele regionów DNA stało się bardziej otwartych i wykazywało silniejsze wiązanie PU.1. Geny w pobliżu tych miejsc PU.1 były wzbogacone w funkcje kontrolujące cykl komórkowy oraz szlaki kierujące komórki w stronę erytro- i innych losów mieloidalnych, podczas gdy geny związane z głęboką uśpieniem komórek macierzystych miały tendencję do represji. Około połowa genów reagujących na obniżenie Kdr miała w pobliżu miejsca PU.1, a sam PU.1 wiązał się blisko genu Kdr, co sugeruje sprzężenie zwrotne. Razem dane te stawiają PU.1 w roli wewnętrznego „policjanta ruchu”, który w kontekście zmniejszonego sygnału KDR przekierowuje starzejące się komórki macierzyste ku stanowi przypominającemu ograniczenie kalorii — młodszemu programowi sprzyjającemu komórkom krwi ukierunkowanym na przetrwanie.
Co to oznacza dla zdrowego starzenia
Praca ta przedstawia zniuansowany obraz wpływu długotrwałego ograniczenia kalorii na naszą „fabrykę krwi”. U samców myszy jedzenie mniej skłania komórki macierzyste do priorytetowego wytwarzania erytrocytów, płytek krwi i szybkodziałających komórek odpornościowych, jednocześnie ograniczając komórki produkujące przeciwciała, co może wyjaśniać osłabione odpowiedzi na infekcje przy rygorystycznych dietach. Równocześnie precyzyjnie ukierunkowane zmiany epigenetyczne w genach takich jak Kdr oraz przesunięcia w aktywności PU.1 pomagają zachować bardziej młodzieńczy program genowy w tych komórkach macierzystych. Chociaż badanie przeprowadzono na myszach i tylko na samcach, sugeruje, że przyszłe terapie mogłyby dążyć do naśladowania korzystnych molekularnych efektów ograniczenia kalorii w komórkach tworzących krew — bez konieczności ekstremalnego odżywiania czy poświęcania ochrony odpornościowej.
Cytowanie: Zong, L., Park, B., Tekin-Turhan, F. et al. Epigenetic profiling of hematopoietic stem cells from male mice identifies KDR and PU.1 as regulators of aging transcriptome and caloric restriction response. Nat Commun 17, 2978 (2026). https://doi.org/10.1038/s41467-026-69718-0
Słowa kluczowe: ograniczenie kalorii, komórki macierzyste układu krwiotwórczego, starzenie się układu odpornościowego, epigenetyka, PU.1 i KDR