Clear Sky Science · pt
Perfil epigenético de células-tronco hematopoéticas de camundongos machos identifica KDR e PU.1 como reguladores do transcriptoma do envelhecimento e da resposta à restrição calórica
Por que comer menos pode remodelar nosso sangue
Reduzir calorias sem ficar desnutrido tem demonstrado prolongar a vida em muitos animais, e algumas pessoas adotam dietas rigorosas na esperança de viver mais. Mas comer menos também pode enfraquecer o sistema imunológico. Este estudo faz uma pergunta simples, porém importante: como a redução calórica de longo prazo altera as células-tronco na medula óssea que constantemente reconstroem nosso sangue e sistema imune, e essas mudanças podem ajudar a manter essas células "jovens" enquanto ainda nos protegem?
Como o estudo foi conduzido em camundongos
Os pesquisadores trabalharam com camundongos machos que comiam à vontade ou foram mantidos em uma dieta ao longo da vida com cerca de 40% menos calorias, iniciada no início da vida adulta. Alguns dos animais com restrição calórica posteriormente voltaram a comer livremente, para verificar com que rapidez seu sistema sanguíneo se recuperava. A equipe mediu contagens sanguíneas, examinou populações celulares na medula óssea e perfilou atividade gênica e marcas epigenéticas — marcadores químicos no DNA e nas proteínas que ajudam a controlar quais genes estão ativos — nas raras células-tronco hematopoéticas que dão origem a todas as células sanguíneas.
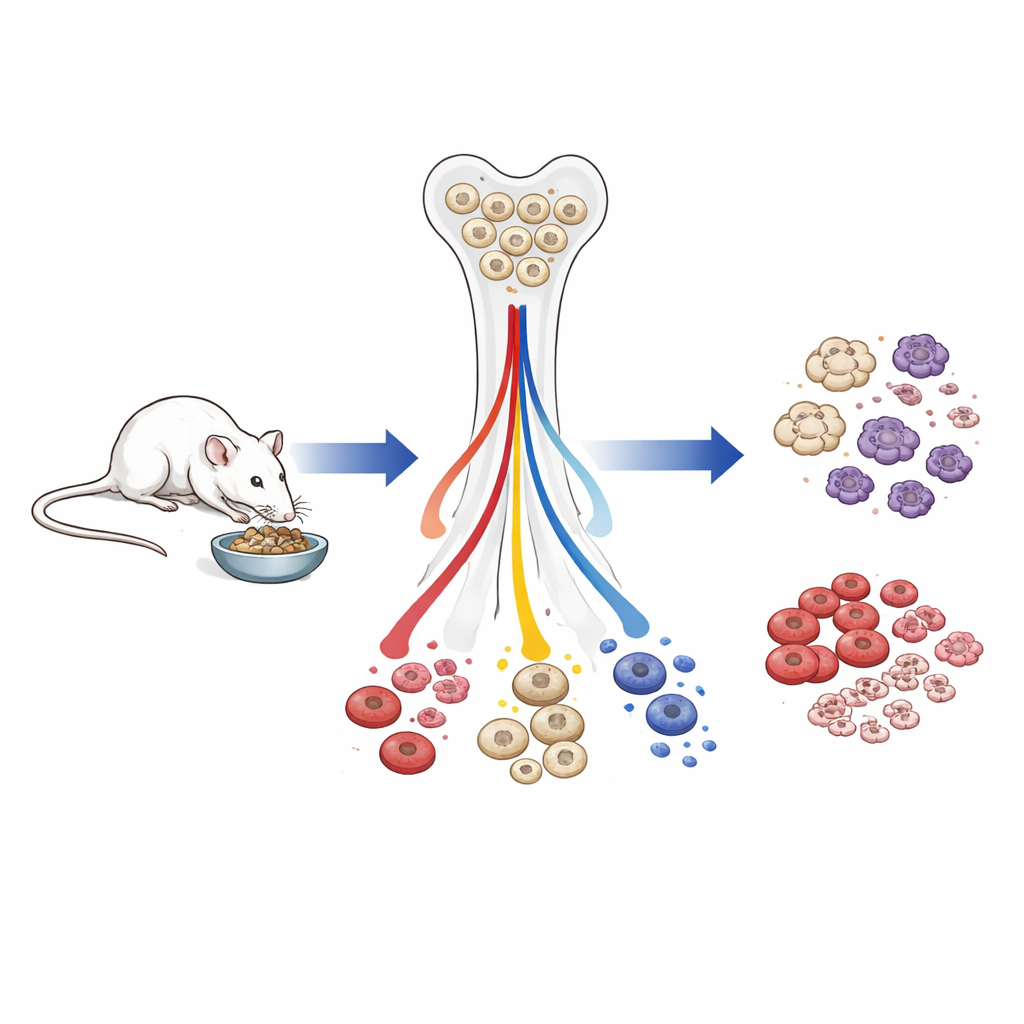
Menos glóbulos brancos no total, mas células essenciais são preservadas
Em camundongos mais velhos que passaram a maior parte da vida com menos calorias, o número total de leucócitos na corrente sanguínea caiu. Tanto células da imunidade inata quanto adaptativa diminuíram, mas não na mesma proporção. Células importantes para a sobrevivência imediata — glóbulos vermelhos que transportam oxigênio, plaquetas que promovem a coagulação e defesas mieloides de linha de frente como granulócitos — foram relativamente preservadas. Em contraste, células linfoides, especialmente células B que sustentam respostas de anticorpos, foram fortemente reduzidas desde progenitores precoces na medula óssea até células maduras no sangue. Quando animais em restrição calórica foram realimentados por apenas quatro semanas, as contagens de leucócitos e o tamanho do baço rebateram em grande parte, e a produção linfoide aumentou significativamente, mostrando que muitas dessas mudanças são rapidamente reversíveis.
Células-tronco trabalham mais e escolhem destinos diferentes
Surpreendentemente, as células-tronco no topo da hierarquia sanguínea não se tornaram mais dormentes com a escassez de alimento; em vez disso, passaram a ciclar mais ativamente. Análises detalhadas de expressão gênica revelaram que, sob restrição calórica, essas células reduziram programas ligados à autorrenovação de longo prazo e aumentaram genes associados a células-tronco de curto prazo e progenitores que geram linhagens mieloides e eritróides. Em outras palavras, as células-tronco foram pressionadas a trabalhar mais no curto prazo para manter tipos celulares essenciais à sobrevivência, em detrimento da renovação lenta de si mesmas ou da geração de células linfoides. Ainda assim, apesar desse trabalho extra, seu padrão geral de atividade gênica parecia mais similar ao de células-tronco jovens do que ao de velhas.
Reprogramação de programas de envelhecimento via chaves epigenéticas
A equipe então investigou como comer menos poderia fazer com que células-tronco velhas parecessem molecularmente mais jovens. Mapearam duas marcas de histona comuns que, em geral, promovem ou reprimem a atividade gênica. Embora ambas as marcas estivessem globalmente reduzidas em células-tronco de animais com restrição calórica, um pequeno conjunto de genes associados ao envelhecimento ganhou uma marca repressora e perdeu uma ativadora. Dois se destacaram: Kdr, que codifica um receptor para sinais de crescimento vascular, e Bmpr1a, outro receptor de superfície celular. Sob restrição calórica, ambos os genes foram mais firmemente silenciados. Quando os pesquisadores reduziram experimentalmente Kdr e Bmpr1a em células-tronco envelhecidas de camundongos com alimentação normal e transplantaram essas células em receptores, as células adotaram um padrão de expressão gênica que lembrava o das células-tronco com restrição calórica, sugerindo que esses receptores ajudam a dirigir o programa de envelhecimento e podem ser ajustados epigeneticamente.
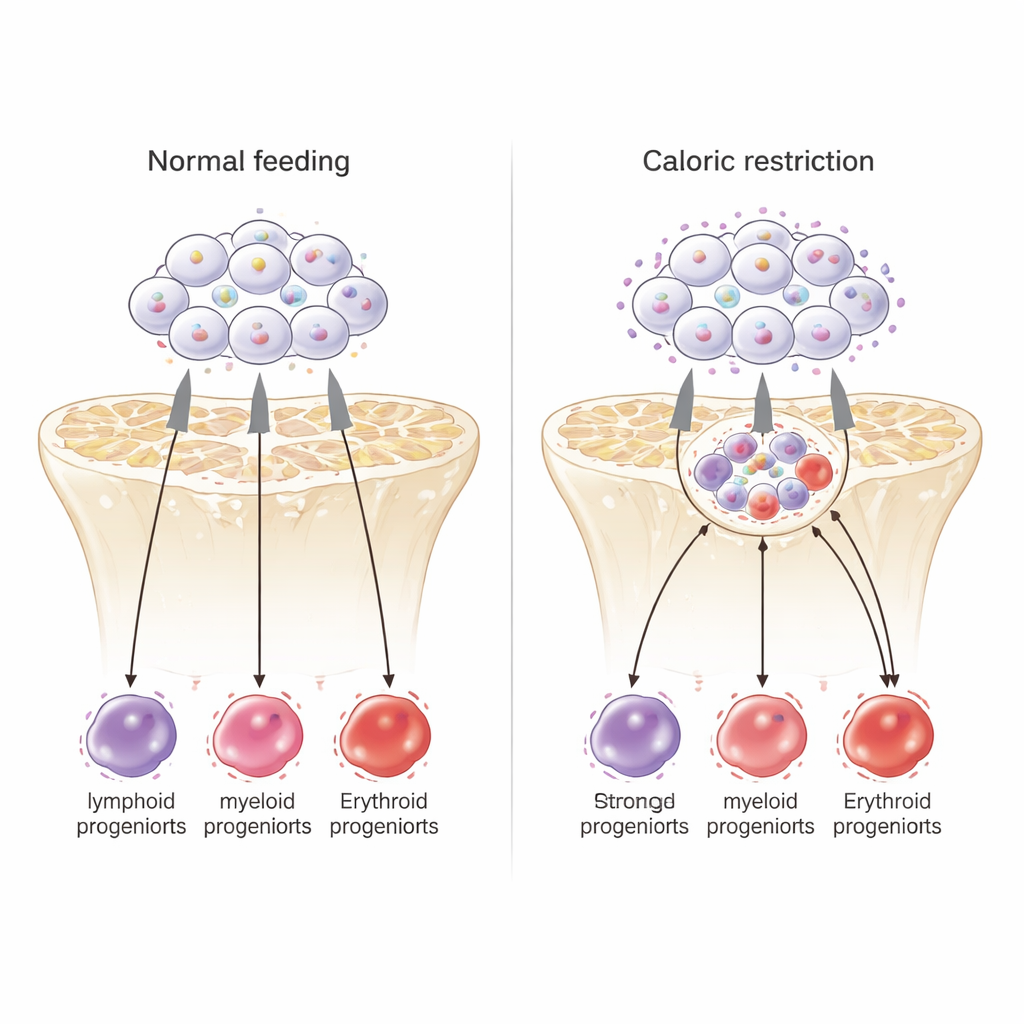
Um controlador interno regula a resposta
Para descobrir pontos de controle internos, os cientistas examinaram quão acessível o DNA estava ao longo do genoma das células-tronco e onde um fator de transcrição chave, PU.1, estava ligado. Com restrição calórica, muitas regiões de DNA tornaram-se mais abertas e mostraram ligação mais forte de PU.1. Genes próximos a esses sítios de PU.1 foram enriquecidos para controle do ciclo celular e vias que direcionam células para destinos eritróides e outras linhagens mieloides, enquanto genes associados à quiescência profunda das células-tronco tenderam a ser reprimidos. Cerca de metade dos genes que responderam à redução de Kdr apresentaram PU.1 nas proximidades, e o próprio PU.1 ligou-se próximo ao gene Kdr, sugerindo um circuito de retroalimentação. Em conjunto, esses dados posicionam PU.1 como um fiscal interno do tráfego que, no contexto de sinalização KDR reduzida, redireciona células-tronco envelhecidas para um estado semelhante ao da restrição calórica, mais jovem e favorável à produção de células sanguíneas orientadas à sobrevivência.
O que isso significa para um envelhecimento saudável
Este trabalho oferece um retrato nuançado de como o corte calórico de longo prazo afeta nossa "fábrica" de sangue. Em camundongos machos, comer menos empurra as células-tronco a priorizar a produção de eritrócitos, plaquetas e células imunes de ação rápida enquanto reprime células produtoras de anticorpos, o que pode explicar respostas enfraquecidas a infecções sob dietas rigorosas. Ao mesmo tempo, mudanças epigenéticas direcionadas em genes como Kdr e alterações na atividade de PU.1 ajudam a preservar um programa gênico mais juvenil nessas células-tronco. Embora o estudo tenha sido realizado em camundongos e apenas em machos, sugere que terapias futuras poderiam visar imitar os efeitos moleculares benéficos da restrição calórica sobre células-tronco formadoras de sangue — sem exigir dietas extremas ou sacrificar a proteção imunológica.
Citação: Zong, L., Park, B., Tekin-Turhan, F. et al. Epigenetic profiling of hematopoietic stem cells from male mice identifies KDR and PU.1 as regulators of aging transcriptome and caloric restriction response. Nat Commun 17, 2978 (2026). https://doi.org/10.1038/s41467-026-69718-0
Palavras-chave: restrição calórica, células-tronco hematopoéticas, envelhecimento do sistema imune, epigenética, PU.1 e KDR