Clear Sky Science · fr
Profil épigénétique des cellules souches hématopoïétiques de souris mâles identifie KDR et PU.1 comme régulateurs du transcriptome du vieillissement et de la réponse à la restriction calorique
Pourquoi manger moins pourrait remodeler notre sang
Réduire les calories sans tomber en malnutrition prolonge la durée de vie chez de nombreux animaux, et certaines personnes adoptent des régimes stricts dans l’espoir de vivre plus longtemps. Mais moins manger peut aussi affaiblir le système immunitaire. Cette étude pose une question simple mais importante : comment une réduction calorique prolongée modifie-t-elle les cellules souches de la moelle osseuse qui reconstituent en permanence notre sang et notre immunité, et ces changements peuvent-ils aider à maintenir ces cellules « jeunes » tout en nous protégeant ?
Conception de l’étude chez la souris
Les chercheurs ont travaillé avec des souris mâles qui mangeaient librement ou qui suivaient tout au long de leur vie un régime réduisant d’environ 40 % les calories, commencé au début de l’âge adulte. Certaines souris en restriction calorique ont ensuite été réalimentées librement pour observer la rapidité de la récupération du système sanguin. L’équipe a mesuré les numérations sanguines, examiné les populations cellulaires de la moelle osseuse et profilé l’activité génique ainsi que les marques épigénétiques — des étiquettes chimiques sur l’ADN et les protéines qui régulent l’activation des gènes — dans les rares cellules souches hématopoïétiques à l’origine de toutes les cellules sanguines.
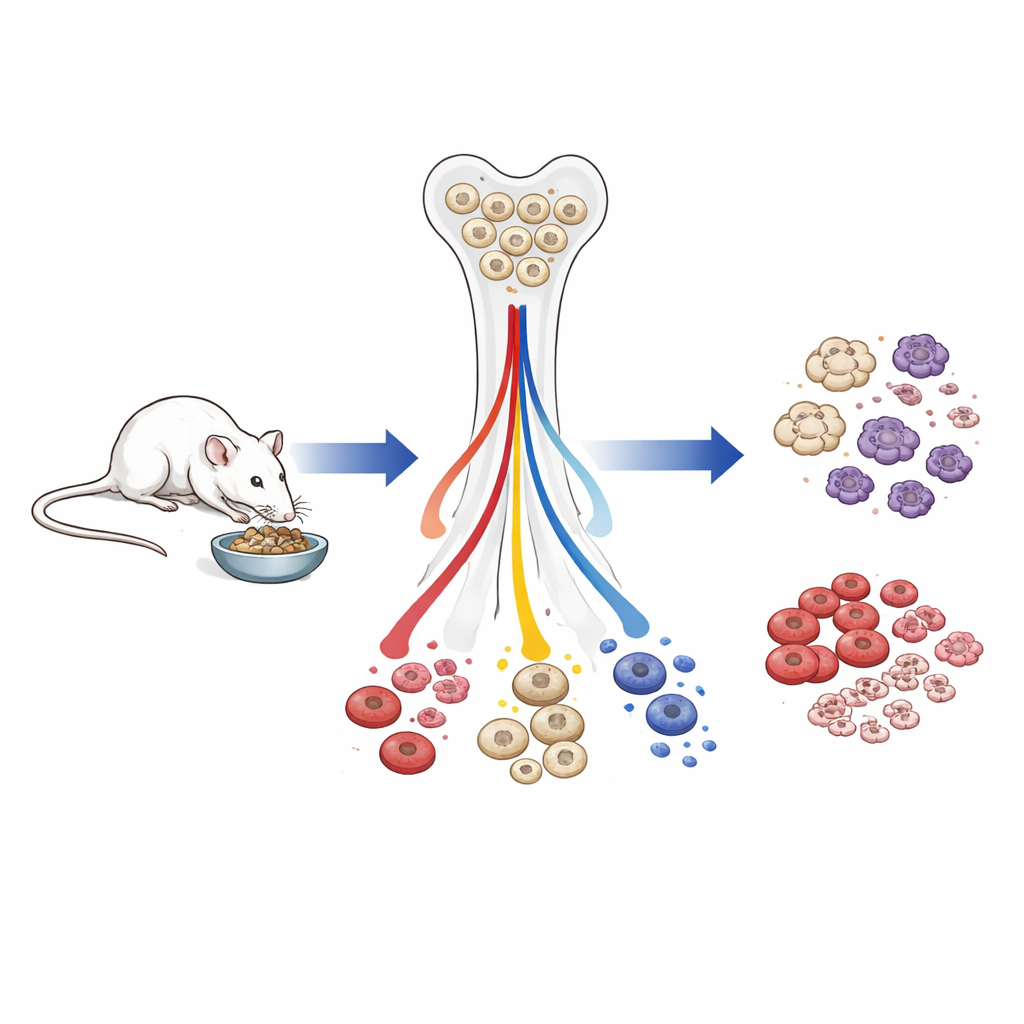
Moins de globules blancs au total, mais les cellules vitales sont protégées
Chez les souris âgées ayant passé la majeure partie de leur vie avec moins de calories, le nombre total de globules blancs dans le sang a diminué. Les cellules du système immunitaire inné et adaptatif ont chuté, mais pas à égalité. Les cellules importantes pour la survie immédiate — les globules rouges qui transportent l’oxygène, les plaquettes qui participent à la coagulation et les effecteurs myéloïdes de première ligne comme les granulocytes — ont été relativement préservées. En revanche, les cellules lymphoïdes, en particulier les cellules B qui produisent les anticorps, ont été fortement réduites depuis les progéniteurs précoces de la moelle jusqu’aux cellules matures circulantes. Lorsque les animaux soumis à la restriction calorique ont été réalimentés pendant seulement quatre semaines, les numérations de globules blancs et la taille de la rate sont en grande partie revenues et la production lymphoïde a rebondi, montrant que bon nombre de ces modifications sont rapidement réversibles.
Les cellules souches travaillent davantage et choisissent d’autres destinées
De manière surprenante, les cellules souches au sommet de la hiérarchie sanguine ne sont pas devenues plus dormantes en cas de restriction alimentaire ; au contraire, elles ont augmenté leur cycle d’activité. Des analyses détaillées de l’expression génique ont montré que, sous restriction calorique, ces cellules ont atténué les programmes liés au renouvellement à long terme et ont activé des gènes associés aux cellules souches à court terme et aux progéniteurs produisant les lignées myéloïdes et érythroïdes. Autrement dit, les cellules souches ont été poussées à travailler davantage à court terme pour maintenir les types cellulaires essentiels à la survie, au détriment de leur capacité à se renouveler lentement ou à générer des cellules lymphoïdes. Pourtant, malgré cet effort accru, leur profil global d’expression génique ressemblait davantage à celui de cellules souches jeunes qu’à celui de cellules âgées.
Réinitialiser les programmes du vieillissement par des commutateurs épigénétiques
L’équipe s’est ensuite demandé comment le fait de manger moins pouvait faire paraître les cellules souches âgées plus jeunes au niveau moléculaire. Ils ont cartographié deux marques d’histones courantes qui favorisent généralement ou répriment l’activité des gènes. Bien que les deux marques soient globalement réduites dans les cellules souches en restriction calorique, un petit ensemble de gènes associés au vieillissement a gagné une marque répressive et perdu une marque activatrice. Deux gènes se sont distingués : Kdr, qui code un récepteur pour les signaux de croissance des vaisseaux sanguins, et Bmpr1a, un autre récepteur de surface. Sous restriction calorique, ces deux gènes ont été plus strictement réprimés. Lorsque les chercheurs ont expérimenté une diminution de Kdr et Bmpr1a dans des cellules souches âgées provenant de souris nourries normalement puis transplanté ces cellules chez des receveurs, les cellules ont adopté un profil d’expression génique semblable à celui des cellules souches en restriction calorique, ce qui suggère que ces récepteurs contribuent au programme de vieillissement et peuvent être modulés épigénétiquement.
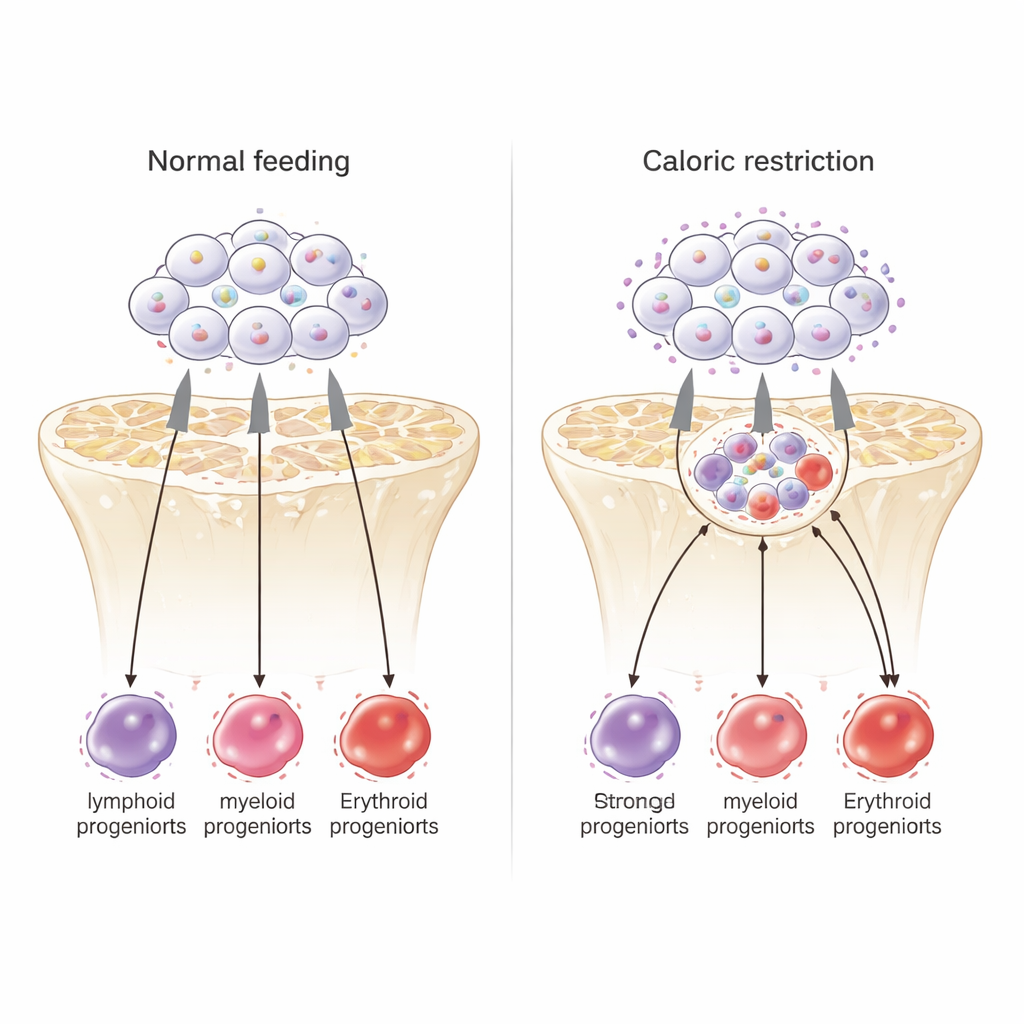
Un chef d’orchestre interne ajuste la réponse
Pour identifier des points de contrôle internes, les scientifiques ont examiné l’accessibilité de l’ADN à l’échelle du génome des cellules souches et les sites de liaison d’un facteur de transcription clé, PU.1. Sous restriction calorique, de nombreuses régions d’ADN sont devenues plus ouvertes et ont montré une liaison plus forte de PU.1. Les gènes proches de ces sites PU.1 étaient enrichis pour le contrôle du cycle cellulaire et pour des voies conduisant les cellules vers des destinées érythroïdes et autres lignées myéloïdes, tandis que les gènes associés à la quiescence profonde des cellules souches avaient tendance à être réprimés. Environ la moitié des gènes ayant répondu à la diminution de Kdr présentaient un site PU.1 à proximité, et PU.1 lui-même se liait près du gène Kdr, suggérant une boucle de rétroaction. Ensemble, ces données positionnent PU.1 comme un chef d’orchestre interne qui, dans le contexte d’une signalisation KDR réduite, redirige les cellules souches vieillissantes vers un état semblable à celui induit par la restriction calorique, favorisant des cellules sanguines orientées vers la survie.
Implications pour un vieillissement en bonne santé
Ce travail dresse un tableau nuancé de la façon dont une restriction calorique prolongée affecte notre « usine » sanguine. Chez la souris mâle, manger moins pousse les cellules souches à prioriser la fabrication de globules rouges, de plaquettes et de cellules immunitaires à action rapide tout en freinant les cellules productrices d’anticorps, ce qui peut expliquer une réponse affaiblie aux infections sous régimes stricts. Parallèlement, des modifications épigénétiques ciblées de gènes tels que Kdr et des changements dans l’activité de PU.1 contribuent à préserver un programme génique plus jeune dans ces cellules souches. Bien que l’étude ait été menée chez la souris et uniquement sur des mâles, elle suggère que des thérapies futures pourraient tenter d’imiter les effets moléculaires bénéfiques de la restriction calorique sur les cellules souches hématopoïétiques — sans nécessiter des régimes extrêmes ni sacrifier la protection immunitaire.
Citation: Zong, L., Park, B., Tekin-Turhan, F. et al. Epigenetic profiling of hematopoietic stem cells from male mice identifies KDR and PU.1 as regulators of aging transcriptome and caloric restriction response. Nat Commun 17, 2978 (2026). https://doi.org/10.1038/s41467-026-69718-0
Mots-clés: restriction calorique, cellules souches hématopoïétiques, vieillissement du système immunitaire, épigénétique, PU.1 et KDR