Clear Sky Science · es
Perfil epigenético de células madre hematopoyéticas de ratones machos identifica a KDR y PU.1 como reguladores del transcriptoma del envejecimiento y de la respuesta a la restricción calórica
Por qué comer menos podría remodelar nuestra sangre
Reducir las calorías sin llegar a la desnutrición ha demostrado alargar la vida en muchos animales, y algunas personas incluso adoptan dietas estrictas con la esperanza de vivir más. Pero comer menos también puede debilitar el sistema inmunitario. Este estudio plantea una pregunta simple pero importante: ¿cómo cambia, a largo plazo, la reducción calórica las células madre de la médula ósea que reconstruyen constantemente nuestra sangre y sistema inmune, y pueden esos cambios ayudar a mantener estas células «jóvenes» sin dejar de protegernos?
Cómo se diseñó el estudio en ratones
Los investigadores trabajaron con ratones machos que o bien comían libremente o bien siguieron, desde la adultez temprana y durante toda la vida, una dieta con aproximadamente un 40% menos de calorías. A algunos ratones con restricción calórica se les permitió volver a comer libremente posteriormente, para ver con qué rapidez se recuperaba su sistema sanguíneo. El equipo midió recuentos sanguíneos, examinó las poblaciones celulares en la médula ósea y perfiló la actividad génica y las marcas epigenéticas —etiquetas químicas en el ADN y en las proteínas que ayudan a controlar qué genes se activan— en las raras células madre hematopoyéticas que dan lugar a todas las células sanguíneas.
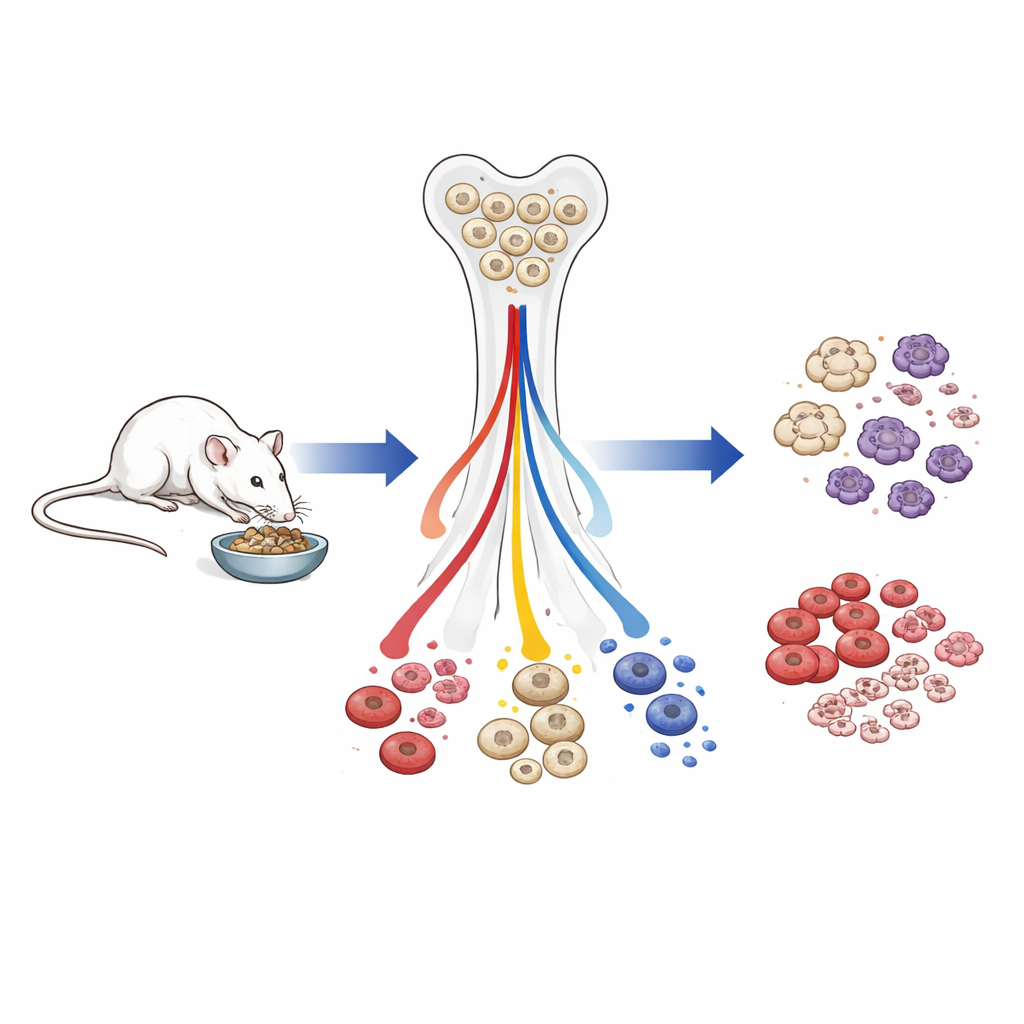
Menos glóbulos blancos totales, pero las células esenciales se protegen
En ratones envejecidos que pasaron la mayor parte de su vida con menos calorías, el número total de leucocitos en la circulación disminuyó. Tanto las células inmunitarias innatas como las adaptativas se redujeron, pero no por igual. Las células importantes para la supervivencia inmediata —los glóbulos rojos que transportan oxígeno, las plaquetas que coagulan la sangre y defensores mieloides de primera línea como los granulocitos— se conservaron relativamente. En contraste, las células linfoides, especialmente las células B que sostienen las respuestas de anticuerpos, se redujeron de forma marcada desde los progenitores tempranos en la médula ósea hasta las células maduras en la sangre. Cuando los animales con restricción calórica fueron re-alimentados durante solo cuatro semanas, los recuentos de glóbulos blancos y el tamaño del bazo se recuperaron en gran medida, y la producción linfoide se disparó, lo que muestra que muchos de estos cambios son rápidamente reversibles.
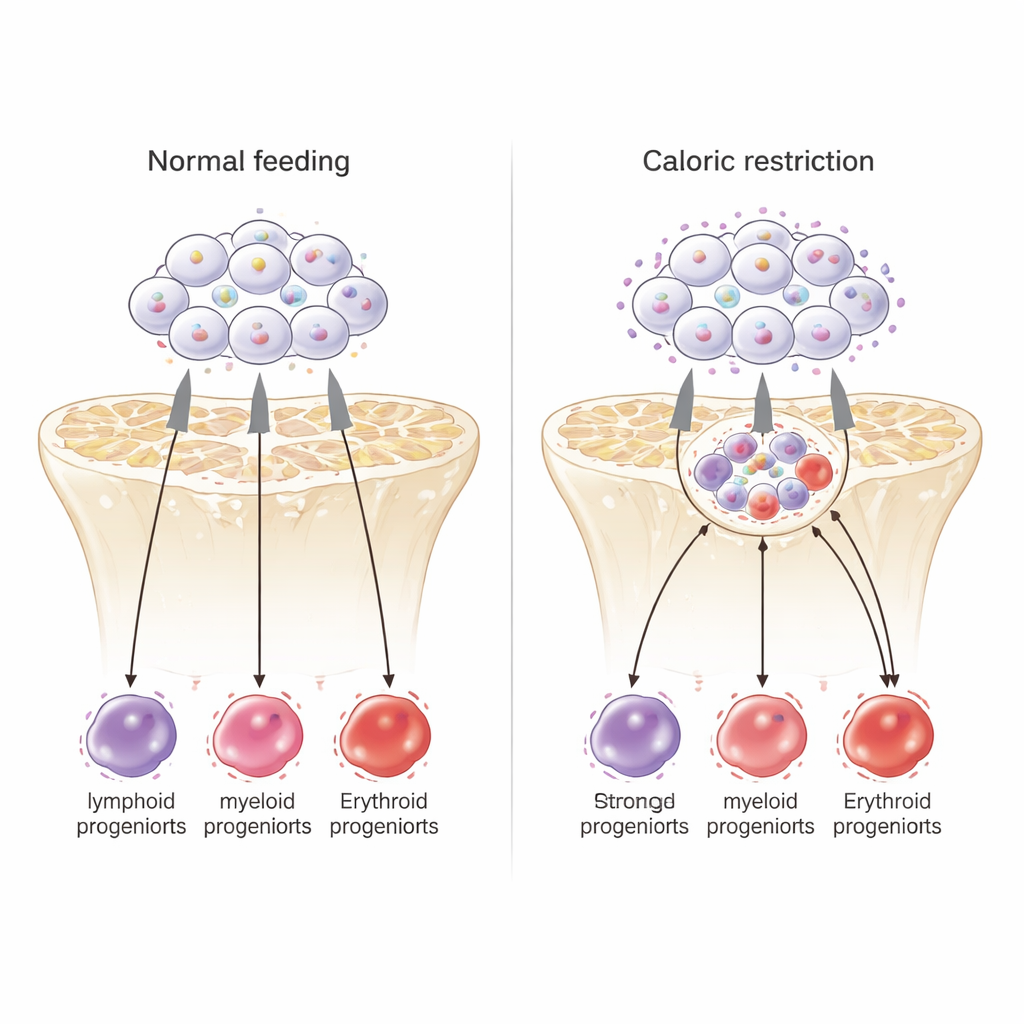
Las células madre trabajan más y eligen destinos distintos
Sorprendentemente, las células madre en la cúspide de la jerarquía sanguínea no entraron en mayor latencia por la falta de comida; en cambio, ciclo celular aumentó. Análisis detallados de la expresión génica revelaron que, bajo restricción calórica, estas células madre atenuaron programas vinculados a la autorrenovación a largo plazo y aumentaron genes asociados con células madre de corta duración y progenitores que generan linajes mieloides y eritroides. En otras palabras, las células madre se vieron forzadas a trabajar más a corto plazo para mantener tipos celulares críticos para la supervivencia, a costa de renovarse lentamente o de generar células linfoides. Aun así, pese a este esfuerzo adicional, su patrón global de actividad génica se parecía más al de células madre jóvenes que al de células viejas.
Reajustar programas de envejecimiento mediante interruptores epigenéticos
El equipo se preguntó luego cómo comer menos podía hacer que las células madre envejecidas se asemejaran molecularmente a células más jóvenes. Mapearon dos marcas de histonas comunes que suelen promover o reprimir la actividad génica. Aunque ambas marcas se redujeron globalmente en las células madre con restricción calórica, un pequeño conjunto de genes asociados al envejecimiento ganó una marca represora y perdió una marca activadora. Sobresalieron dos: Kdr, que codifica un receptor para señales de crecimiento vascular, y Bmpr1a, otro receptor de membrana. Bajo restricción calórica, ambos genes quedaron más fuertemente silenciados. Cuando los investigadores redujeron experimentalmente Kdr y Bmpr1a en células madre envejecidas de ratones alimentados normalmente y transplataron estas células en receptores, las células adoptaron un patrón de expresión génica semejante al de las células madre con restricción calórica, lo que sugiere que estos receptores ayudan a impulsar el programa de envejecimiento y pueden ajustarse epigenéticamente.
Un controlador interno modula la respuesta
Para descubrir puntos de control internos, los científicos examinaron la accesibilidad del ADN a lo largo del genoma de las células madre y dónde se unía un factor de transcripción clave, PU.1. Bajo restricción calórica, muchas regiones del ADN se volvieron más abiertas y mostraron una unión más fuerte de PU.1. Los genes cercanos a estos sitios de PU.1 estuvieron enriquecidos en control del ciclo celular y en vías que dirigen a las células hacia linajes eritroides y otros mieloides, mientras que los genes asociados con la profunda quiescencia de las células madre tendieron a estar reprimidos. Aproximadamente la mitad de los genes que respondieron a la reducción de Kdr mostraron PU.1 en las proximidades, y el propio PU.1 se unió cerca del gen Kdr, lo que sugiere un bucle de retroalimentación. En conjunto, estos datos sitúan a PU.1 como un controlador interno que, en el contexto de una menor señalización de KDR, redirige las células madre envejecidas hacia un estado similar al de la restricción calórica y juvenil que favorece células sanguíneas orientadas a la supervivencia.
Qué significa esto para un envejecimiento saludable
Este trabajo dibuja un panorama matizado de cómo el recorte calórico a largo plazo afecta nuestra factoría sanguínea. En ratones machos, comer menos impulsa a las células madre a priorizar la producción de glóbulos rojos, plaquetas y células inmunitarias de respuesta rápida, mientras limita las células productoras de anticuerpos, lo que puede explicar respuestas debilitadas frente a infecciones bajo dietas estrictas. Al mismo tiempo, cambios epigenéticos dirigidos en genes como Kdr y cambios en la actividad de PU.1 ayudan a preservar un programa génico más juvenil en estas células madre. Aunque el estudio se realizó en ratones y solo en machos, sugiere que futuras terapias podrían intentar imitar los efectos moleculares beneficiosos de la restricción calórica en las células madre hematopoyéticas —sin necesidad de una dieta extrema ni de sacrificar la protección inmunitaria.
Cita: Zong, L., Park, B., Tekin-Turhan, F. et al. Epigenetic profiling of hematopoietic stem cells from male mice identifies KDR and PU.1 as regulators of aging transcriptome and caloric restriction response. Nat Commun 17, 2978 (2026). https://doi.org/10.1038/s41467-026-69718-0
Palabras clave: restricción calórica, células madre hematopoyéticas, envejecimiento inmunitario, epigenética, PU.1 y KDR