Clear Sky Science · ar
التحليل فوق الجيني لخلايا الدم الجذعية المكونة للدم لدى ذكور الفئران يحدد KDR وPU.1 كمنظمين لمخطط التعبير الجيني المرتبط بالشيخوخة واستجابة تقييد السعرات
لماذا قد يعيد تقليل الطعام تشكيل دمنا
ثبت أن تقليل السعرات دون التسبب بسوء تغذية يطيل متوسط العمر في العديد من الحيوانات، ويقبل بعض الأشخاص على حميات صارمة على أمل العيش لفترة أطول. لكن تقليل الأكل يمكن أن يضعف الجهاز المناعي أيضاً. تطرح هذه الدراسة سؤالاً بسيطاً لكنه مهم: كيف يغيّر تقليل السعرات على المدى الطويل خلايا الدم الجذعية في نخاع العظم التي تعيد بناء دمنا وجهازنا المناعي باستمرار، وهل يمكن لهذه التغيرات أن تساعد على إبقاء هذه الخلايا «شابة» مع الاستمرار في حمايتنا؟
كيف نُفِّذت الدراسة في الفئران
عمل الباحثون مع فئران ذكور كانت إما تتغذى بحرية أو خضعت لحمية مدى الحياة تقل فيها السعرات بنحو 40% بدءاً من مرحلة البلوغ المبكر. أُتيح لبعض الفئران المقيدة السعرات لاحقاً أن تتغذى بحرية مرة أخرى، لمعرفة مدى سرعة تعافي نظام الدم لديها. قاس الفريق تعداد الدم، وفحص مجموعات الخلايا في نخاع العظم، وبنى ملفات نشاط الجينات والوسوم فوق الجينية — وهي علامات كيميائية على الحمض النووي والبروتينات تساعد في التحكم بتشغيل الجينات — في خلايا الدم الجذعية النادرة التي تنشأ منها كل خلايا الدم.
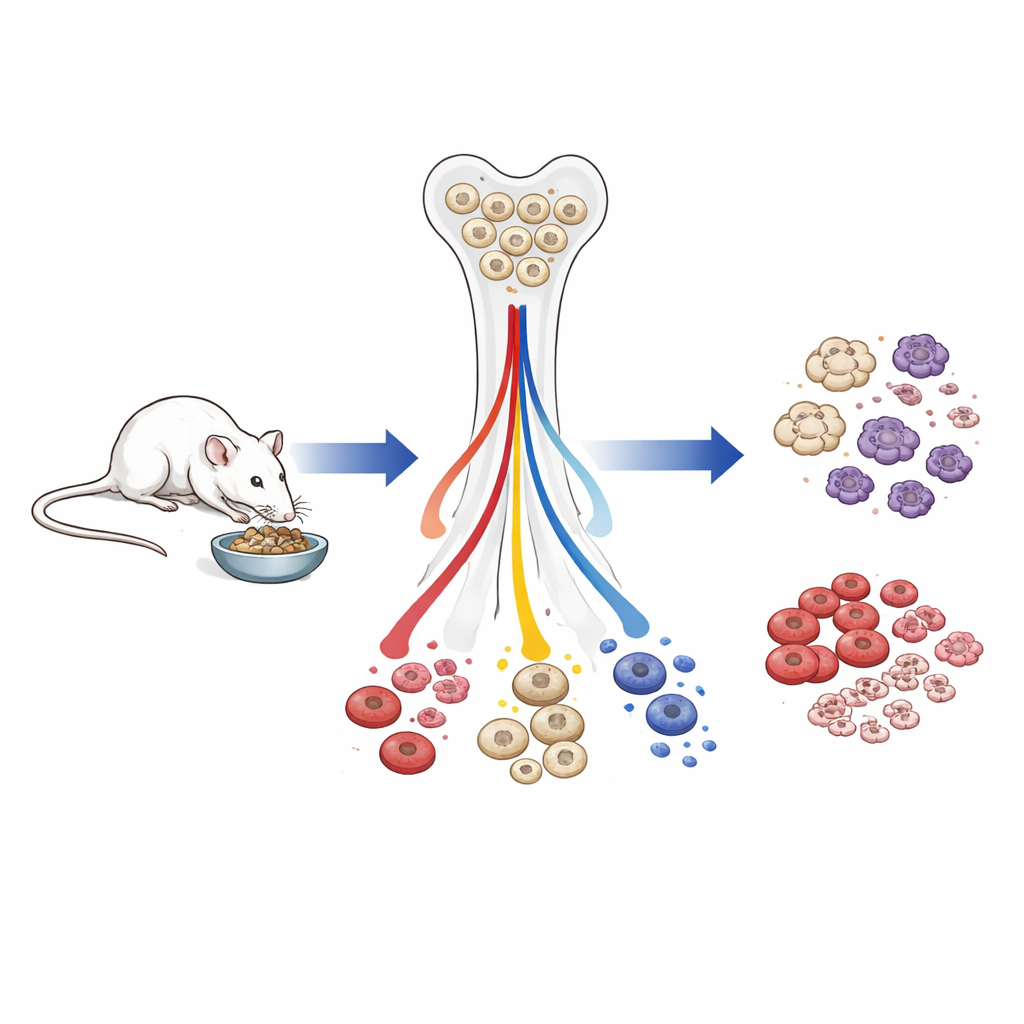
انخفاض إجمالي خلايا الدم البيضاء، لكن خلايا البقاء محمية
في الفئران المسنة التي قضت معظم حياتها على سعرات أقل، انخفض عدد خلايا الدم البيضاء في الدورة الدموية عموماً. انخفضت كل من خلايا الجهاز المناعي الفطري والمكتسب، لكن ليس بالتساوي. كانت الخلايا المهمة للبقاء الفوري — خلايا الدم الحمراء الناقلة للأكسجين، والصفائح الدموية المجلطة، ودفاعات النخاع المباشرة مثل حبيبات الدم — محفوظة نسبياً. في المقابل، تراجعت الخلايا اللمفاوية، خصوصاً الخلايا البائية المسؤولة عن الاستجابات بالأجسام المضادة، بشدة بدءاً من الخلايا الجذعية البادئة في نخاع العظم وحتى الخلايا الناضجة في الدم. عندما أعيد إطعام الحيوانات المقيدة لمدة أربعة أسابيع فقط، عاد تعداد خلايا الدم وحجم الطحال إلى حد كبير، وتدفق إنتاج الخلايا اللمفاوية، ما يبيّن أن كثيراً من هذه التغيرات قابلة للعكس بسرعة.
الخلايا الجذعية تعمل بجهد أكبر وتختار مصائر مختلفة
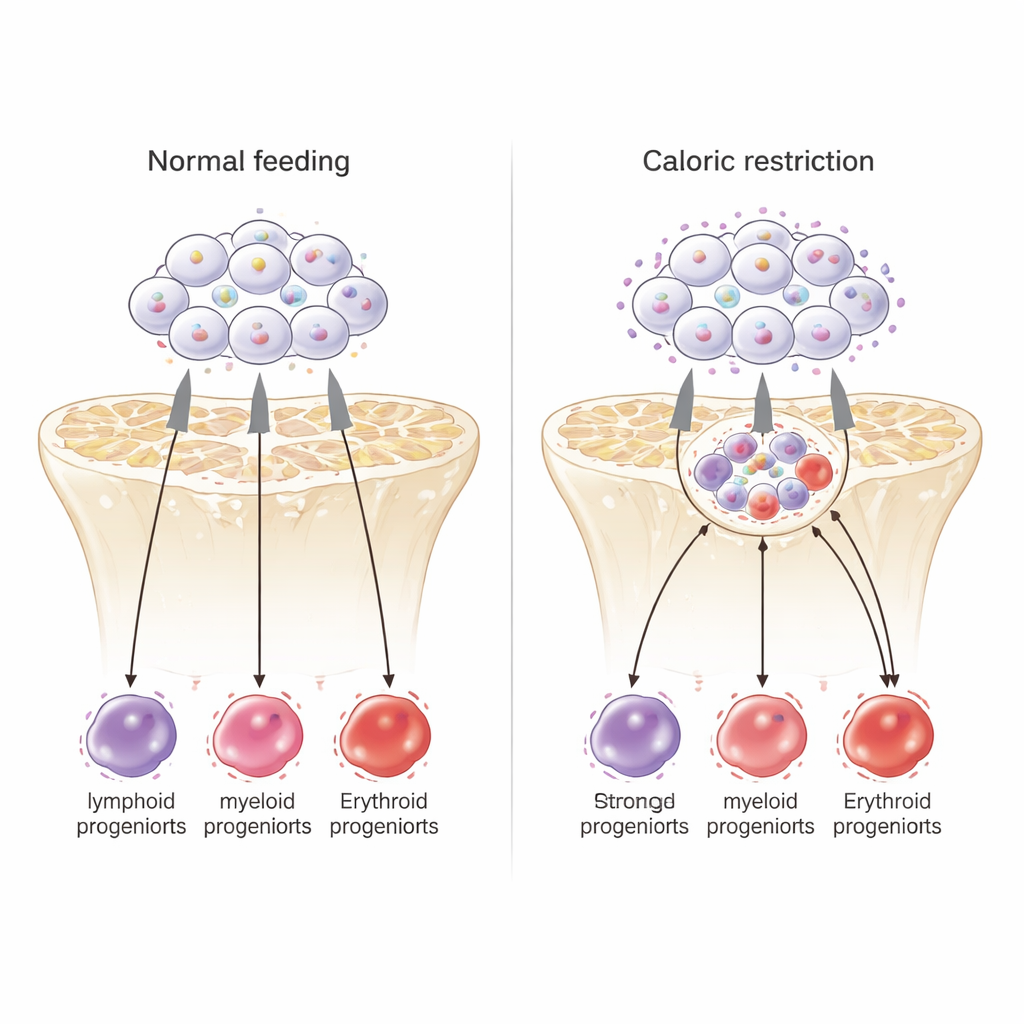
من المدهش أن الخلايا الجذعية في قمة هرَم الدم لم تدخل في سبات أكثر خلال نقص الغذاء؛ بل على العكس، كانت تتكاثر بنشاط أكبر. كشفت تحليلات تفصيلية لنشاط الجينات أن هذه الخلايا تحت تقييد السعرات خفّضت برامج مرتبطة بالتجدد الذاتي طويل الأمد، وزادت تعبيرات جينات مرتبطة بالخلايا الجذعية قصيرة الأمد والنسائل التي تُنتج السلالات المحببة والدم الحمراء. بعبارة أخرى، دفعت الحمية الخلايا الجذعية للعمل أكثر على المدى القصير للحفاظ على أنواع الخلايا الضرورية للبقاء، على حساب تجددها البطيء أو إنتاج الخلايا اللمفاوية. ومع ذلك، وبالرغم من هذا العمل الإضافي، بدا نمط نشاط جيناتها أقرب إلى خلايا جذعية شابة منه إلى خلايا مسنة.
إعادة ضبط برامج الشيخوخة عبر مفاتيح فوق جينية
سأل الفريق بعد ذلك كيف يمكن لتقليل الأكل أن يجعل الخلايا الجذعية المسنة تبدو أصغر جزيئياً. رسموا خرائط لوسمين شائعين في الهيستون عادةً ما يعززان أو يكبتان نشاط الجينات. رغم أن كلا الوسمين انخفضا على الصعيد العام في الخلايا الجذعية المقيدة السعرات، حصلت مجموعة صغيرة من الجينات المرتبطة بالشيخوخة على وسم قمعي وفقدت وسم تنشيطي. برزت اثنتان منهما: Kdr، الذي يشفر لمستقبل لإشارات نمو الأوعية الدموية، وBmpr1a، مستقبل سطحي آخر. تحت تقييد السعرات، أُغلقت هاتان الجينتان بإحكام أكبر. عندما خفض الباحثون تجريبياً تعبير Kdr وBmpr1a في خلايا جذعية مسنة من فئران مُغذَّاة طبيعياً وزرعوا هذه الخلايا في مستلمين، تبنت الخلايا نمط تعبير جيني يشبه خلايا الجذعية المقيدة السعرات، ما يوحي بأن هذه المستقبلات تساهم في دفع برنامج الشيخوخة ويمكن ضبطها فوق جينياً.
شرطي مروري داخلي يضبط الاستجابة
لاكتشاف نقاط التحكم الداخلية، فحص العلماء مدى إمكانية الوصول إلى الحمض النووي عبر جينوم الخلايا الجذعية وأماكن ارتباط عامل نسخي رئيسي، PU.1. تحت تقييد السعرات، أصبحت العديد من مناطق الحمض النووي أكثر انفتاحاً وأظهرت ارتباط PU.1 أقوى. كانت الجينات المجاورة لمواقع PU.1 هذه غنية بعناصر ضبط دورة الخلية وبالمسارات التي توجه الخلايا نحو خلايا الدم الحمراء وسلالات المايلويد الأخرى، بينما ميّلت الجينات المرتبطة بسبات الخلايا الجذعية العميق إلى أن تكون مكبوتة. نحو نصف الجينات التي استجابت عند خفض Kdr أظهر وجود PU.1 بالقرب منها، كما ارتبط PU.1 نفسه بالقرب من جين Kdr، في إشارة إلى وجود حلقة تغذية راجعة. مجتمعة، تضع هذه البيانات PU.1 كشرطي مروري داخلي يقوم، في سياق انخفاض إشارات KDR، بإعادة توجيه خلايا الدم الجذعية المسنة نحو حالة شبيهة بتلك الناتجة عن تقييد السعرات وتفضل خلايا الدم الموجهة للبقاء.
ماذا يعني هذا للشيخوخة الصحية
تقدم هذه الدراسة صورة مدروسة لكيفية تأثير تقليل السعرات على مدى طويل على مصنع الدم لدينا. في الفئران الذكور، يدفع تقليل الأكل الخلايا الجذعية إلى إعطاء الأولوية لصنع خلايا الدم الحمراء والصفائح الدموية وخلايا مناعية سريعة الاستجابة بينما يكبح خلايا إنتاج الأجسام المضادة، مما قد يفسر ضعف الاستجابة للعدوى تحت حميات صارمة. في الوقت نفسه، تُسهم تغييرات فوق جينية مستهدفة عند جينات مثل Kdr وتحولات في نشاط PU.1 في الحفاظ على برنامج جيني أكثر شبابية في هذه الخلايا الجذعية. رغم أن الدراسة أُجريت في الفئران وعلى الذكور فقط، فإنها توحي بأن علاجات مستقبلية قد تسعى إلى محاكاة التأثيرات الجزيئية المفيدة لتقييد السعرات على خلايا الدم المكونة — دون الحاجة إلى حميات قاسية أو التضحية بالحماية المناعية.
الاستشهاد: Zong, L., Park, B., Tekin-Turhan, F. et al. Epigenetic profiling of hematopoietic stem cells from male mice identifies KDR and PU.1 as regulators of aging transcriptome and caloric restriction response. Nat Commun 17, 2978 (2026). https://doi.org/10.1038/s41467-026-69718-0
الكلمات المفتاحية: تقييد السعرات, خلايا الدم الجذعية المكونة للدم, شيخوخة الجهاز المناعي, علم التوارث فوق الجيني, PU.1 و KDR