Clear Sky Science · zh
DUSP26通过去磷酸化p53在丝氨酸312位保护急性肾损伤
为什么肾脏受压对每个人都重要
急性肾损伤是肾功能的突然下降,可在大手术、严重感染、脱水或癌症治疗期间发生。这在住院患者中很常见,会增加需要透析、在重症监护室停留更久以及之后发展为慢性肾病的风险。然而,临床上仍无直接保护肾脏实质细胞的靶向药物。本研究揭示了这些细胞内一种内在的保护开关,并展示了开启或关闭该开关如何显著改变肾脏是否受损或得以保全。
肾细胞内的隐秘守护者
作者关注肾脏中那些过滤并精细调节我们血液的微小输尿管。通过使用现代机器学习工具挖掘若干大型人类数据集,他们锁定了一个名为DUSP26的基因,该基因在急性肾损伤患者中持续表现为低表达,相较于健康肾脏患者。当他们检查人体活检样本时发现,近端小管细胞——承担肾脏大部分工作负荷的细胞——在损伤期间DUSP26蛋白明显减少,且这种缺失与更严重的组织损伤和更差的肾功能紧密相关。这提示DUSP26通常有助于这些细胞抵御应激。
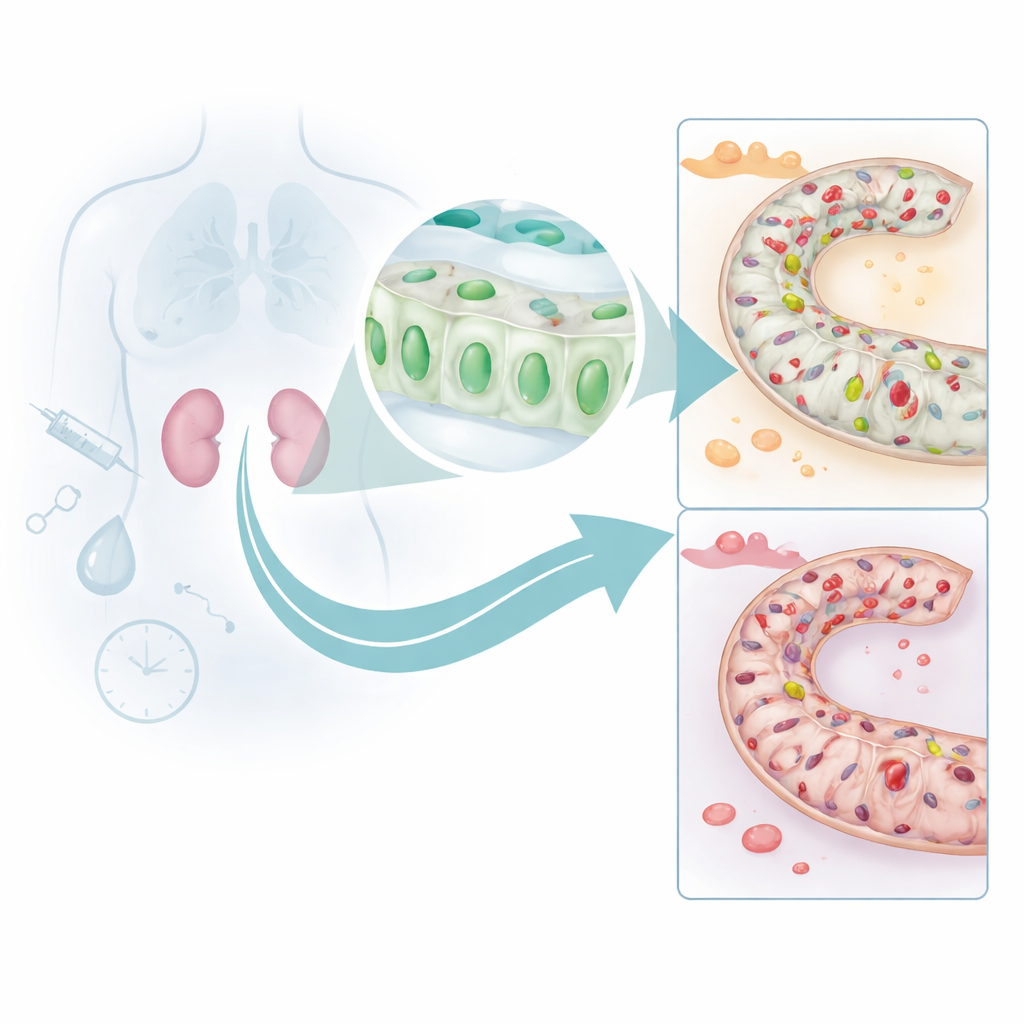
肾脏保护如何被关闭
为了解DUSP26水平为何下降,研究团队转向两种常见肾脏应激的小鼠模型:一种是对肾毒性的化疗药物,另一种是阻断血流后再灌注的缺血‑再灌注。在两种情况下,肾脏中DUSP26水平的下降与细胞死亡的增加并行。他们将这种丧失追溯到分布在DUSP26基因调控区的化学标签——DNA甲基化。这些标签就像贴在开关上的胶带,阻止基因被开启。培养的肾细胞实验显示,损伤会增加甲基化并关闭DUSP26,负责添加这些标签的酶被招募到该基因的启动子区域。在遭受缺血‑再灌注损伤的小鼠中,深度测序证实同一启动子区域的多个位点出现了高度甲基化。
在动物体内关闭与打开保护
研究者接着探问如果移除或加强这一分子屏障会如何。在细胞培养中,用基因工具或小分子药物阻断DUSP26会在毒性或低氧应激后诱导更多的caspase‑3活化,caspase‑3是程序性细胞死亡的主要执行者;而增强DUSP26则产生相反效果,减少细胞死亡。在小鼠中,先给动物使用DUSP26抑制剂再施加肾损伤,会导致血液代谢废物水平更高、显微结构损伤更多以及小管细胞死亡增加。相反,特异性在近端小管中过表达DUSP26的小鼠在药物诱导和缺血损伤两种情形下都显示出显著的保护,肾功能更佳、组织损伤更少。这些功能获得与丧失的实验共同揭示了DUSP26作为小管完整性强有力守护者的角色。
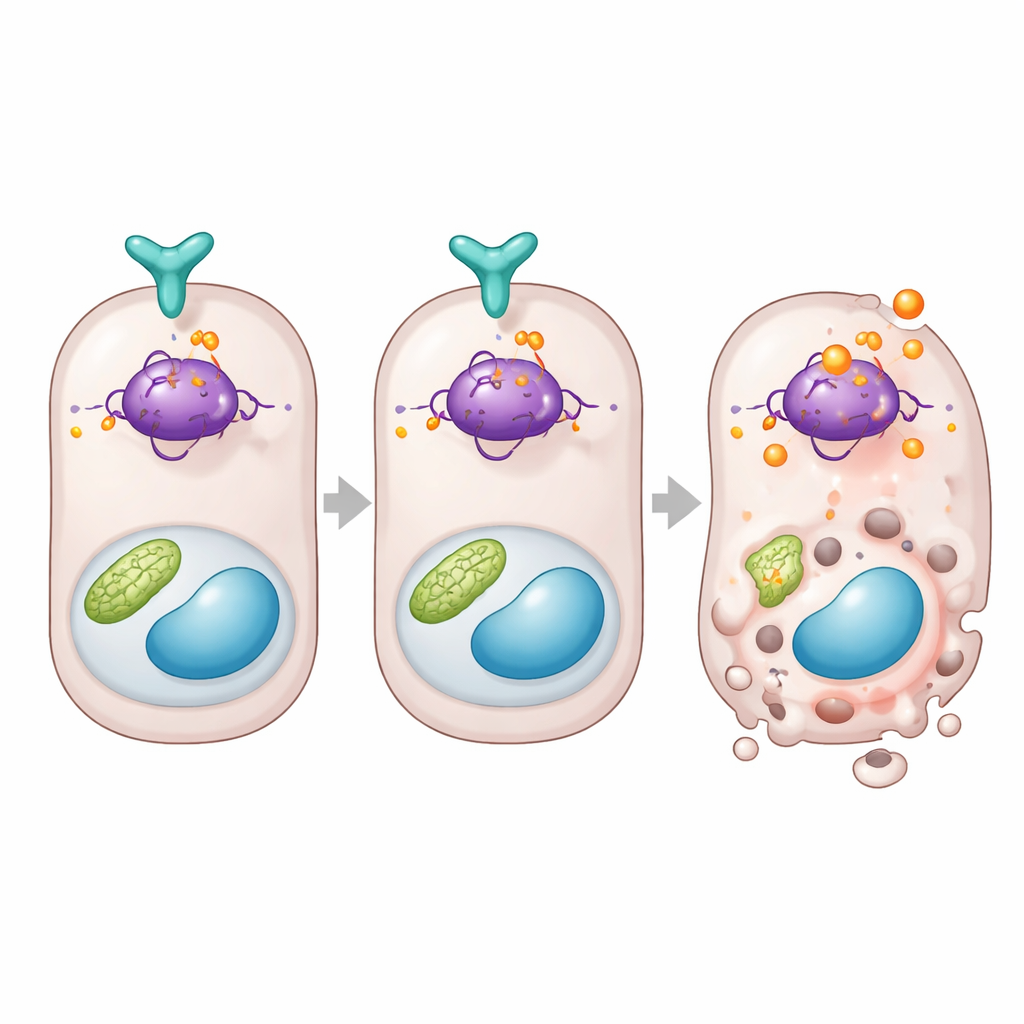
对决定细胞死亡蛋白的直接制动
更深入的研究将DUSP26与著名的细胞决策蛋白p53联系起来,该蛋白决定受压细胞是修复自身还是自毁。研究小组发现,在人类数据或小鼠肾脏中DUSP26水平较低时,p53控制的促死基因如Bax和Puma被上调。在细胞水平上,DUSP26可与p53物理结合并选择性地从蛋白上的一个特定位点去除磷酸基,已知在小鼠中该位点为丝氨酸312。当DUSP26缺失时,该位点被大量修饰,p53活性上升,促死基因被激活。为证明该位点的重要性,作者重建了不能在该位点被修饰的p53版本的肾细胞和小鼠。尽管p53系统的其他部分保持完整,这些细胞和动物对肾损伤的抵抗力显著提高,表现为更少的小管细胞死亡和更少的器官功能障碍。
从分子洞见到未来疗法
综合来看,这项工作勾勒出一条清晰的事件链:肾脏应激增加了DUSP26基因的DNA甲基化,降低了近端小管中的DUSP26蛋白。可用的DUSP26减少后,p53在关键位点上保持磷酸化状态、活性增强,并驱动促细胞死亡基因的表达。恢复DUSP26或模拟其对该单个位点的作用可以抑制这一死亡程序并保护肾组织。对患者而言,这表明精心设计的药物或基因靶向策略以增强DUSP26活性——或特异性减少p53在该位点的磷酸化——有望在手术、化疗或重症期间保护肾脏,甚至可能保护其他器官免受类似的急性损伤。
引用: Fu, Y., Xiang, Y., Han, Y. et al. DUSP26 protects against acute kidney injury by dephosphorylating p53 at serine 312. Nat Commun 17, 3208 (2026). https://doi.org/10.1038/s41467-026-69688-3
关键词: 急性肾损伤, 肾小管细胞, p53信号, 表观遗传调控, 细胞死亡