Clear Sky Science · tr
DUSP26, p53’ü serin 312’de defosforile ederek akut böbrek hasarına karşı korur
Neden böbrek stresi herkes için önemlidir
Akut böbrek hasarı, büyük ameliyat, şiddetli enfeksiyon, dehidrasyon veya kanser tedavisi sırasında ortaya çıkabilen ani bir böbrek fonksiyon düşüşüdür. Hastanelerde sık görülür ve diyaliz gereksinimi, yoğun bakımda daha uzun kalma ve daha sonra kronik böbrek hastalığı gelişme riskini artırır. Yine de doktorların böbreğin çalışan hücrelerini doğrudan koruyan hedefe yönelik bir ilacı yoktur. Bu çalışma, bu hücrelerin içinde yerleşik bir koruyucu anahtar keşfediyor ve o anahtarın açılıp kapatılmasının böbreğin zarar görüp görmeyeceğini nasıl dramatik şekilde değiştirdiğini gösteriyor.
Böbrek hücrelerinin içindeki gizli bir savunucu
Yazarlar, kanımızı filtreleyip ince ayar yapan böbreğin küçük tüplerine odaklandı. Birkaç büyük insan veri setini modern makine öğrenimi araçlarıyla tarayarak, akut böbrek hasarı olan kişilerde sağlıklı böbreklere göre tutarlı şekilde daha düşük düzeyde görülen DUSP26 adında bir gen belirlediler. İnsan biyopsi örneklerini incelediklerinde, böreğin işinin çoğunu yapan proksimal tübül hücrelerinde yaralanma sırasında DUSP26 proteininin keskin bir şekilde azaldığını ve bu kaybın doku hasarının kötüleşmesi ve böbrek fonksiyonunun düşmesi ile yakından ilişkili olduğunu buldular. Bu bulgu, DUSP26’nın normalde bu hücrelerin strese dayanmasına yardımcı olduğunu düşündürdü.
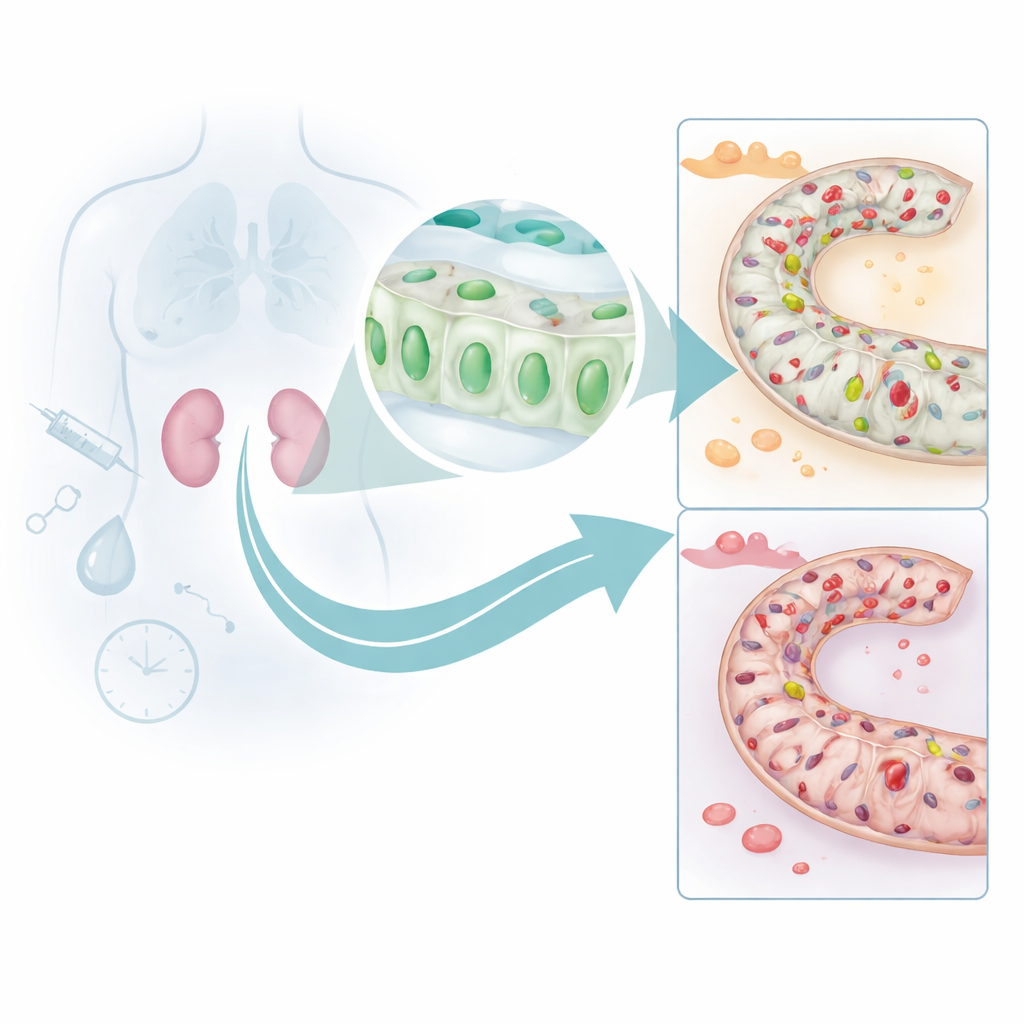
Böbreğin kalkanının nasıl kapandığı
DUSP26 düzeylerinin neden düştüğünü anlamak için ekip, kemoterapi ilacının böbreğe toksik olduğu ve kan akışının engellenip sonra yeniden sağlandığı iki yaygın böbrek stres formunun fare modellerine yöneldi. Her iki durumda da böbrekteki DUSP26 düzeyleri hücre ölümünün artmasıyla paralel olarak düştü. Bu kaybı, DUSP26 geninin kontrol bölgesine yerleştirilen DNA metilasyonu adı verilen kimyasal etiketlere bağladılar. Bu etiketler, bir ışık anahtarının üzerine yapıştırılan bant parçaları gibi davranarak genin açılmasını engelliyor. Kültürdeki böbrek hücrelerinde yapılan deneyler, yaralanmanın metilasyonu artırdığını ve DUSP26’yı kapattığını; bu etiketleri ekleyen enzimlerin genin promotör bölgesine çekildiğini gösterdi. İskemi‑reperfüzyon hasarlı farelerde yapılan derin dizileme, aynı promotör bölgesindeki birçok sitenin yoğun şekilde metillenmiş hale geldiğini doğruladı.
Hayvanlarda korumayı kapatmak ve açmak
Araştırmacılar daha sonra bu moleküler kalkan kaldırılırsa veya güçlendirilirse ne olduğunu sordular. Hücre kültüründe DUSP26’yı genetik yöntemlerle veya küçük moleküllü bir ilaçla engellemek, toksik veya düşük oksijen stresinden sonra programlı hücre ölümünün kilit yürütücüsü olan kaspaz‑3’ün daha fazla aktivasyonuna yol açtı. DUSP26’yı artırmak ise ters etki göstererek hücre ölümünü azalttı. Farelerde, böbrek hasarından önce hayvanlara DUSP26 inhibitörü verildiğinde kan atık düzeyleri yükseldi, mikroskopik hasar arttı ve daha fazla tübül hücresi öldü. Buna karşılık, proksimal tübüllerde özel olarak DUSP26 fazladan üreten fareler, hem ilaç kaynaklı hem de iskemik hasardan dikkat çekici derecede korunma gösterdi; böbrek fonksiyonu daha iyi ve doku hasarı daha azdı. Bu kazanım‑ve‑kayıp fonksiyon deneyleri bir arada, DUSP26’yı tübüler bütünlüğün güçlü bir koruyucusu olarak ortaya koyuyor.
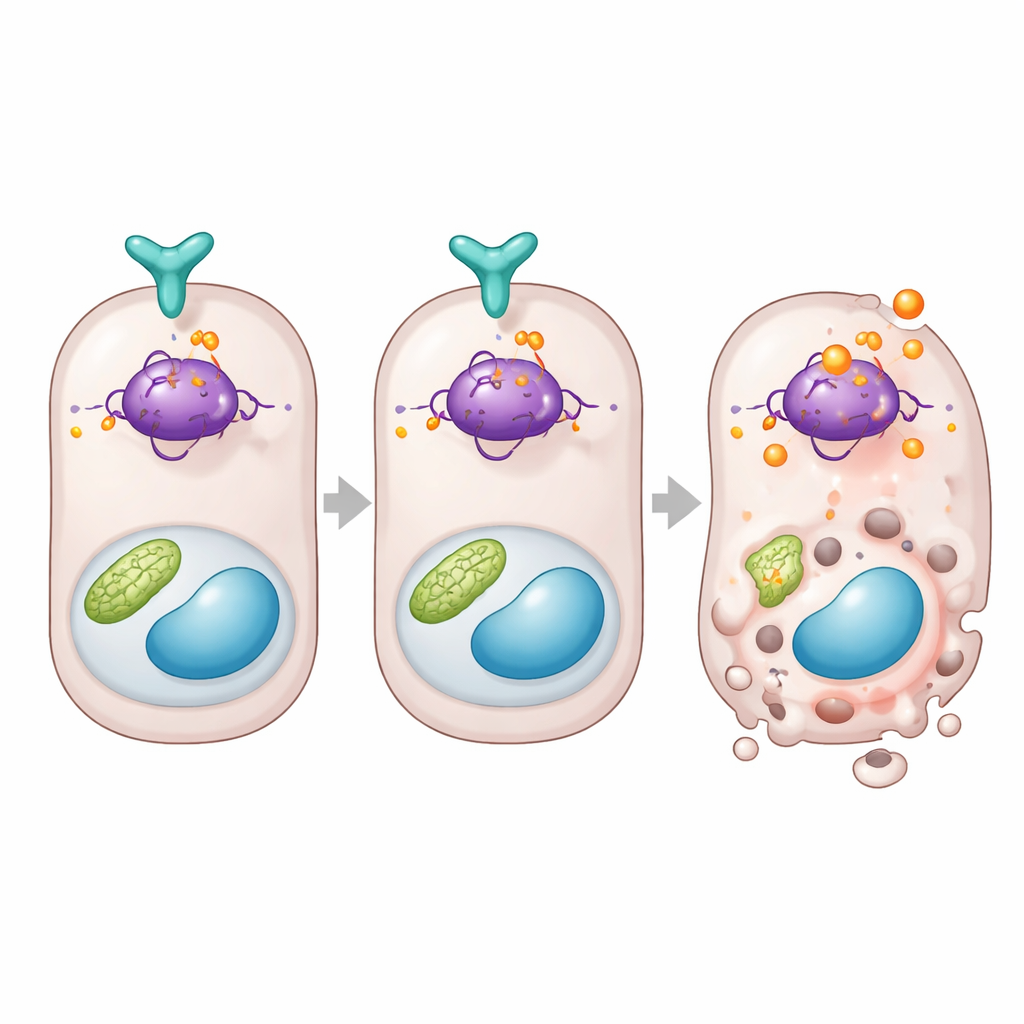
Hücrenin ölüm kararını veren proteini üzerine doğrudan bir fren
Daha derine inen çalışma, DUSP26’yı strese maruz kalan bir hücrenin kendini onarıp onarmayacağına ya da kendini yok edeceğine karar veren ünlü p53 proteiniyle ilişkilendiriyor. Ekip, insan verilerinde veya fare böbreklerinde DUSP26 düşük olduğunda Bax ve Puma gibi p53 kontrolündeki ölüm genlerinin yükseldiğini buldu. Hücrelerde DUSP26, p53’e fiziksel olarak bağlandı ve proteinin tek bir bölgesinden, farelerde serin 312 olarak bilinen yerden seçici olarak bir fosfat grubunu kaldırdı. DUSP26 yok olduğunda bu bölge yoğun şekilde modifiye oldu, p53 aktivitesi arttı ve hücre ölümünü destekleyen genler açıldı. Bu bölgenin önemini kanıtlamak için yazarlar, o noktada artık modifiye edilemeyen bir p53 versiyonuyla hem böbrek hücrelerini hem de fareleri yeniden inşa ettiler. Bu hücreler ve hayvanlar, p53 sisteminin diğer parçaları sağlam kalmasına rağmen böbrek hasarına karşı çok daha dirençliydi; daha az tübül hücresi ölüyordu ve organ fonksiyonu daha az bozuluyordu.
Moleküler içgörüslerden gelecekteki tedavilere
Toplanınca çalışma şu açık olay zincirini özetliyor: böbrek stresi DUSP26 geninde DNA metilasyonunu artırıyor ve proksimal tübüllerde DUSP26 proteinini azaltıyor. Daha az DUSP26 mevcut olduğunda, p53 kritik bir bölgede fosforile olarak kalıyor, daha aktif hale geliyor ve hücreleri ölüme iten genlerin ifadesini tetikliyor. DUSP26’yı yeniden sağlamak veya onun tek bir bölge üzerindeki etkisini taklit etmek, bu ölüm programını zayıflatıyor ve böbrek dokusunu koruyor. Hastalar için bu, dikkatle tasarlanmış ilaçların veya gen hedefli yaklaşımların DUSP26 aktivitesini artırmasının —ya da özel olarak p53’ün bu bölgedeki fosforilasyonunu azaltmasının— bir gün ameliyat, kemoterapi veya ciddi hastalık sırasında böbrekleri korumaya ve belki benzer akut hasar biçimlerinden diğer organları korumaya yardımcı olabileceğini öne sürüyor.
Atıf: Fu, Y., Xiang, Y., Han, Y. et al. DUSP26 protects against acute kidney injury by dephosphorylating p53 at serine 312. Nat Commun 17, 3208 (2026). https://doi.org/10.1038/s41467-026-69688-3
Anahtar kelimeler: akut böbrek hasarı, böbrek tübül hücreleri, p53 sinyalizasyonu, epigenetik düzenleme, hücre ölümü