Clear Sky Science · es
DUSP26 protege frente a la lesión renal aguda desfosforilando p53 en la serina 312
Por qué el estrés renal importa a todos
La lesión renal aguda es una caída súbita de la función renal que puede aparecer durante cirugías mayores, infecciones graves, deshidratación o tratamientos contra el cáncer. Es frecuente en hospitales y aumenta el riesgo de necesitar diálisis, de permanecer más tiempo en la UCI y de desarrollar posteriormente enfermedad renal crónica. Aun así, los médicos no disponen de un medicamento específico que proteja directamente las células funcionales del riñón. Este estudio descubre un interruptor protector interno en esas células y muestra cómo activarlo o desactivarlo puede cambiar de forma drástica si los riñones resultan dañados o se mantienen indemnes.
Un defensor oculto dentro de las células renales
Los autores se centraron en los diminutos túbulos del riñón que filtran y afinan nuestra sangre. Al explorar varios grandes conjuntos de datos humanos con herramientas modernas de aprendizaje automático, identificaron un gen llamado DUSP26 que aparecía consistentemente reducido en personas con lesión renal aguda respecto a quienes tenían riñones sanos. Al examinar biopsias humanas, observaron que las células del túbulo proximal —las que realizan la mayor parte del trabajo del riñón— presentaban cantidades marcadamente reducidas de la proteína DUSP26 durante la lesión, y que esa pérdida se asociaba estrechamente con un mayor daño tisular y peor función renal. Esto sugiere que DUSP26 ayuda normalmente a estas células a resistir el estrés.
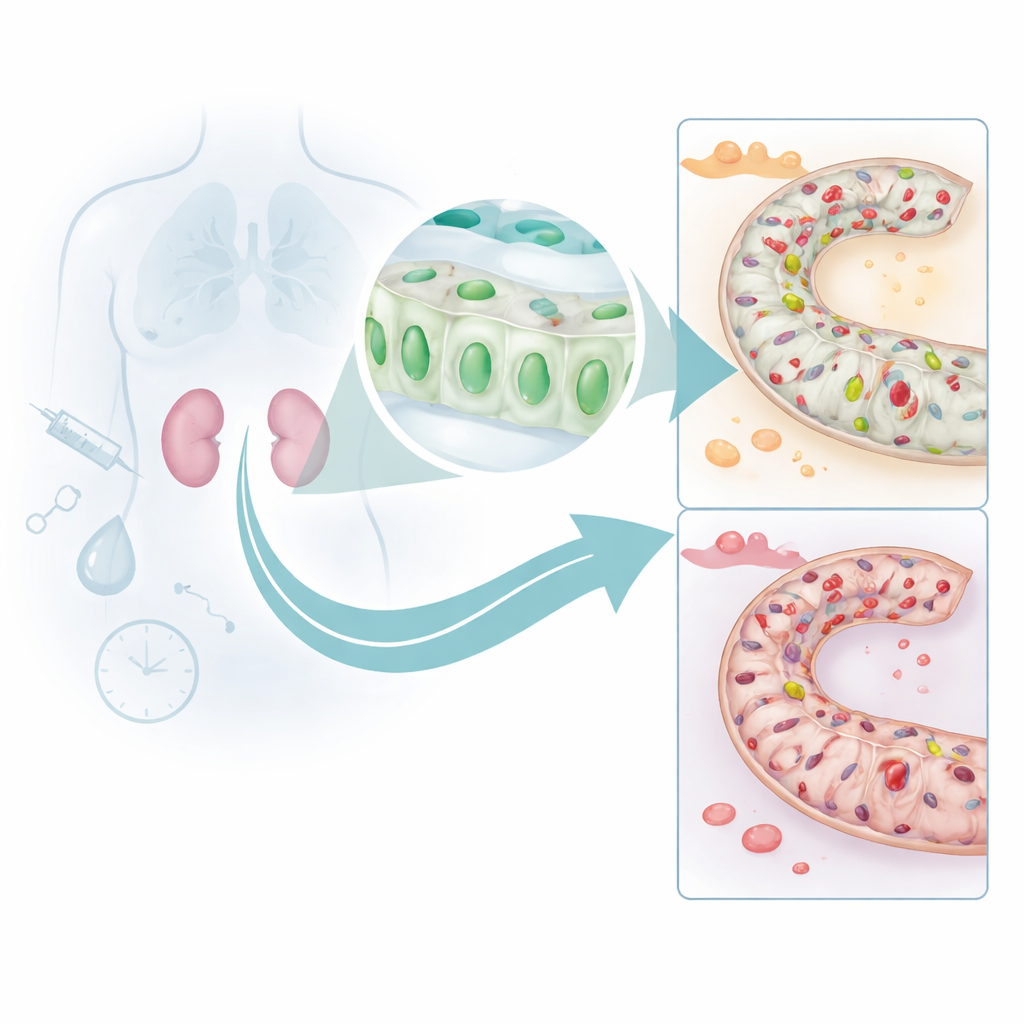
Cómo se apaga el escudo del riñón
Para entender por qué disminuyen los niveles de DUSP26, el equipo recurrió a modelos animales de dos formas comunes de estrés renal: un fármaco quimioterápico tóxico para el riñón y un periodo de flujo sanguíneo obstruido seguido de reperfusión. En ambas situaciones, los niveles de DUSP26 en el riñón cayeron en paralelo con un aumento de la muerte celular. Rastrearon esta pérdida hasta marcas químicas, llamadas metilación del ADN, depositadas a lo largo de la región reguladora del gen DUSP26. Estas marcas actúan como tiras de cinta sobre un interruptor, impidiendo que el gen se active. Experimentos en células renales cultivadas mostraron que la lesión aumentaba la metilación y silenciaba DUSP26, y que las enzimas encargadas de añadir estas marcas se dirigían al promotor del gen. En ratones con lesión por isquemia‑reperfusión, el secuenciamiento profundo confirmó que muchos sitios dentro de la misma región promotora se volvían altamente metilados.
Apagar y encender la protección en animales
Los investigadores se preguntaron qué ocurre si se elimina o refuerza este escudo molecular. En cultivo celular, bloquear DUSP26 con herramientas genéticas o con un fármaco de pequeña molécula condujo a una mayor activación de la caspasa‑3, un ejecutor clave de la muerte celular programada, tras estrés tóxico o por falta de oxígeno. Aumentar DUSP26 tuvo el efecto contrario, reduciendo la muerte celular. En ratones, el pretratamiento con el inhibidor de DUSP26 antes de la lesión renal ocasionó niveles más altos de desechos en sangre, más daño microscópico y más células tubulares muriendo. En contraste, ratones diseñados para sobreproducir DUSP26 específicamente en los túbulos proximales mostraron una protección notable frente tanto a la lesión inducida por fármacos como a la isquémica, con mejor función renal y menor daño tisular. Estos experimentos de ganancia y pérdida de función revelan en conjunto a DUSP26 como un potente guardián de la integridad tubular.
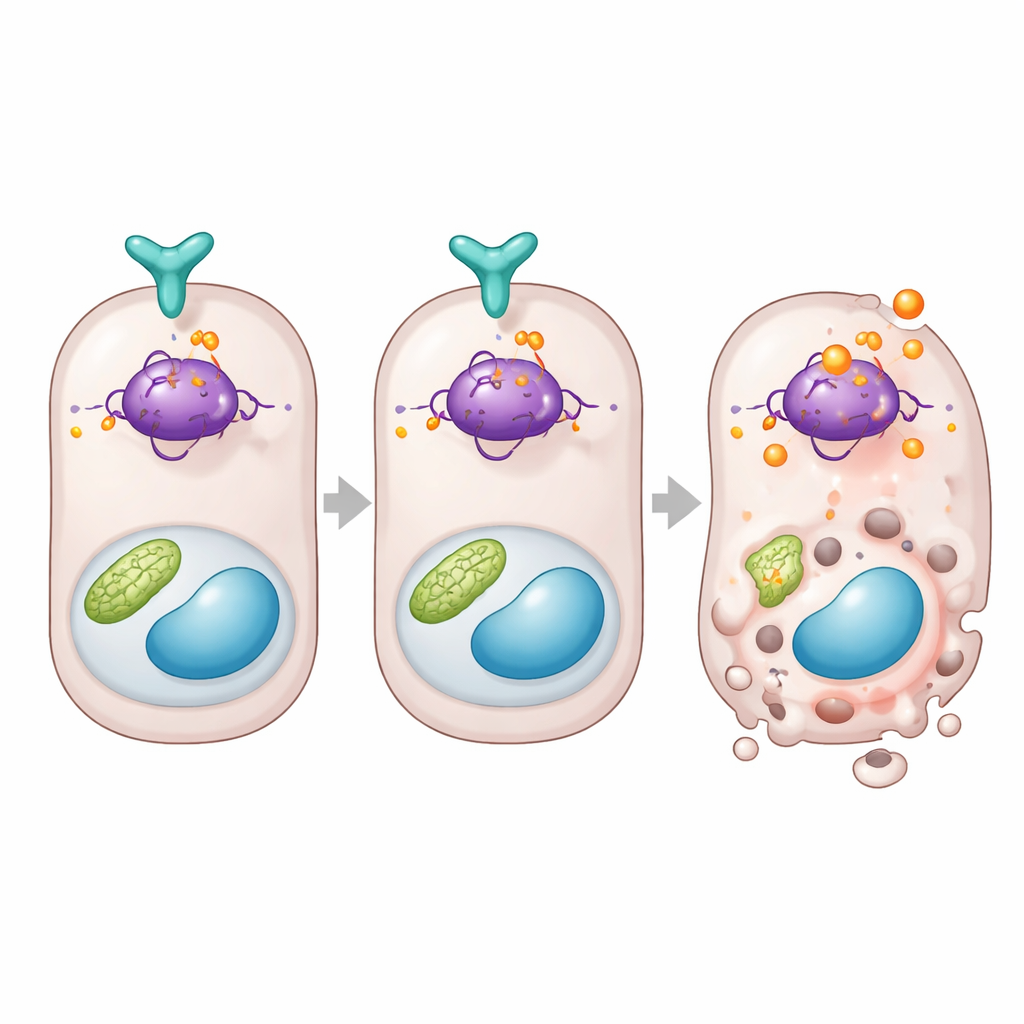
Un freno directo sobre la proteína que decide la muerte celular
Indagando más a fondo, el estudio conecta DUSP26 con p53, una proteína famosa que decide si una célula estresada se repara o se autodestruye. El equipo encontró que cuando DUSP26 era bajo en datos humanos o en riñones de ratón, los genes de muerte controlados por p53, como Bax y Puma, se expresaban más. En células, DUSP26 se unía físicamente a p53 y eliminaba de forma selectiva un grupo fosfato en un sitio específico de la proteína, conocido como serina 312 en ratones. Cuando DUSP26 faltaba, este sitio se modificaba intensamente, la actividad de p53 aumentaba y se activaban genes promotores de la muerte. Para demostrar la importancia de este sitio, los autores reconstruyeron células renales y ratones con una versión de p53 que ya no podía modificarse en ese punto. Esas células y animales fueron mucho más resistentes a la lesión renal, con menos células tubulares muriendo y menos disfunción orgánica, aunque otras partes del sistema p53 permanecieran intactas.
De la comprensión molecular a futuras terapias
En conjunto, el trabajo describe una cadena clara de eventos: el estrés renal incrementa la metilación del ADN en el gen DUSP26, reduciendo la proteína DUSP26 en los túbulos proximales. Con menos DUSP26 disponible, p53 permanece fosforilado en un sitio crítico, se vuelve más activo y promueve la expresión de genes que empujan a las células hacia la muerte. Restaurar DUSP26, o imitar su acción sobre ese único sitio, atenúa este programa de muerte y preserva el tejido renal. Para los pacientes, esto sugiere que fármacos cuidadosamente diseñados o enfoques dirigidos por genes que aumenten la actividad de DUSP26 —o que reduzcan específicamente la fosforilación de p53 en este sitio— podrían algún día ayudar a proteger los riñones durante cirugías, quimioterapia o enfermedades graves, y quizás salvaguardar otros órganos frente a formas similares de lesión aguda.
Cita: Fu, Y., Xiang, Y., Han, Y. et al. DUSP26 protects against acute kidney injury by dephosphorylating p53 at serine 312. Nat Commun 17, 3208 (2026). https://doi.org/10.1038/s41467-026-69688-3
Palabras clave: lesión renal aguda, células del túbulo renal, señalización p53, regulación epigenética, muerte celular