Clear Sky Science · ru
DUSP26 защищает от острой почечной недостаточности, дефосфорилируя p53 на серине 312
Почему стресс почек важен для всех
Острая почечная недостаточность — это внезапное падение функции почек, которое может возникнуть во время крупной операции, при тяжелой инфекции, обезвоживании или при лечении рака. Она часто встречается в больницах и повышает риск необходимости диализа, продлевает время пребывания в ОИТ и повышает вероятность развития хронической болезни почек в будущем. Тем не менее у врачей пока нет целевого лекарства, которое напрямую защищало бы рабочие клетки почки. В этом исследовании описан встроенный защитный переключатель внутри этих клеток и показано, как его включение или выключение может кардинально изменить исход — повреждение или сохранение почки.
Скрытый защитник внутри клеток почки
Авторы сосредоточились на тонких канальцах почки, которые фильтруют и тонко настраивают нашу кровь. Анализируя несколько крупных человеческих наборов данных с помощью современных методов машинного обучения, они выделили ген DUSP26, который последовательно обнаруживался в пониженной экспрессии у людей с острой почечной недостаточностью по сравнению со здоровыми почками. При изучении образцов биопсии человека оказалось, что проксимальные тубулярные клетки — те, что выполняют основную работу почки — содержали резко сниженное количество белка DUSP26 во время повреждения, и эта потеря тесно коррелировала с более тяжелыми повреждениями тканей и ухудшением функции почек. Это указывало на то, что DUSP26 обычно помогает этим клеткам противостоять стрессу.
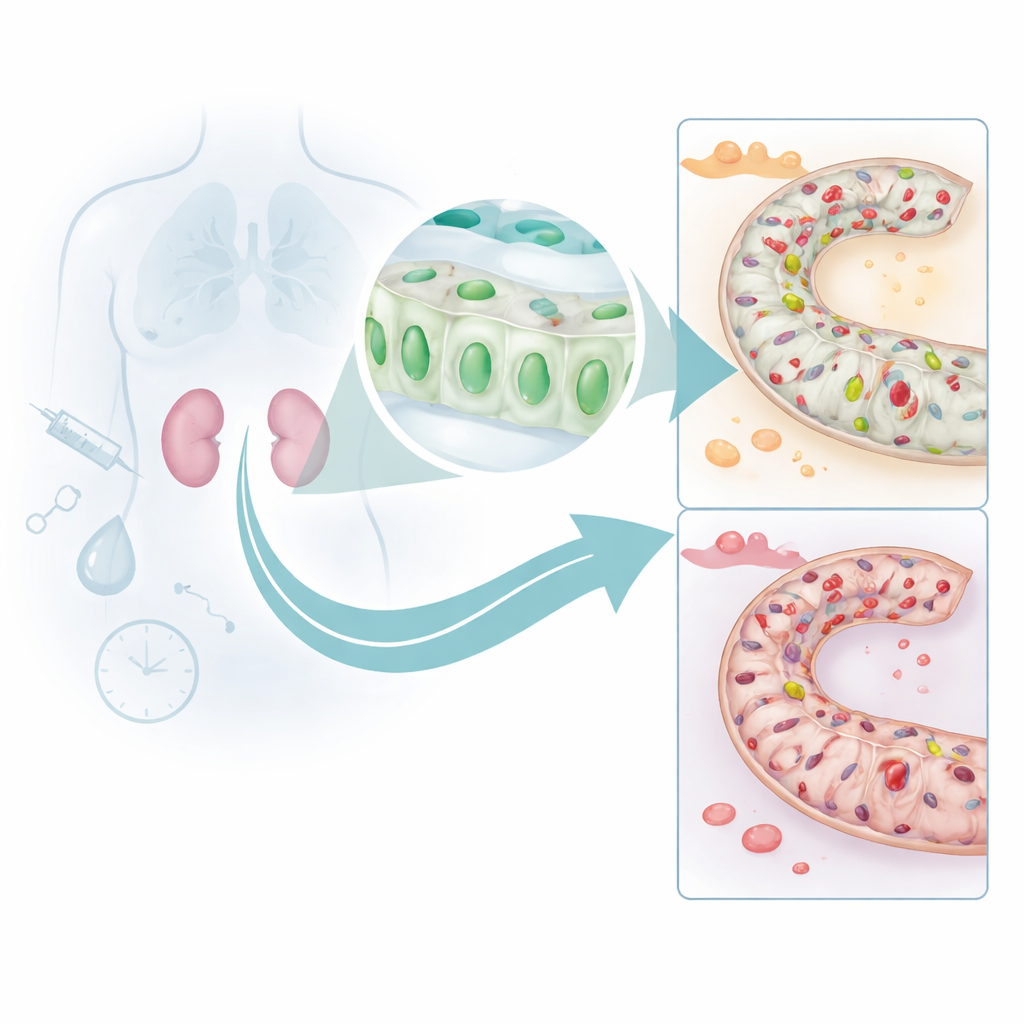
Как щит почки выключают
Чтобы понять, почему уровни DUSP26 падают, команда обратилась к мышиным моделям двух распространенных форм почечного стресса: нефротоксичности, вызванной химиотерапевтическим препаратом, и эпизода ишемии с реперфузией. В обеих ситуациях уровни DUSP26 в почках падали параллельно с ростом клеточной гибели. Авторы проследили эту потерю до химических меток, называемых метилированием ДНК, которые наносятся по регуляторной области гена DUSP26. Эти метки действуют как куски ленты над выключателем света, препятствуя включению гена. Эксперименты на культивируемых почечных клетках показали, что при повреждении метилирование увеличивается и DUSP26 выключается, а ферменты, ответственные за добавление этих меток, привлекаются к промотору гена. У мышей с ишемией‑реперфузией глубокое секвенирование подтвердило, что многие сайты в той же промоторной области становятся сильно метилированными.
Выключение и включение защиты в животных
Далее исследователи спросили, что произойдет, если этот молекулярный щит убрать или усилить. В культуре клеток блокирование DUSP26 с помощью генетических инструментов или малой молекулы приводило к возрастанию активации каспазы‑3, ключевого «исполнителя» программируемой клеточной смерти, после токсического воздействия или нехватки кислорода. Усиление экспрессии DUSP26 давало обратный эффект — снижало гибель клеток. У мышей предобработка ингибитором DUSP26 перед повреждением почек вызывала более высокий уровень азотистых отходов в крови, больше микроскопических повреждений и больше умирающих тубулярных клеток. Напротив, мыши, генетически сконструированные так, чтобы переэкспрессировать DUSP26 специально в проксимальных тубулах, демонстрировали впечатляющую защиту от как лекарственно‑индуцированного, так и ишемического повреждения — лучшую функцию почек и меньшее повреждение тканей. Эти эксперименты, демонстрирующие как потерю, так и усиление функции, вместе выявляют DUSP26 как мощного хранителя целостности канальцев.
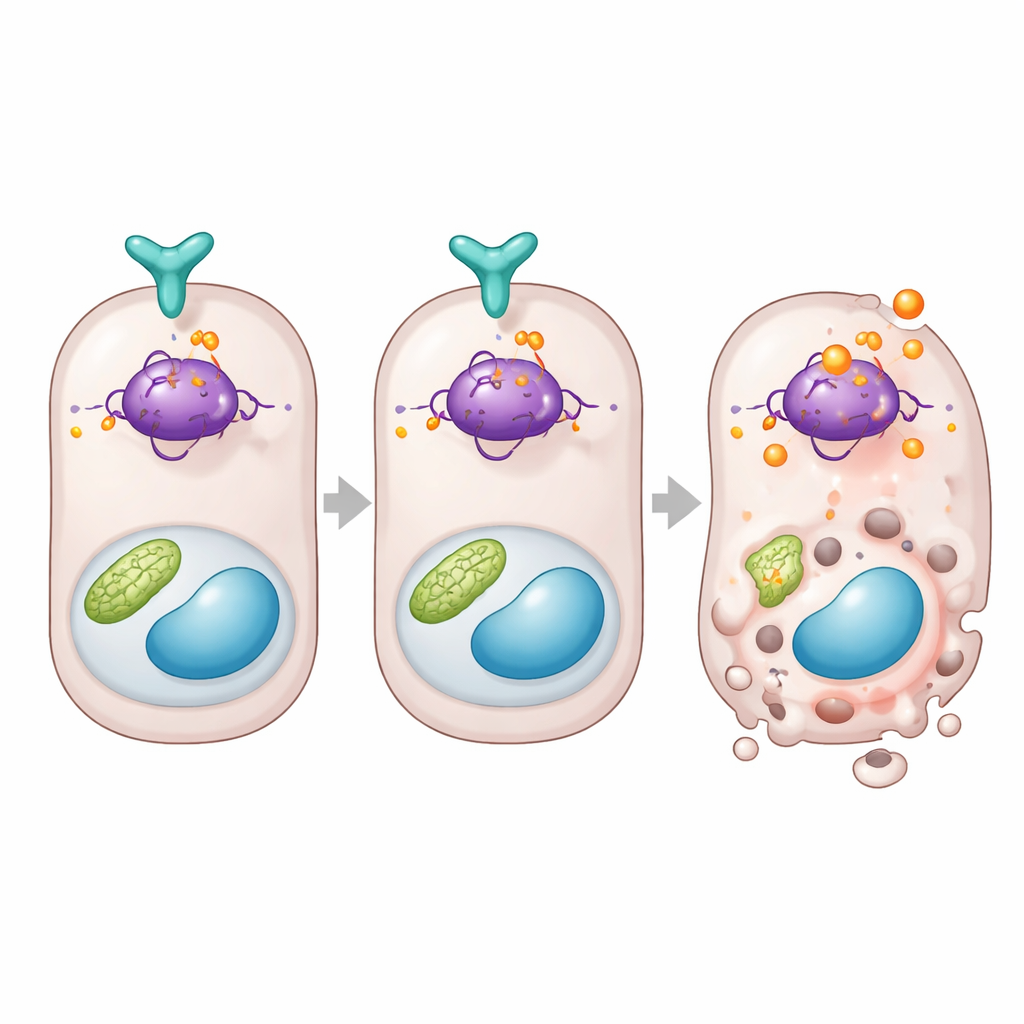
Прямой тормоз белка, решающего судьбу клетки
Углубляясь дальше, исследование связывает DUSP26 с p53 — известным белком, который решает, отремонтирует ли подвергшаяся стрессу клетка себя или саморазрушится. Команда обнаружила, что при низком уровне DUSP26 в человеческих данных или в почках мышей повышалась активность p53‑зависимых генов смерти, таких как Bax и Puma. В клетках DUSP26 физически связывался с p53 и селективно удалял фосфатную группу с одного специфического участка белка, известного как серин 312 в мышах. При отсутствии DUSP26 этот сайт становился сильно модифицированным, активность p53 возрастала, и включались гены, стимулирующие смерть. Чтобы доказать важность именно этого участка, авторы воссоздали почечные клетки и мышей с версией p53, которую больше нельзя модифицировать в этой позиции. Эти клетки и животные оказались значительно более устойчивыми к повреждению почек: у них было меньше умирающих тубулярных клеток и меньше дисфункции органа, хотя другие компоненты системы p53 оставались нетронутыми.
От молекулярного понимания к будущим терапиям
В целом работа описывает четкую цепочку событий: стресс почек увеличивает метилирование ДНК в гене DUSP26, снижая содержание белка DUSP26 в проксимальных тубулах. При уменьшении DUSP26 p53 остается фосфорилированным в критической позиции, его активность повышается и он запускает экспрессию генов, подталкивающих клетки к гибели. Восстановление DUSP26 или имитация его действия в отношении этого единственного сайта подавляет программу смерти и сохраняет ткань почки. Для пациентов это значит, что тщательно подобранные лекарства или ген‑нацеливающие подходы, усиливающие активность DUSP26 — или специфически уменьшающие фосфорилирование p53 в этой позиции — могли бы в будущем помочь защитить почки во время операций, химиотерапии или тяжелых заболеваний, а возможно, и другие органы от аналогичных форм острого повреждения.
Цитирование: Fu, Y., Xiang, Y., Han, Y. et al. DUSP26 protects against acute kidney injury by dephosphorylating p53 at serine 312. Nat Commun 17, 3208 (2026). https://doi.org/10.1038/s41467-026-69688-3
Ключевые слова: острая почечная недостаточность, клетки почечных канальцев, сигнализация p53, эпигенетическая регуляция, клеточная гибель