Clear Sky Science · it
DUSP26 protegge dall'insufficienza renale acuta defosforilando p53 alla serina 312
Perché lo stress renale riguarda tutti
L'insufficienza renale acuta è un calo improvviso della funzione renale che può manifestarsi durante grandi interventi chirurgici, infezioni gravi, disidratazione o trattamenti oncologici. È comune negli ospedali e aumenta il rischio di necessità di dialisi, di degenze più lunghe in terapia intensiva e, successivamente, di evoluzione verso malattia renale cronica. Eppure i medici non dispongono ancora di farmaci mirati che proteggano direttamente le cellule funzionanti del rene. Questo studio mette in luce un interruttore protettivo intrinseco in quelle cellule e mostra come attivarlo o disattivarlo possa cambiare drasticamente se i reni vengono danneggiati o risparmiati.
Un difensore nascosto all'interno delle cellule renali
Gli autori si sono concentrati sui piccoli tubuli all'interno del rene che filtrano e regolano finemente il sangue. Analizzando diversi grandi dataset umani con strumenti di machine learning moderni, hanno identificato un gene chiamato DUSP26 che risultava costantemente espresso a livelli più bassi nelle persone con insufficienza renale acuta rispetto a soggetti con reni sani. Esaminando campioni bioptici umani, hanno rilevato che le cellule del tubulo prossimale — quelle che compiono la maggior parte del lavoro renale — presentavano quantità nettamente ridotte della proteina DUSP26 durante l'insulto, e questa perdita correla strettamente con danno tissutale più grave e funzione renale peggiorata. Ciò suggerisce che DUSP26 aiuta normalmente queste cellule a resistere allo stress.
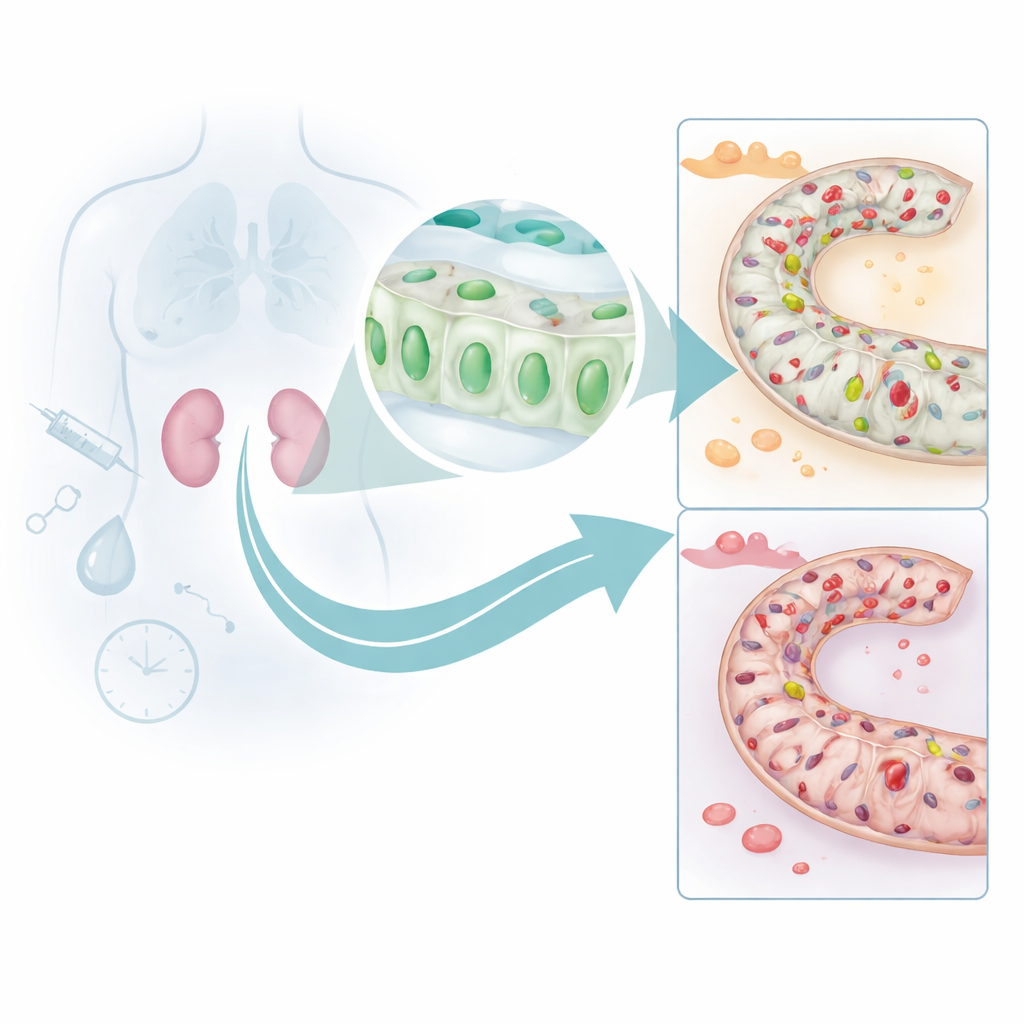
Come lo scudo renale viene spento
Per capire perché i livelli di DUSP26 diminuiscano, il gruppo ha utilizzato modelli murini di due forme comuni di stress renale: un farmaco chemioterapico tossico per il rene e un periodo di insufficiente flusso sanguigno seguito da riperfusione. In entrambi i casi, i livelli di DUSP26 nel rene calavano in parallelo con l'aumento della morte cellulare. Hanno ricondotto questa perdita a marcatori chimici, chiamati metilazioni del DNA, depositati nella regione di controllo del gene DUSP26. Questi marcatori agiscono come pezzi di nastro su un interruttore, impedendo l'attivazione del gene. Esperimenti in colture cellulari renali hanno mostrato che l'insulto aumenta la metilazione e spegne DUSP26, e che gli enzimi responsabili dell'aggiunta di questi tag vengono richiamati al promotore del gene. In topi con danno da ischemia‑riperfusione, il sequenziamento profondo ha confermato che molti siti all'interno della stessa regione promotrice diventano fortemente metilati.
Spegnere e riaccendere la protezione negli animali
I ricercatori hanno poi chiesto cosa accade se questo scudo molecolare viene rimosso o rafforzato. In coltura cellulare, bloccare DUSP26 con strumenti genetici o con una piccola molecola ha portato a una maggiore attivazione della caspasi‑3, un esecutore chiave della morte cellulare programmata, dopo stress tossico o ipossico. Potenziare DUSP26 ha avuto l'effetto opposto, riducendo la morte cellulare. Nei topi, il pretrattamento con l'inibitore di DUSP26 prima dell'insulto renale ha causato livelli di scarto ematico più alti, più danno microscopico e più cellule tubulari in via di morte. Al contrario, topi ingegnerizzati per sovraesprimere DUSP26 specificamente nei tubuli prossimali hanno mostrato una protezione evidente sia dall'insulto indotto da farmaco sia da quello ischemico, con migliore funzione renale e minor danno tissutale. Questi esperimenti di guadagno e perdita di funzione rivelano congiuntamente DUSP26 come un potente guardiano dell'integrità tubulare.
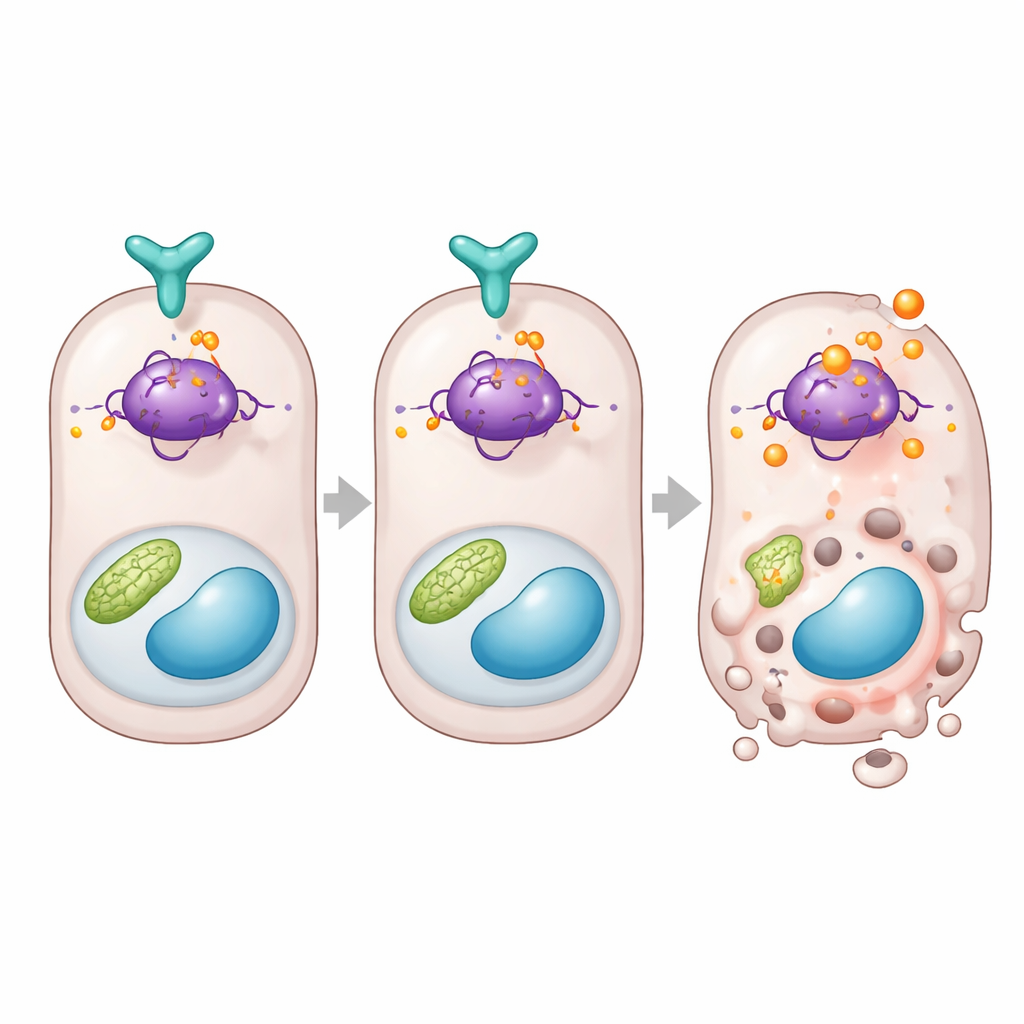
Un freno diretto sulla proteina che decide la morte cellulare
Approfondendo, lo studio collega DUSP26 a p53, una proteina nota che decide se una cellula stressata si ripara o si autodistrugge. Il gruppo ha scoperto che quando DUSP26 era basso nei dati umani o nei reni murini, i geni controllati da p53 che promuovono la morte, come Bax e Puma, risultavano sovraespressi. In cellule, DUSP26 si legava fisicamente a p53 e rimuoveva selettivamente un gruppo fosfato da un sito specifico della proteina, noto come serina 312 nei topi. In assenza di DUSP26, questo sito diventava fortemente modificato, l'attività di p53 aumentava e i geni pro‑morte venivano attivati. Per dimostrare l'importanza di questo sito, gli autori hanno ricostruito cellule renali e topi con una versione di p53 che non poteva più essere modificata in quel punto. Quelle cellule e quegli animali erano molto più resistenti all'insulto renale, con meno cellule tubulari morenti e minore disfunzione d'organo, nonostante altre parti del sistema p53 rimanessero intatte.
Dall'intuizione molecolare a future terapie
Complessivamente, il lavoro delinea una catena di eventi chiara: lo stress renale aumenta la metilazione del DNA sul gene DUSP26, riducendo la proteina DUSP26 nei tubuli prossimali. Con meno DUSP26 disponibile, p53 rimane fosforilato in un sito critico, diventa più attivo e guida l'espressione di geni che spingono le cellule verso la morte. Ripristinare DUSP26, o imitare la sua azione su quel singolo sito, attenua questo programma di morte e preserva il tessuto renale. Per i pazienti, ciò suggerisce che farmaci progettati con cura o approcci mirati al gene che aumentino l'attività di DUSP26 — o che riducano specificamente la fosforilazione di p53 in questo sito — potrebbero un giorno contribuire a proteggere i reni durante interventi chirurgici, chemioterapia o malattie gravi, e forse proteggere anche altri organi da forme simili di danno acuto.
Citazione: Fu, Y., Xiang, Y., Han, Y. et al. DUSP26 protects against acute kidney injury by dephosphorylating p53 at serine 312. Nat Commun 17, 3208 (2026). https://doi.org/10.1038/s41467-026-69688-3
Parole chiave: insufficienza renale acuta, cellule dei tubuli renali, segnalazione di p53, regolazione epigenetica, morte cellulare