Clear Sky Science · fr
DUSP26 protège contre les lésions rénales aiguës en déphosphorylant p53 à la sérine 312
Pourquoi le stress rénal nous concerne tous
La lésion rénale aiguë est une chute soudaine de la fonction rénale qui peut survenir lors d’une chirurgie majeure, d’une infection sévère, d’une déshydratation ou d’un traitement anti‑cancéreux. Elle est fréquente à l’hôpital et augmente le risque de nécessiter une dialyse, de prolonger le séjour en réanimation et de développer ultérieurement une maladie rénale chronique. Pourtant, les médecins ne disposent toujours pas de médicament ciblé qui protège directement les cellules de travail du rein. Cette étude met au jour un interrupteur protecteur intégré à l’intérieur de ces cellules et montre comment l’activer ou l’inhiber peut modifier profondément le devenir des tissus rénaux, entre dommage et protection.
Un défenseur caché à l’intérieur des cellules rénales
Les auteurs se sont concentrés sur les petits tubes à l’intérieur du rein qui filtrent et ajustent précisément notre sang. En exploitant plusieurs grandes bases de données humaines avec des outils modernes d’apprentissage automatique, ils ont identifié un gène nommé DUSP26 qui apparaissait de façon récurrente à des niveaux plus faibles chez les personnes atteintes de lésion rénale aiguë que chez celles ayant des reins sains. L’examen d’échantillons biopsiques humains a montré que les cellules du tubule proximal — celles qui accomplissent la majeure partie du travail rénal — présentaient des quantités fortement réduites de la protéine DUSP26 lors de la lésion, et cette perte était étroitement corrélée à des dommages tissulaires plus importants et à une fonction rénale plus altérée. Cela suggère que DUSP26 aide normalement ces cellules à résister au stress.
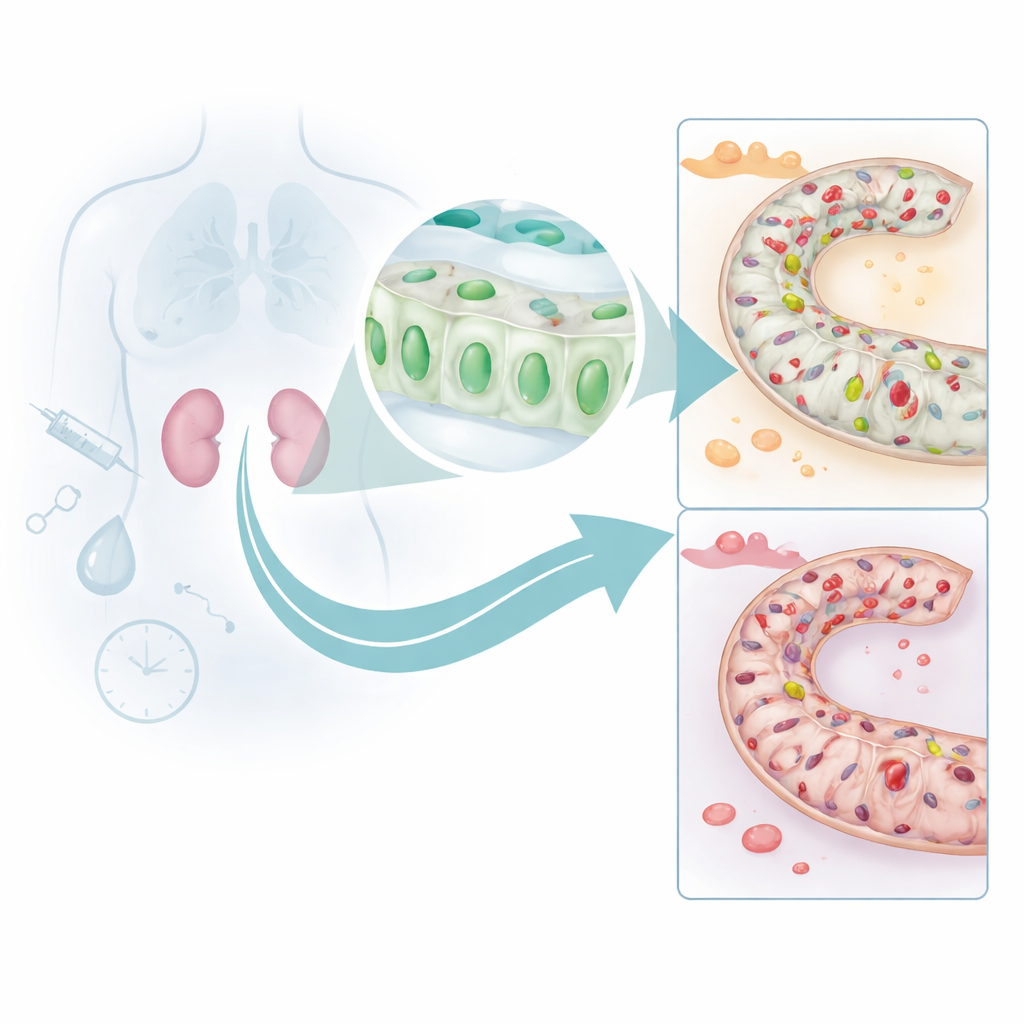
Comment le bouclier rénal est désactivé
Pour comprendre pourquoi les niveaux de DUSP26 diminuent, l’équipe a utilisé des modèles murins de deux formes courantes de stress rénal : un médicament chimiothérapeutique toxique pour le rein et une période d’ischémie suivie de reperfusion. Dans les deux situations, les niveaux de DUSP26 dans le rein chutaient parallèlement à l’augmentation de la mort cellulaire. Ils ont relié cette perte à des marques chimiques, appelées méthylations de l’ADN, apposées sur la région régulatrice du gène DUSP26. Ces marques agissent comme des bandes adhésives sur un interrupteur, empêchant l’activation du gène. Des expériences en culture cellulaire ont montré que la lésion augmentait la méthylation et inhibait DUSP26, et que les enzymes responsables de l’ajout de ces marques étaient recrutées vers le promoteur du gène. Chez les souris soumises à une ischémie‑reperfusion, le séquençage profond a confirmé que de nombreux sites dans cette même région promotrice devenaient fortement méthylés.
Éteindre et rallumer la protection chez l’animal
Les chercheurs ont ensuite testé ce qui se passe si ce bouclier moléculaire est retiré ou renforcé. en culture cellulaire, bloquer DUSP26 avec des outils génétiques ou une petite molécule augmentait l’activation de la caspase‑3, un exécuteur clé de la mort programmée, après un stress toxique ou hypoxique. Augmenter DUSP26 avait l’effet inverse, réduisant la mortalité cellulaire. Chez la souris, un prétraitement avec un inhibiteur de DUSP26 avant la lésion rénale entraînait des taux sanguins de déchets azotés plus élevés, davantage de dommages microscopiques et plus de cellules tubulaires en train de mourir. En revanche, des souris génétiquement modifiées pour surexprimer DUSP26 spécifiquement dans les tubules proximaux montraient une protection frappante contre les lésions induites par le médicament et l’ischémie, avec une meilleure fonction rénale et moins de dégâts tissulaires. Ces expériences de perte et de gain de fonction désignent DUSP26 comme un gardien puissant de l’intégrité tubulaire.
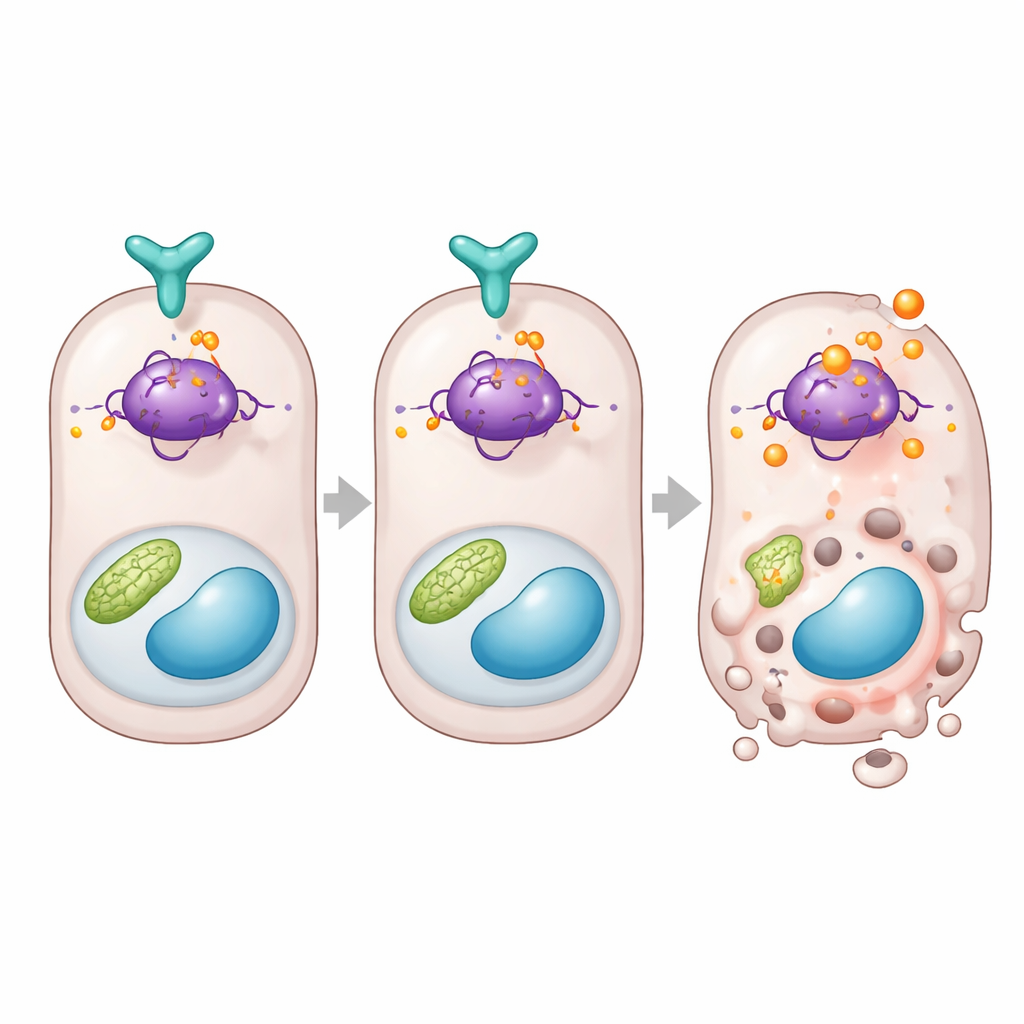
Un frein direct sur la protéine qui décide de la mort cellulaire
En approfondissant, l’étude relie DUSP26 à p53, une protéine célèbre qui décide si une cellule stressée se répare ou s’autodétruit. L’équipe a constaté que lorsque DUSP26 était faible dans les données humaines ou chez la souris, les gènes de mort contrôlés par p53 tels que Bax et Puma étaient augmentés. In vitro, DUSP26 se liait physiquement à p53 et retirait sélectivement un groupe phosphate d’un site spécifique de la protéine, connu sous le nom de sérine 312 chez la souris. En l’absence de DUSP26, ce site devenait fortement modifié, l’activité de p53 augmentait et les gènes pro‑mort étaient activés. Pour démontrer l’importance de ce site, les auteurs ont reconstruit des cellules rénales et des souris avec une version de p53 qui ne pouvait plus être modifiée à cet endroit. Ces cellules et ces animaux étaient beaucoup plus résistants à la lésion rénale, avec moins de cellules tubulaires mourantes et moins de dysfonctionnement de l’organe, même si d’autres composantes du système p53 restaient intactes.
De l’insight moléculaire aux thérapies futures
Au total, le travail décrit une chaîne d’événements claire : le stress rénal augmente la méthylation de l’ADN au niveau du gène DUSP26, abaissant la protéine DUSP26 dans les tubules proximaux. Avec moins de DUSP26 disponible, p53 reste phosphorylé à un site critique, devient plus actif et stimule l’expression de gènes qui poussent les cellules vers la mort. Restaurer DUSP26, ou imiter son action sur ce seul site, atténue ce programme de mort et préserve le tissu rénal. Pour les patients, cela suggère que des médicaments conçus avec soin ou des approches ciblées sur le gène qui augmentent l’activité de DUSP26 — ou réduisent spécifiquement la phosphorylation de p53 en ce site — pourraient un jour aider à protéger les reins lors de chirurgies, de chimiothérapies ou de maladies graves, et peut‑être préserver d’autres organes contre des formes similaires de lésions aiguës.
Citation: Fu, Y., Xiang, Y., Han, Y. et al. DUSP26 protects against acute kidney injury by dephosphorylating p53 at serine 312. Nat Commun 17, 3208 (2026). https://doi.org/10.1038/s41467-026-69688-3
Mots-clés: lésion rénale aiguë, cellules des tubules rénaux, signalisation p53, régulation épigénétique, mort cellulaire