Clear Sky Science · ar
يحمي DUSP26 من الإصابة الحادة بالكِلى عن طريق إزالة الفسفرة عن p53 عند السيرين 312
لماذا يهم إجهاد الكِلى الجميع
الإصابة الحادة بالكِلى هي انخفاض مفاجئ في وظيفة الكِلى يمكن أن يحدث أثناء جراحة كُبرى أو عدوى شديدة أو الجفاف أو علاج السرطان. وهي شائعة في المستشفيات وتزيد من خطر الحاجة إلى غسيل كِلوى، والبقاء لفترة أطول في العناية المركزة، وتطور مرض كِلوى مزمن لاحقًا. ومع ذلك، لا يزال الأطباء يفتقرون إلى دواء متخصص يحمي خلايا الكِلى العاملة مباشرة. تكشف هذه الدراسة عن مفتاح وقائي داخلي داخل تلك الخلايا وتبيّن كيف أن تشغيله أو إيقافه يمكن أن يغيّر بشكل كبير ما إذا كانت الكِلى تتضرر أو تُحفظ.
مدافع مخفي داخل خلايا الكِلى
ركّز الباحثون على الأنابيب الدقيقة داخل الكِلى التي تفرز وتُنقِّح دمنا. من خلال التنقيب في عدة مجموعات بيانات بشرية كبيرة باستخدام أدوات تعلّم آلي حديثة، حدّدوا جينًا يُدعى DUSP26 كان يظهر باستمرار عند مستويات أقل في الأشخاص المصابين بالإصابة الحادة بالكِلى مقارنة بأصحاب الكِلى السليمة. وعند فحص عينات خزعة بشرية، وجدوا أن خلايا الأنابيب القريبة — وهي الخلايا التي تقوم بالجزء الأكبر من عمل الكِلى — كان لديها كميات منخفضة جدًا من بروتين DUSP26 أثناء الإصابة، وكان هذا النقص مرتبطًا بشكل وثيق بضرر أنسجة أسوأ ووظيفة كِلوية أدنى. هذا يوحي بأن DUSP26 يساعد عادة هذه الخلايا على مقاومة الإجهاد.
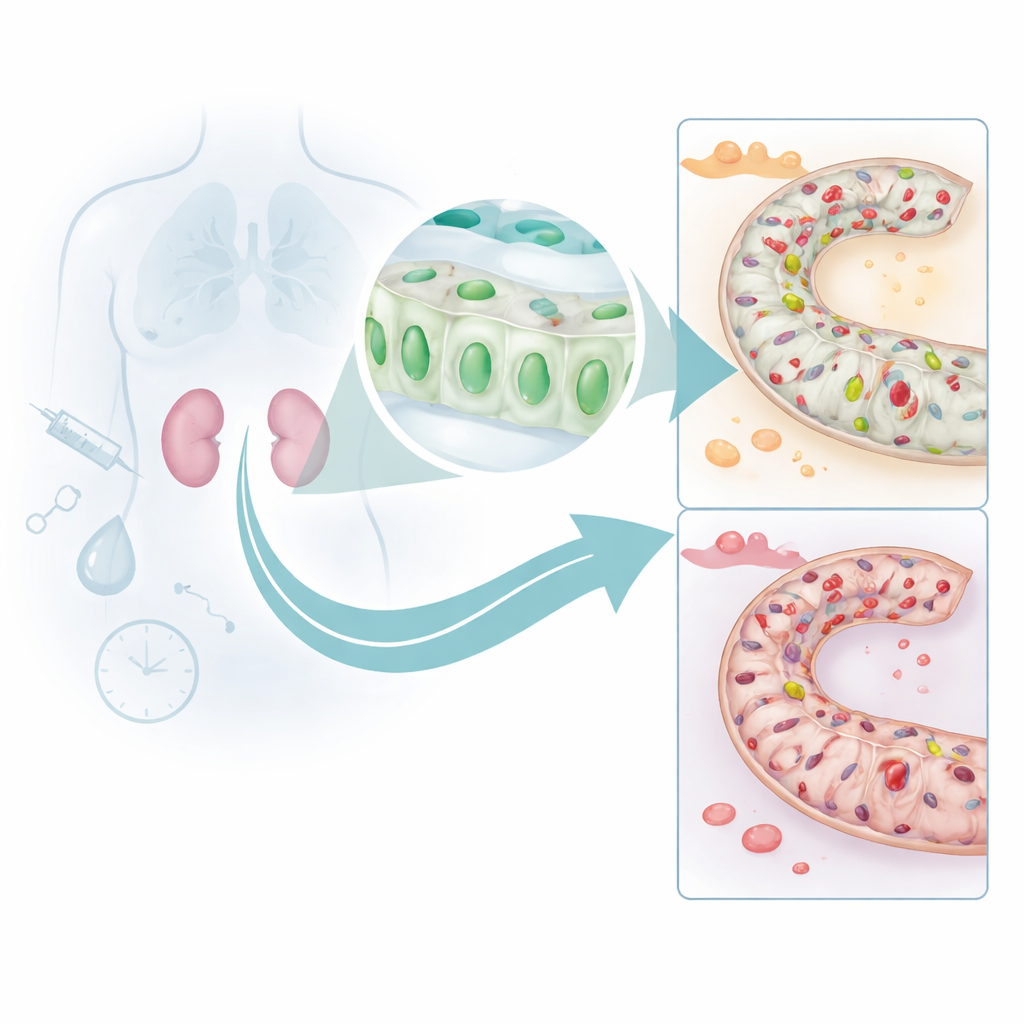
كيف يُطفأ درع الكِلى
لفهم سبب انخفاض مستويات DUSP26، اتجه الفريق إلى نماذج فأرية لنوعين شائعين من ضغوط الكِلى: دواء كيماوي سام للكِلى وفترة من انقطاع تدفُّق الدم تليها إعادة التروية. في كلتا الحالتين، انخفضت مستويات DUSP26 في الكِلى بالتوازي مع ازدياد موت الخلايا. ونسبوا هذا النقص إلى علامات كيميائية تسمى مثيلة الحمض النووي (DNA methylation) وُضعت عبر منطقة التحكم في جين DUSP26. تعمل هذه العلامات كشرائط تغطي مفتاحًا وإيقافًا، مانعةً تشغيل الجين. أظهرت تجارب في خلايا كِلوية مزروعة أن الإصابة زادت المثيلة وأغلقت DUSP26، وأن الإنزيمات المسؤولة عن إضافة هذه العلامات تجمعت عند مُحَرِّك الجين. وفي الفئران المصابة بنقص التروية وإعادة التروية، أكدت تسلسلات عميقة أن مواقع عديدة داخل نفس منطقة المُحَرِّك أصبحت مثيلة بشدة.
إطفاء وتشغيل الحماية في الحيوان
سأل الباحثون بعد ذلك ماذا يحدث إذا أُزيل هذا الدرع الجزيئي أو عُزّز. في الزرع الخلوي، أدى تثبيط DUSP26 بأدوات جينية أو بدواء جزيئي صغير إلى مزيد من تنشيط الكاسبيز‑3، وهو منفذ رئيسي لبرنامج موت الخلايا المبرمج، بعد التعرض للسموم أو نقص الأكسجة. أما تعزيز DUSP26 فكان له أثر معاكس، إذ خفض موت الخلايا. في الفئران، أدى المعالَجة المسبقة بمثبط DUSP26 قبل إصابة الكِلى إلى رفع مستويات النفايات في الدم، ومزيد من الضرر المجهري، ومزيد من خلايا الأنابيب الميتة. على النقيض من ذلك، أظهرت الفئران المصممة لإنتاج كميات زائدة من DUSP26 تحديدًا في الأنابيب القريبة حماية لافتة من كل من الإصابة الدوائية ونقص التروية، مع وظيفة كِلوية أفضل وضرر نسجي أقل. تكشف هذه تجارب الكسب والخسارة معًا أن DUSP26 هو حارس قوي لنزاهة الأنابيب.
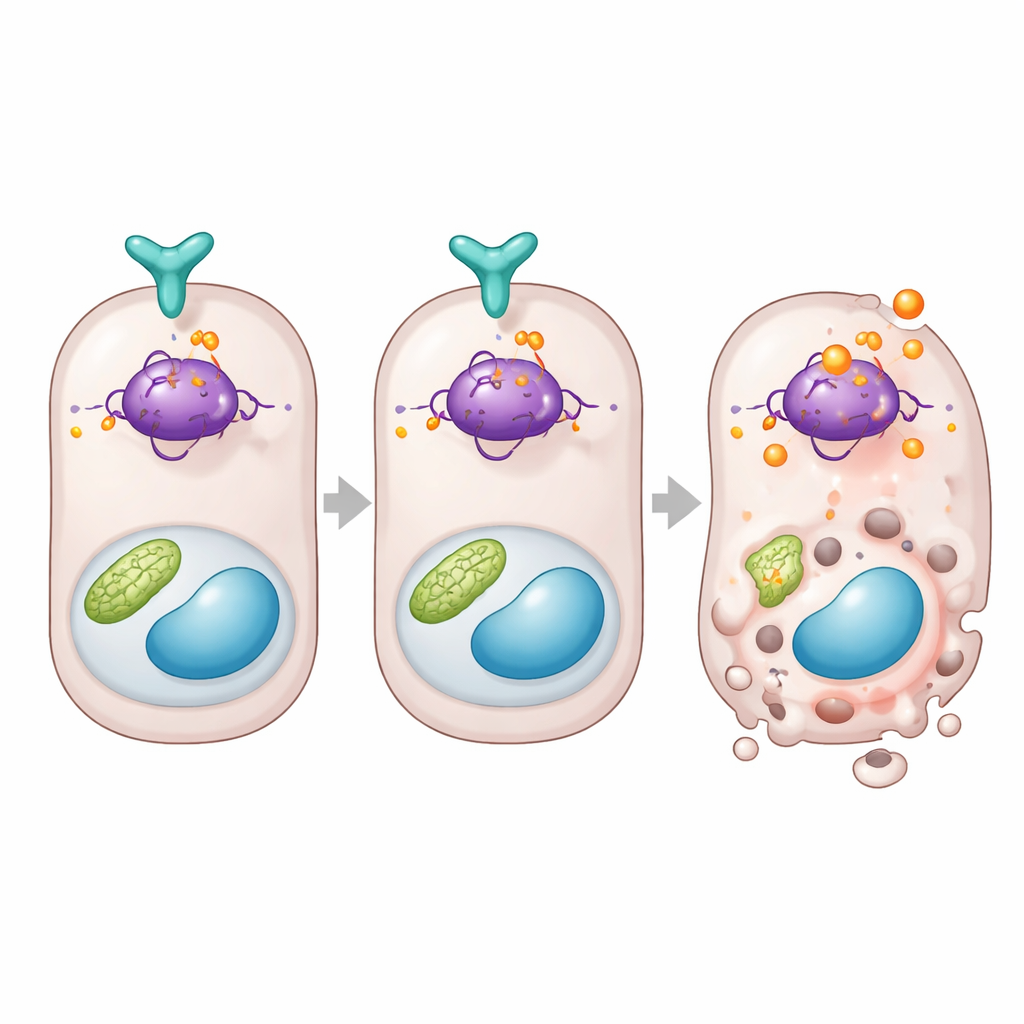
فرملة مباشرة على بروتين اتخاذ القرار بالموت
عند التعمق أكثر، تربط الدراسة DUSP26 بـ p53، البروتين الشهير الذي يقرّر ما إذا كانت الخلية المُجهدة تُصلِح نفسها أم تُدمر ذاتيًا. وجد الفريق أنه عندما كان DUSP26 منخفضًا في بيانات بشرية أو في كِلى الفئران، ارتفعت مستويات جينات الموت التي يتحكم بها p53 مثل Bax وPuma. في الخلايا، ارتبط DUSP26 ماديًا بـ p53 وأزاله انتقائيًا لمجموعة فوسفات من موقع محدد على البروتين، المعروف بالسيرين 312 في الفئران. عندما غاب DUSP26، أصبح هذا الموقع شديد التعديل، وارتفعت نشاطية p53، وتفعّلت الجينات المروِّجة للموت. لإثبات أهمية هذا الموقع، أعاد المؤلفون بناء خلايا كِلوية وفئران بنسخة من p53 لا يمكن تعديلها عند تلك البقعة. كانت تلك الخلايا والحيوانات أكثر مقاومة للإصابة الكِلوية بكثير، مع عدد أقل من خلايا الأنابيب الميتة وقصور أقل في العضو، رغم أن أجزاء أخرى من نظام p53 بقيت سليمة.
من البصيرة الجزيئية إلى علاجات مستقبلية
بالنظر إلى الصورة الكاملة، توضح النتائج سلسلة أحداث واضحة: يزيد إجهاد الكِلى من مثيلة الحمض النووي على جين DUSP26، مما يخفض بروتين DUSP26 في الأنابيب القريبة. ومع قلة DUSP26 المتاحة، يبقى p53 مفسفرًا عند موقع حاسم، فترتفع نشاطيته وتدفع تعبير جينات تدفع الخلايا نحو الموت. استعادة DUSP26، أو محاكاة فعله على ذلك الموقع الواحد، يخفف هذا البرنامج القاتل ويحافظ على نسيج الكِلى. وبالنسبة للمرضى، يقترح هذا أن أدوية مصممة بعناية أو استراتيجيات موجهة جينيًا لتعزيز نشاط DUSP26 — أو تقليل فسفرة p53 عند هذا الموقع تحديدًا — قد تساعد يومًا ما في حماية الكِلى أثناء الجراحة أو العلاج الكيميائي أو المرض الشديد، وربما تحمي أعضاء أخرى من أشكال مماثلة من الإصابة الحادة.
الاستشهاد: Fu, Y., Xiang, Y., Han, Y. et al. DUSP26 protects against acute kidney injury by dephosphorylating p53 at serine 312. Nat Commun 17, 3208 (2026). https://doi.org/10.1038/s41467-026-69688-3
الكلمات المفتاحية: الإصابة الحادة بالكِلى, خلايا أنابيب الكِلى, إشارة p53, الضبط فوق الجيني, موت الخلايا