Clear Sky Science · pt
DUSP26 protege contra lesão renal aguda desfosforilando p53 na serina 312
Por que o estresse renal importa para todos
A lesão renal aguda é uma queda súbita da função renal que pode ocorrer durante grandes cirurgias, infecções graves, desidratação ou tratamentos contra o câncer. É comum em hospitais e aumenta o risco de necessidade de diálise, permanência prolongada na UTI e desenvolvimento posterior de doença renal crônica. Ainda assim, os médicos não dispõem de um medicamento direcionado que proteja diretamente as células funcionais do rim. Este estudo revela um interruptor protetor embutido nessas células e mostra como ativá‑lo ou desativá‑lo pode mudar dramaticamente se os rins serão lesionados ou preservados.
Um defensor oculto dentro das células renais
Os autores concentraram‑se nos pequenos túbulos do rim que filtram e afinam o sangue. Ao analisar vários grandes conjuntos de dados humanos com ferramentas modernas de aprendizado de máquina, identificaram um gene chamado DUSP26 que apareceu consistentemente em níveis mais baixos em pessoas com lesão renal aguda do que naquelas com rins saudáveis. Ao examinar amostras de biópsia humana, observaram que as células do túbulo proximal — responsáveis pela maior parte do trabalho renal — exibiam quantidades fortemente reduzidas da proteína DUSP26 durante a lesão, e essa perda acompanhava de perto maior dano tecidual e pior função renal. Isso sugeriu que o DUSP26 normalmente ajuda essas células a resistir ao estresse.
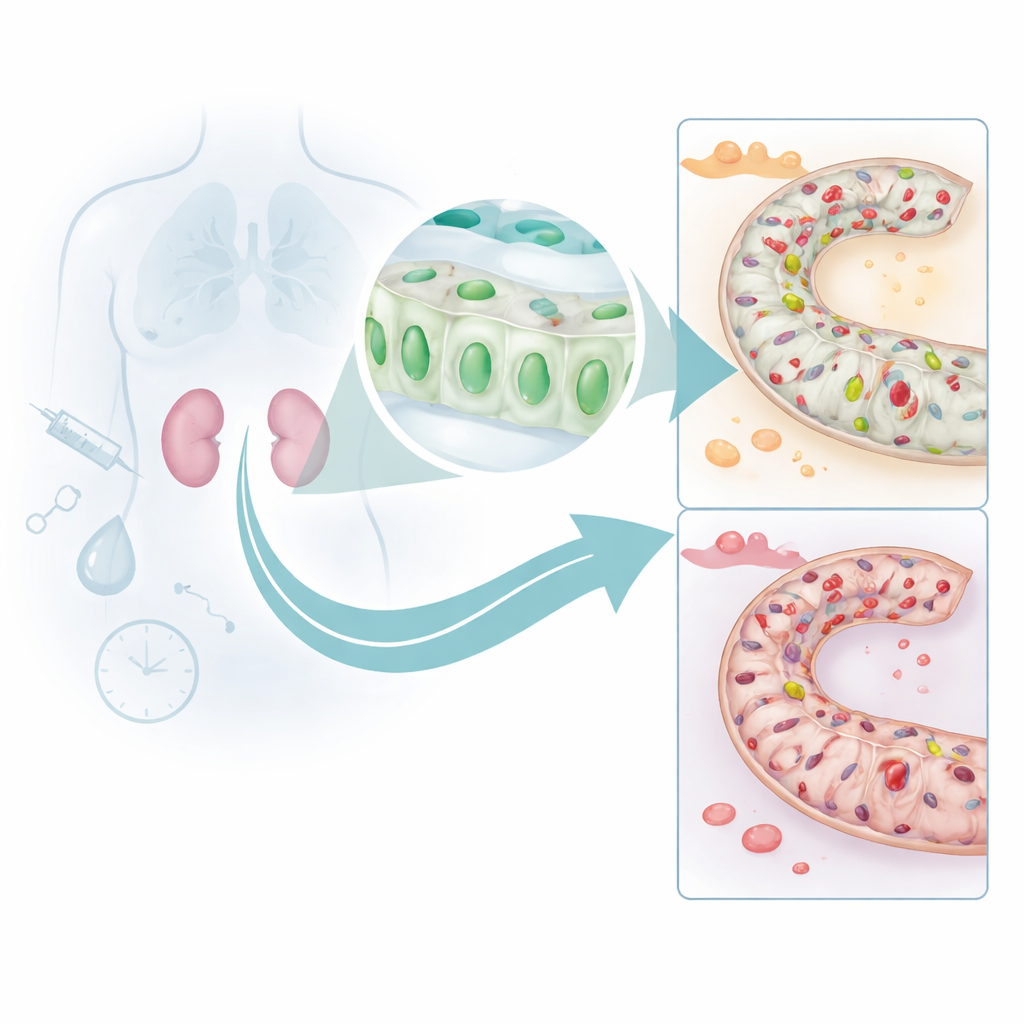
Como o escudo do rim é desligado
Para entender por que os níveis de DUSP26 caem, a equipe recorreu a modelos murinos de duas formas comuns de estresse renal: um quimioterápico tóxico para o rim e um período de fluxo sanguíneo bloqueado seguido de reperfusão. Em ambas as situações, os níveis de DUSP26 no rim diminuíram em paralelo com o aumento da morte celular. Eles atribuíram essa perda a marcas químicas chamadas metilação do DNA, depositadas na região reguladora do gene DUSP26. Essas marcas agem como fitas sobre um interruptor de luz, impedindo que o gene seja ativado. Experimentos em células renais cultivadas mostraram que a lesão aumentou a metilação e silenciou o DUSP26, e que enzimas responsáveis por adicionar essas marcas foram atraídas ao promotor do gene. Em camundongos com lesão por isquemia‑reperfusão, o sequenciamento profundo confirmou que muitos sítios dentro da mesma região promotora tornaram‑se fortemente metilados.
Desligando e ligando a proteção em animais
Os pesquisadores então perguntaram o que acontece se esse escudo molecular for removido ou reforçado. Em cultura celular, bloquear o DUSP26 com ferramentas genéticas ou um pequeno inibidor molecular levou a maior ativação da caspase‑3, um executor chave da morte programada, após estresse tóxico ou de baixo oxigênio. Aumentar o DUSP26 teve o efeito oposto, reduzindo a morte celular. Em camundongos, pré‑tratamento com o inibidor de DUSP26 antes da lesão renal causou níveis mais altos de resíduos no sangue, mais dano microscópico e mais células tubulares morrendo. Em contraste, camundongos programados para superexpressar DUSP26 especificamente nos túbulos proximais mostraram proteção marcante tanto contra lesão induzida por droga quanto isquêmica, com melhor função renal e menor dano tecidual. Esses experimentos de ganho e perda de função revelam juntos o DUSP26 como um guardião poderoso da integridade tubular.
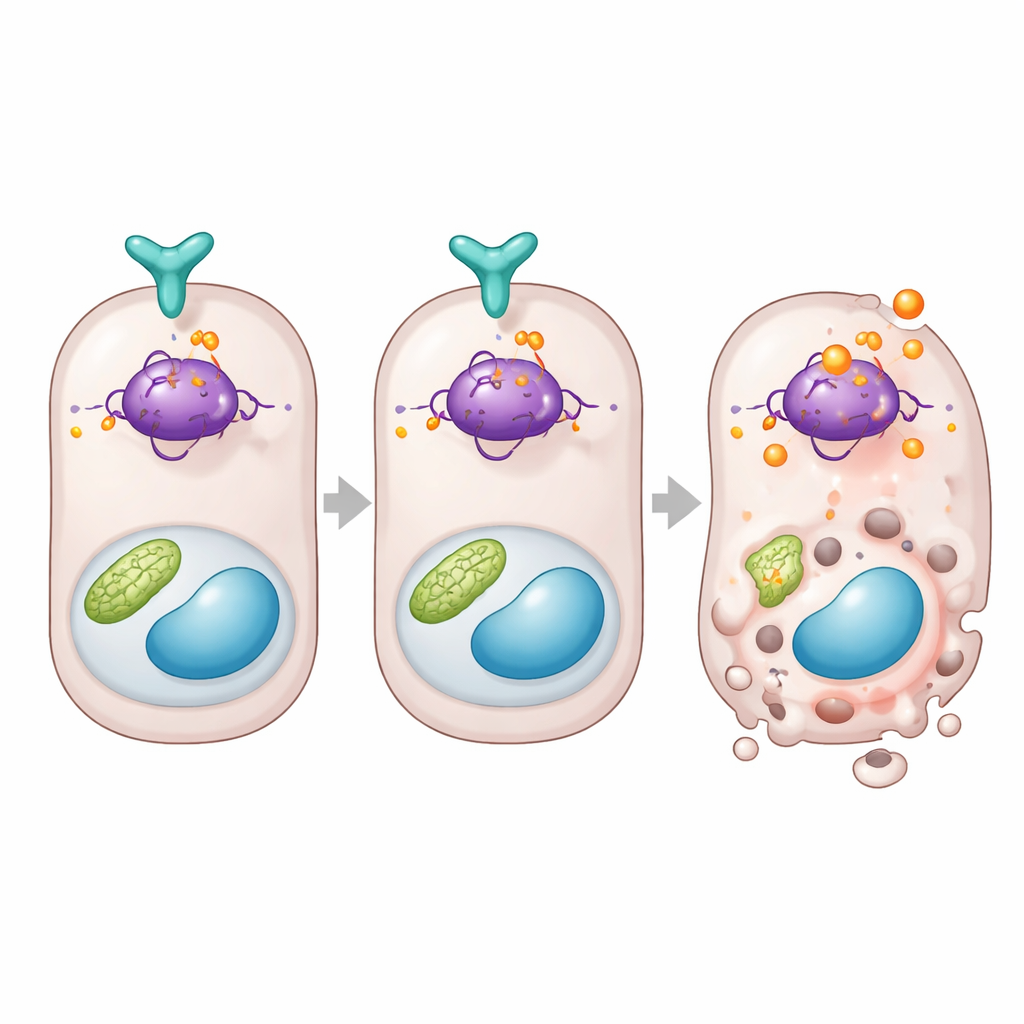
Um freio direto na proteína que decide a morte celular
Investigando mais a fundo, o estudo conecta o DUSP26 ao p53, uma proteína conhecida por decidir se uma célula estressada se repara ou se autodestrói. A equipe descobriu que, quando o DUSP26 estava baixo em dados humanos ou em rins de camundongos, genes de morte controlados por p53, como Bax e Puma, estavam aumentados. Em células, o DUSP26 ligou‑se fisicamente ao p53 e removeu seletivamente um grupo fosfato de um sítio específico da proteína, conhecido como serina 312 em camundongos. Quando o DUSP26 estava ausente, esse sítio tornou‑se fortemente modificado, a atividade do p53 aumentou e genes promotores de morte foram acionados. Para provar a importância desse sítio, os autores reconstruíram células renais e camundongos com uma versão do p53 que não podia mais ser modificada naquele ponto. Essas células e animais foram muito mais resistentes à lesão renal, com menos células tubulares morrendo e menor disfunção do órgão, embora outras partes do sistema p53 permanecessem intactas.
Da compreensão molecular às futuras terapias
Em conjunto, o trabalho delineia uma cadeia clara de eventos: o estresse renal aumenta a metilação do DNA no gene DUSP26, reduzindo a proteína DUSP26 nos túbulos proximais. Com menos DUSP26 disponível, o p53 permanece fosforilado em um sítio crítico, torna‑se mais ativo e impulsiona a expressão de genes que empurram as células rumo à morte. Restaurar o DUSP26, ou imitar sua ação naquele único sítio, atenua esse programa de morte e preserva o tecido renal. Para os pacientes, isso sugere que medicamentos cuidadosamente desenhados ou abordagens direcionadas por genes que aumentem a atividade de DUSP26 — ou que reduzam especificamente a fosforilação do p53 nesse sítio — poderiam um dia ajudar a proteger os rins durante cirurgias, quimioterapia ou doenças graves, e talvez proteger outros órgãos de formas semelhantes de lesão aguda.
Citação: Fu, Y., Xiang, Y., Han, Y. et al. DUSP26 protects against acute kidney injury by dephosphorylating p53 at serine 312. Nat Commun 17, 3208 (2026). https://doi.org/10.1038/s41467-026-69688-3
Palavras-chave: lesão renal aguda, células dos túbulos renais, sinalização p53, regulação epigenética, morte celular