Clear Sky Science · he
DUSP26 מגן מפגיעה כלייתית חריפה על‑ידי דה‑פוספורילציה של p53 בסרין 312
מדוע מצבי לחץ בכליה חשובים לכולנו
נזק כלייתי חריף הוא ירידה פתאומית בתפקוד הכליה שעלולה להתרחש במהלך ניתוח גדול, זיהום חמור, התייבשות או טיפול בסרטן. זה מצב נפוץ בבתי חולים שמעלה את הסיכון לצורך בדיאליזה, לשהייה ממושכת ביחידת טיפול נמרץ ולהתפתחות מאוחרת של מחלת כליות כרונית. למרות זאת, לרופאים עדיין אין תרופה מכוונת שמגנה ישירות על תאי העבודה של הכליה. המחקר הזה חושף מתג מגן פנימי בתאים אלה וממחיש כיצד הדלקה או כיבוי של מתג זה יכולים לשנות באופן דרמטי האם הכליות יינזקו או יישמרו.
מגן חבוי בתוך תאי הכליה
המחברים התמקדו בצינורות הקטנים בתוך הכליה שמסננים ומדייקים את הדם שלנו. באמצעות כרייה של מספר מאגרי נתונים אנושיים גדולים עם כלים של למידת מכונה מודרנית, הם זיהו גן בשם DUSP26 שהופיע בעקביות ברמות נמוכות יותר באנשים עם נזק כלייתי חריף לעומת אלה עם כליות בריאות. בבדיקת דגימות ביופסיה אנושיות התברר שתאי הצינורית הפרוקסימלית — התאים שמבצעים רוב העומס הכלייתי — הכילו כמויות חזקות מופחתות של חלבון DUSP26 בזמן הפגיעה, והירידה הזו תאמה באופן הדוק נזק רקמתי חמור יותר ותפקוד כלייתי גרוע יותר. הנתונים הללו רמזו ש‑DUSP26 מסייע בדרך כלל לתאים אלה לעמוד בלחץ.
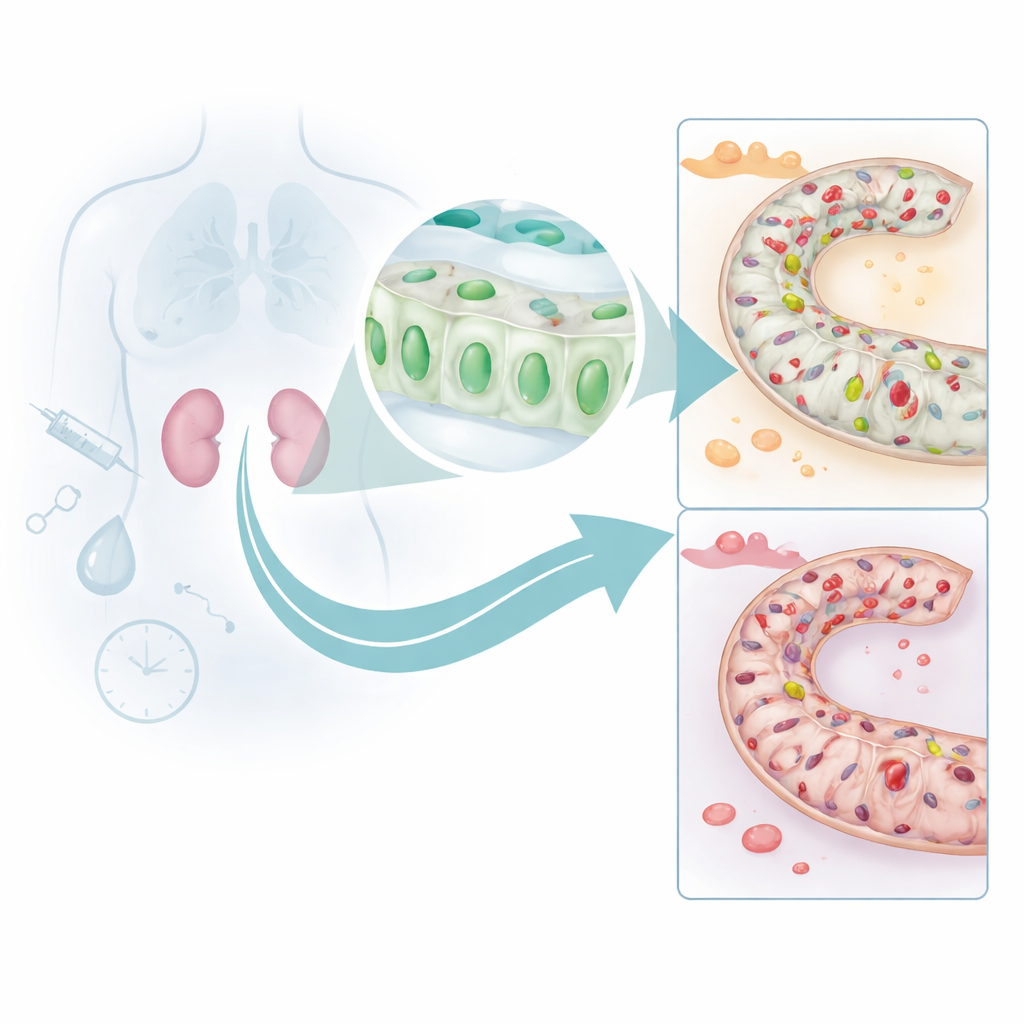
כיצד מגן הכליה מושבת
כדי להבין מדוע רמות DUSP26 יורדות, הצוות פנה למודלים עכבריים של שתי צורות שכיחות של לחץ כלייתי: תרופה כימותרפית רעילה לכליה ותנאי חסימת זרימת דם ואחריו החזרת זרימה (רפרפוזיה). בשני המצבים רמות DUSP26 בכליה ירדו במקביל לעלייה במוות התאי. הם עקבו אחר הירידה הזו עד לתגים כימיים, שנקראים מתילציות DNA, המונצקים באזור בקרה של גן DUSP26. התגים האלה פועלים כמו חתיכות דבק על מתג תאורה ומונעים הפעלה של הגן. ניסויים בתרביות תאים כלייתיים הראו כי פגיעה מגבירה מתילציה ומשתיקה את DUSP26, וכי אנזימים האחראים להוספת התגים נמשכים לפרומוטור של הגן. בעכברים עם פגיעה איסכמית‑רפרפוזיה, רצפי DNA עמוקים אישרו כי אתרים רבים בתוך אותו אזור פרומוטור הפכו למתילטים בעוצמה גבוהה.
הדלקה וכיבוי של ההגנה בבעלי חיים
החוקרים שאלו אז מה קורה אם המגן המולקולרי מוסר או מתחזק. בתרבית התאים, חסימת DUSP26 בעזרת כלים גנטיים או מולקולה קטנה הובילה להגברה של הפעלת קספאז‑3, חלבון מרכזי המבצע מוות תאי מתוכנת, לאחר לחץ רעיל או חוסר חמצן. החזקת רמות DUSP26 הגבירה את ההשפעה ההפוכה וצמצמה את המוות התאי. בעכברים, טיפול מקדים עם מעכב DUSP26 לפני פגיעה בכליה גרם לרמות פסולת בדם גבוהות יותר, נזק מיקרוסקופי רב יותר ויותר תאי צינורית גוססים. לעומת זאת, עכברים מהונדסים המייצרים באופן מופרז DUSP26 ספציפית בצינורות הפרוקסימליים הראו הגנה מרשימה הן מפגיעה הנגרמת על‑ידי תרופה והן מפגיעה איסכמית, עם תפקוד כלייתי טוב יותר ופחות נזק לרקמה. ניסויי רווח‑וחסר פונקציה אלה יחד ממצבים את DUSP26 כשומר רב עוצמה על שלמות הצינורות.
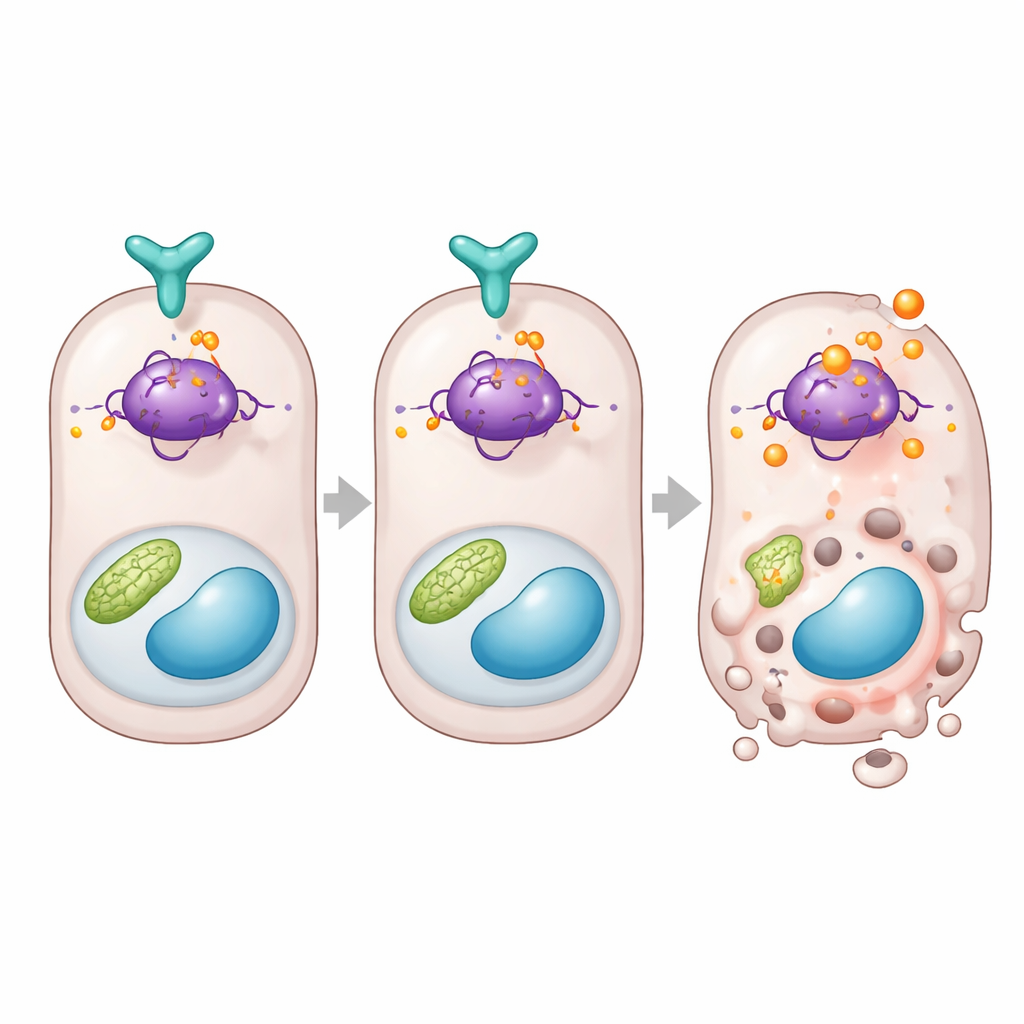
בלם ישיר על חלבון ההחלטה למות התא
בהעמקה נוספת, המחקר מקשר את DUSP26 ל‑p53, חלבון מוכר שמחליט האם תא תחת לחץ יתאושש או יתאבד. הצוות מצא שכאשר DUSP26 היה נמוך בנתונים אנושיים או בכליות עכברים, גנים של p53 המקודדים למוות כגון Bax ו‑Puma הועלו. בתאים, DUSP26 נקשר פיזית ל‑p53 והסיר באופן סלקטיבי קבוצת פוספט מאתר יחיד בחלבון, המוכר כסרין 312 בעכברים. בהיעדר DUSP26, אתר זה הועשר במודיפיקציה, פעילות p53 עלתה וגנים מקדמי המוות הופעלו. כדי להוכיח את חשיבות האתר הזה, המחברים בנו מחדש תאי כליה ועכברים עם גרסה של p53 שלא יכולה עוד לעבור מודיפיקציה באתר זה. תאים ובעלי החיים הללו היו עמידים הרבה יותר לנזק כלייתי, עם פחות תאי צינורית גוססים ופחות אי‑תפקוד של האיבר, אף על פי שחלקים אחרים ממערכת p53 נותרו שלמים.
מתהוות תרופות מתוך הבנה מולקולרית
בצירוף כללי, העבודה משרטטת רצף ברור של אירועים: לחץ כלייתי מעלה את מתילציית ה‑DNA על גן DUSP26, מה שמפחית את חלבון DUSP26 בתאי הצינורית הפרוקסימלית. כש‑DUSP26 זמין פחות, p53 נשאר מזורחן באתר קריטי, פעילותו גוברת והוא מניע את ביטוי גנים שמניעים תאים אל המוות. השבת DUSP26, או חיקוי פעולתו על אותו אתר יחיד, מרכך את תוכנית המוות הזו ושומר על רקמת הכליה. עבור מטופלים, המשמעות היא כי תרופות שנעשות בקפידה או גישות מונחות גנים שמגבירות את פעילות DUSP26 — או שמפחיתות באופן ספציפי את פוספורילציה של p53 באתר זה — עשויות יום אחד לעזור להגן על הכליות במהלך ניתוח, כימותרפיה או מחלה קשה, ואולי גם להגן על איברים אחרים מפגיעות חדות דומות.
ציטוט: Fu, Y., Xiang, Y., Han, Y. et al. DUSP26 protects against acute kidney injury by dephosphorylating p53 at serine 312. Nat Commun 17, 3208 (2026). https://doi.org/10.1038/s41467-026-69688-3
מילות מפתח: נזק כלייתי חריף, תאי צינורות כליה, מעגל איתות p53, ויסות אפיגנטי, מוות תאי