Clear Sky Science · nl
DUSP26 beschermt tegen acuut nierletsel door p53 te dephosphoryleren op serine 312
Waarom nierstress voor iedereen van belang is
Acuut nierletsel is een plotselinge achteruitgang van de nierfunctie die kan optreden tijdens grote operaties, ernstige infecties, uitdroging of kankerbehandelingen. Het komt veel voor in ziekenhuizen en vergroot de kans op dialyse, langere IC-opnamen en later het ontwikkelen van chronische nierziekte. Toch hebben artsen nog geen gerichte medicijnen die direct de werkende niercellen beschermen. Deze studie onthult een ingebouwde beschermingsschakel binnen die cellen en laat zien hoe het omzetten van die schakel dramatisch bepaalt of nieren beschadigen of gespaard blijven.
Een verborgen verdediger in niercellen
De auteurs richtten zich op de kleine buisjes in de nier die ons bloed filteren en verfijnen. Door meerdere grote menselijke datasets met moderne machine‑learningtools te analyseren, identificeerden ze een gen genaamd DUSP26 dat consequent lager tot expressie kwam bij mensen met acuut nierletsel dan bij gezonde controles. Bij onderzoek van menselijke biopsieën bleek dat proximale tubuluscellen—de cellen die het meeste werk in de nier verrichten—sterk verminderde hoeveelheden van het DUSP26-eiwit hadden tijdens letsel, en dat dit verlies nauw samenhing met ernstiger weefselschade en slechtere nierfunctie. Dit suggereerde dat DUSP26 deze cellen normaal helpt om stress te doorstaan.
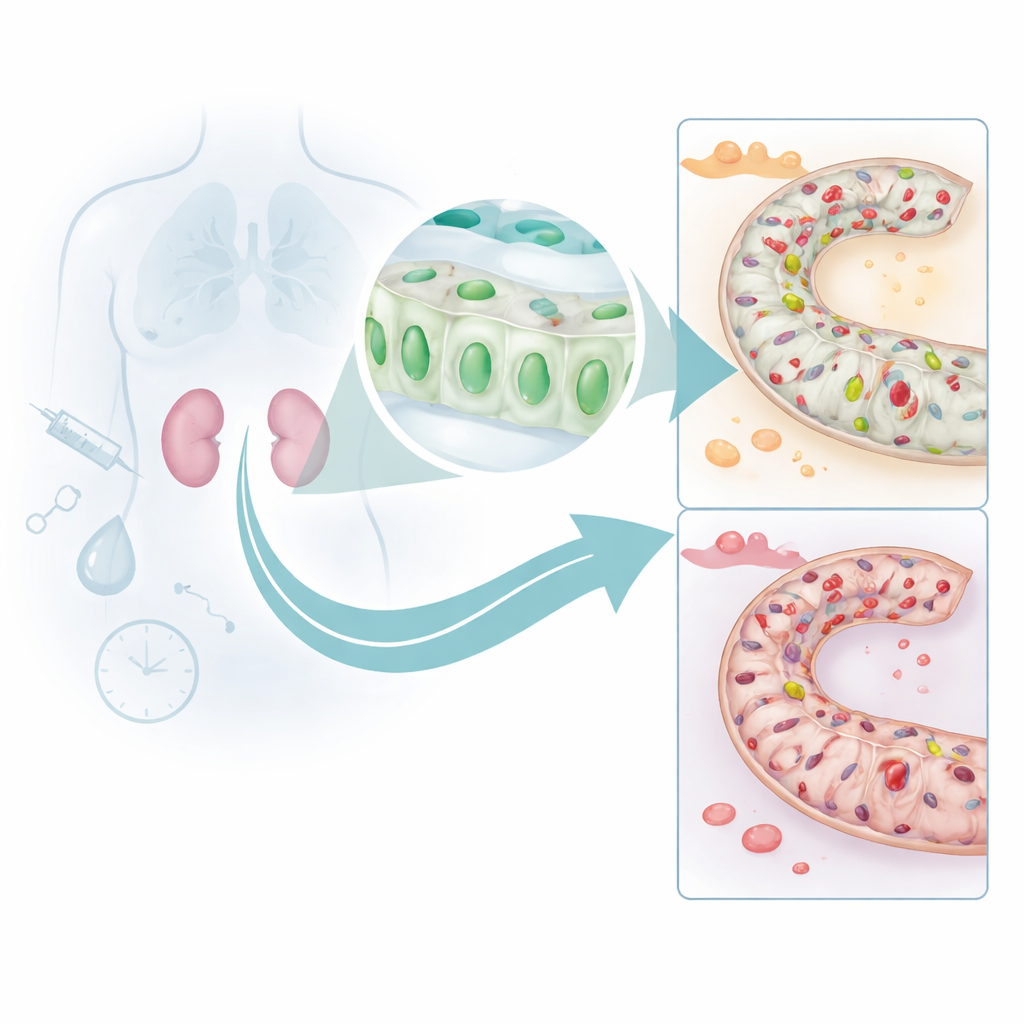
Hoe het nier‑schild wordt uitgezet
Om te begrijpen waarom DUSP26-niveaus dalen, gingen de onderzoekers naar muismodellen van twee veel voorkomende vormen van nierstress: een chemotherapeutisch middel dat nefrotoxisch is en een periode van geblokkeerde bloedtoevoer gevolgd door reperfusie. In beide situaties daalden DUSP26-niveaus in de nier parallel met toenemende celsterfte. Ze herleidden dit verlies tot chemische labels, DNA‑methylatie genoemd, die over het regelgebied van het DUSP26-gen werden aangebracht. Deze labels werken als stukjes tape over een schakelaar en voorkomen dat het gen wordt aangeschakeld. Experimenten in gekweekte niercellen toonden aan dat letsel de methylatie verhoogde en DUSP26 uitschakelde, en dat enzymen die deze labels toevoegen zich naar de promotor van het gen begaven. Bij muizen met ischemie‑reperfusie letsel bevestigde diepe sequencing dat veel plaatsen binnen hetzelfde promotorgebied sterk gemethyleerd waren.
Bescherming uitzetten en inschakelen in dieren
De onderzoekers stelden vervolgens de vraag wat er gebeurt als dit moleculaire schild wordt verwijderd of versterkt. In celkweek leidde het blokkeren van DUSP26 met genetische middelen of een kleinmolecuulremmer tot meer activatie van caspase‑3, een belangrijke uitvoerder van geprogrammeerde celdood, na toxische of laag‑zuurstofstress. Het verhogen van DUSP26 had het tegengestelde effect en verminderde celsterfte. Bij muizen leidde het vooraf behandelen met de DUSP26-remmer voor nierletsel tot hogere bloedafvalwaarden, meer microscopische schade en meer stervende tubuluscellen. Daarentegen vertoonden muizen die speciaal in proximale tubuli teveel DUSP26 produceerden opvallende bescherming tegen zowel medicijngeïnduceerd als ischemisch letsel, met betere nierfunctie en minder weefselschade. Deze experimenten met winst en verlies van functie tonen samen DUSP26 als een krachtige beschermer van tubulaire integriteit.
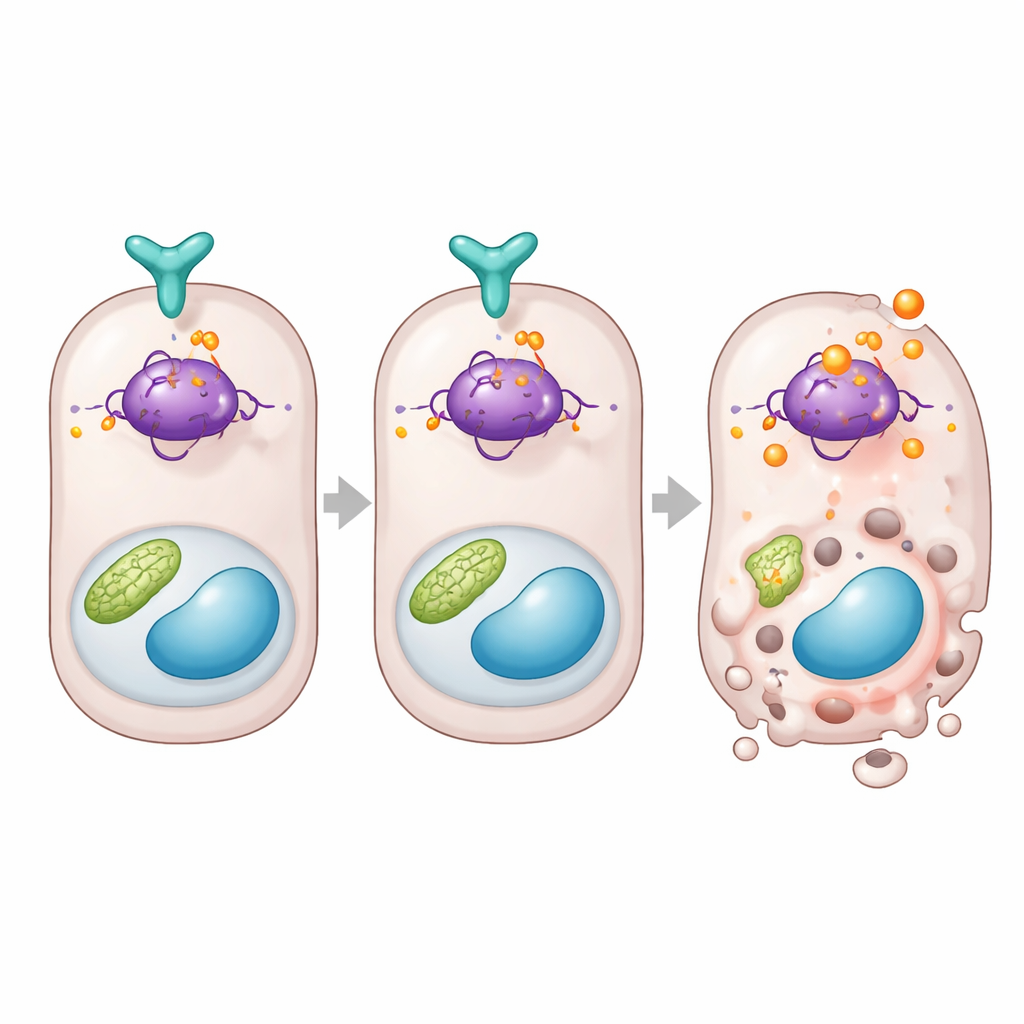
Een directe rem op het doodsbeslissende eiwit van de cel
Dieper gravend verbindt de studie DUSP26 met p53, een bekend eiwit dat bepaalt of een gestreste cel zichzelf herstelt of zelfdestructie toepast. Het team ontdekte dat wanneer DUSP26 laag was in menselijke gegevens of muiernieren, p53‑gereguleerde doodsgenen zoals Bax en Puma verhoogd waren. In cellen bond DUSP26 fysiek aan p53 en verwijderde het selectief een fosfaatgroep van één specifieke plek op het eiwit, bekend als serine 312 in muizen. Als DUSP26 ontbrak, raakte deze plaats sterk gemodificeerd, steeg de p53‑activiteit en werden genen die celdood bevorderen aangezet. Om het belang van deze plek te bewijzen, bouwden de auteurs niercellen en muizen met een versie van p53 die op die plaats niet langer gemodificeerd kon worden. Die cellen en dieren waren veel resistenter tegen nierletsel, met minder stervende tubuluscellen en minder orgaandisfunctie, ook al bleven andere onderdelen van het p53‑systeem intact.
Van moleculair inzicht naar toekomstige therapieën
Gezamenlijk schetst het werk een duidelijke keten van gebeurtenissen: nierstress verhoogt DNA‑methylatie op het DUSP26‑gen, waardoor DUSP26‑eiwit in proximale tubuli afneemt. Met minder DUSP26 blijft p53 gefosforyleerd op een kritieke plaats, wordt actiever en drijft de expressie van genen die cellen naar de dood sturen. Het herstellen van DUSP26, of het nabootsen van zijn werking op die ene plek, dempt dit doodsprogramma en behoudt nierweefsel. Voor patiënten suggereert dit dat zorgvuldig ontworpen geneesmiddelen of gentargetbenaderingen die DUSP26‑activiteit versterken—of specifiek de fosforylering van p53 op deze plek verminderen—op termijn kunnen helpen nieren te beschermen tijdens operaties, chemotherapie of ernstige ziekte, en mogelijk ook andere organen tegen vergelijkbare vormen van acuut letsel kunnen behoeden.
Bronvermelding: Fu, Y., Xiang, Y., Han, Y. et al. DUSP26 protects against acute kidney injury by dephosphorylating p53 at serine 312. Nat Commun 17, 3208 (2026). https://doi.org/10.1038/s41467-026-69688-3
Trefwoorden: acuut nierletsel, nier tubulecellen, p53-signaleringsroute, epigenetische regulatie, celsterfte