Clear Sky Science · zh
由DNA胞嘧啶脱氨酶APOBEC3B对R环的编辑调节雌激素受体增强子活性
这项研究为何重要
许多乳腺癌依赖激素雌激素生长。同样负责开启关键基因的信号也能损伤DNA,促使肿瘤进化并产生耐药性。本研究揭示了一种天然存在的DNA编辑酶APOBEC3B如何在调控DNA开关——增强子处与雌激素受体协同作用。通过精确定位并说明该酶的作用方式,研究将正常的激素驱动基因调控与导致癌症基因组不稳定的突变和断裂联系起来,并提出针对激素依赖性肿瘤的新靶点思路。
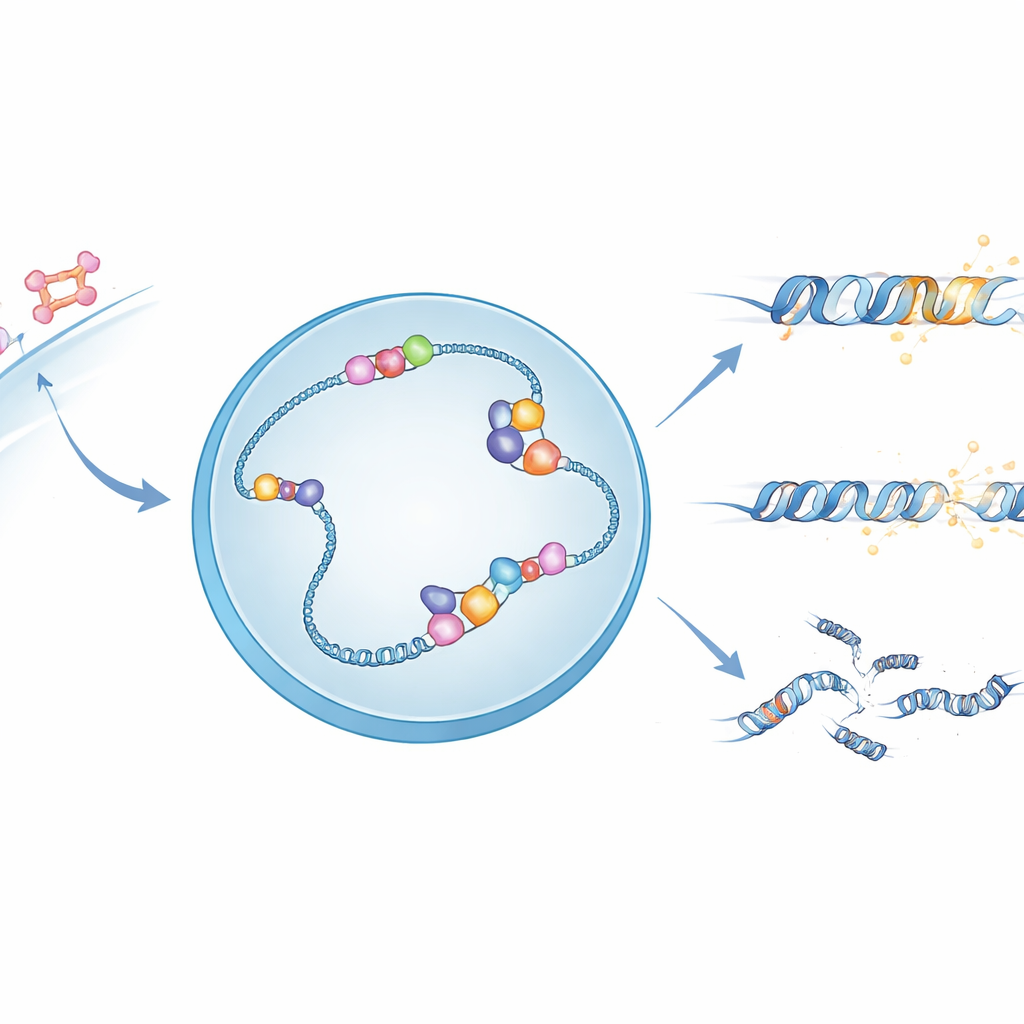
激素信号与脆弱的DNA结构
当雌激素进入细胞,它会激活雌激素受体,这种蛋白进入细胞核并结合特定DNA位点以调控邻近基因。在许多这些位点,DNA转录为RNA的过程中会形成不寻常的三链结构,称为R环——新合成的RNA与一条DNA链结合,另一条DNA链暴露出来。R环可以参与基因调控,但也使DNA更脆弱、易断裂。作者怀疑APOBEC3B(一种已知能化学修饰单链DNA的酶)可能利用R环中暴露的那条单链作为其偏好的作用底物。
绘制DNA编辑者作用的基因组地图
为了观察APOBEC3B在基因组中的足迹,研究组构建了基因工程乳腺癌细胞,阻断了一个关键的DNA修复途径——碱基切除修复。这使得APOBEC3B产生的化学编辑在被全基因组测序捕获前能保留更长时间。他们发现该酶留下的特征性突变并不聚集在编码蛋白的区域,而是集中在基因起始位点和增强子附近的调控DNA上,尤其是在那些早期复制且高度活跃的区域。这些被编辑的位置往往位于有利于R环形成的序列环境,暗示APOBEC3B与这些短暂出现的DNA:RNA结构密切相关。
直接证据:APOBEC3B在R环上作用
研究者随后使用两种基因组范围的检测方法同时观察APOBEC3B与R环。一种方法富集并拉下DNA:RNA杂交体,另一种捕获与带标签APOBEC3B结合的单链DNA。两者结合显示该酶正位于R环内部,并在暴露的DNA链上将胞嘧啶化学转化为尿嘧啶。当过表达能够消除R环的酶(RNase H1)时,APOBEC3B的结合明显下降,证实R环是其必需的停靠平台。在短暂的雌激素刺激下,启动子以及尤其是雌激素受体使用的高转录活性增强子处,R环和APOBEC3B结合均显著上升,将激素信号与R环依赖的DNA编辑爆发联系起来。
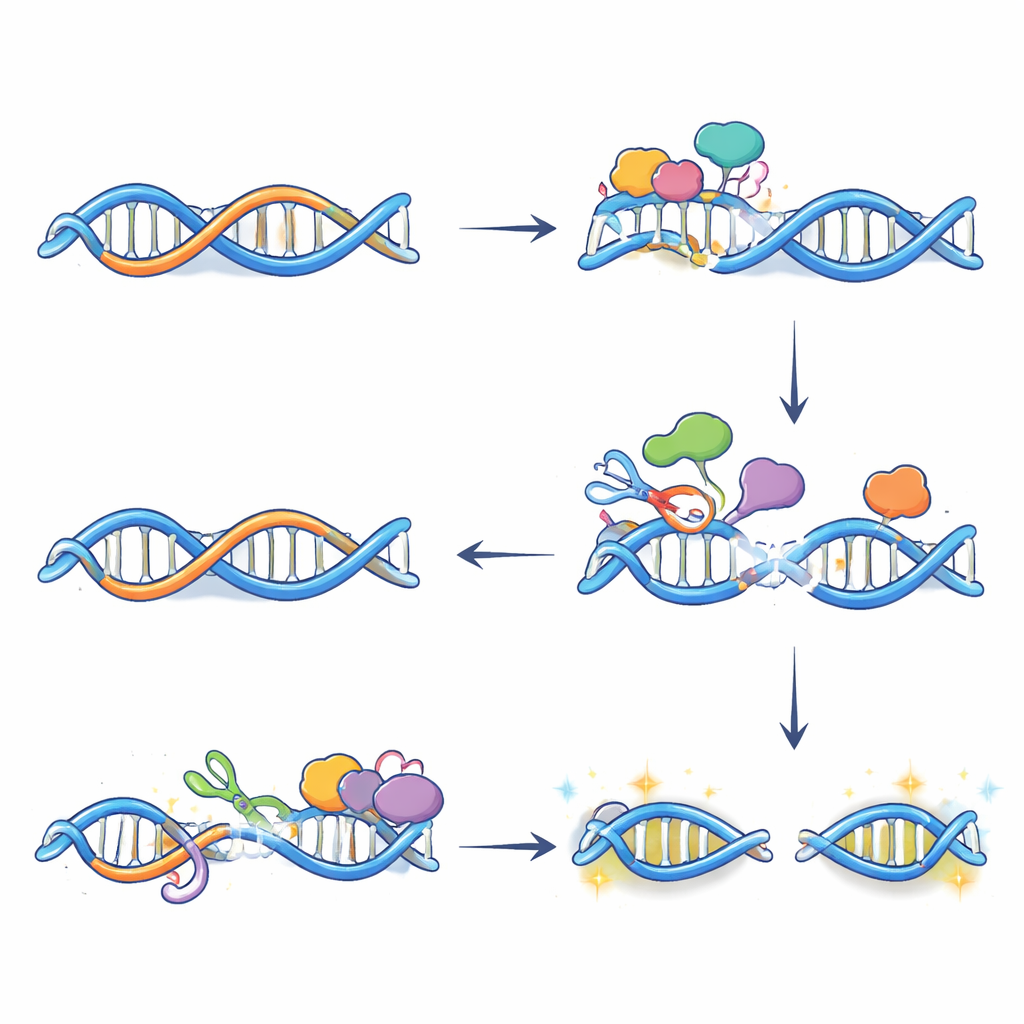
从化学修饰到DNA断裂与基因激活
仅有编辑并不会直接造成DNA断裂;损伤在修复系统处理这些被改变的碱基时产生。利用一种标记断裂DNA末端的技术,作者显示许多在雌激素处理后出现的双链断裂依赖于APOBEC3B,并且准确出现在R环与该酶重合的位点。进一步实验表明,两条修复通路——碱基切除修复和转录偶联核苷酸切除修复——在这些位点协同工作。它们分别在R环附近的相对DNA链上引入切口;当这些切口相遇时,形成完整断裂。阻断APOBEC3B活性或其中任一修复步骤都能减少这些断裂,并削弱许多雌激素响应基因通常在刺激后出现的表达激增,提示受控的DNA损伤实际上有助于在关键增强子处建立更开放、活跃的染色质状态。
对癌症与治疗的意义
这项工作将APOBEC3B描绘成在激素驱动的乳腺癌中具有双重作用的因子。在雌激素受体增强子附近的R环处编辑DNA,它有助于产生短暂的DNA断裂,重塑染色质并提升促生长基因的表达。与此同时,这些事件也留下伤痕——突变和结构改变——推动基因组不稳定性和肿瘤进化。理解激素信号、R环生物学与DNA编辑之间的耦合关系,突出了APOBEC3B及其相关修复步骤作为潜在药物靶点的价值。抑制这一环路可能既能减缓有害的基因激活,又能遏制导致对他莫昔芬等治疗产生耐药的遗传多样化进程。
引用: Zhang, C., Lu, Yj., Chen, B. et al. R-loop editing by DNA cytosine deaminase APOBEC3B modulates the activity of oestrogen receptor enhancers. Nat Commun 17, 2887 (2026). https://doi.org/10.1038/s41467-026-69679-4
关键词: 雌激素受体, APOBEC3B, R环, 乳腺癌, DNA 损伤